- 1.67 MB
- 2022-08-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
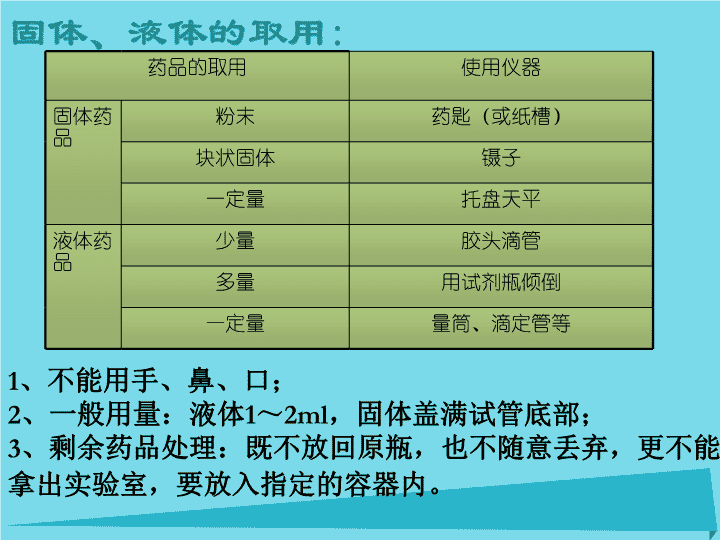
\n第一节 化学实验基本方法固体、液体的取用、物质的加热、以及基本仪器的使用。\n固体、液体的取用:药品的取用使用仪器固体药品粉末药匙(或纸槽)块状固体镊子一定量托盘天平液体药品少量胶头滴管多量用试剂瓶倾倒一定量量筒、滴定管等1、不能用手、鼻、口;2、一般用量:液体1~2ml,固体盖满试管底部;3、剩余药品处理:既不放回原瓶,也不随意丢弃,更不能拿出实验室,要放入指定的容器内。\n2、给试管里的药品加热,不需要垫石棉网,必须先进行预热,以免试管炸裂;物质的加热:1、绝对禁止用酒精灯引燃另一盏酒精灯;绝对禁止向燃着的酒精灯里添加酒精;用完酒精灯,必须用灯帽盖灭,不可用嘴吹灭;3、烧得很热的玻璃试管,不要立即用冷水冲洗,否则可能炸裂。\n1、可直接加热的仪器:2、需垫石棉网加热的仪器\n3、用于分离和加液的仪器4、计量仪器\n仪器的使用——托盘天平(1)调零防腐先调节天平,潮湿或腐蚀的药品必须放在玻璃器皿中称量,其他药品用大小一样质地相同的纸(2)左物右码左盘放称量物,右盘放砝码(3)先大后小取用砝码先取质量大的,再取小的(4)归零放盒称量完毕,应把游码移回零处,砝码放回砝码盒\n一、化学实验安全1、一些常用危险化学品的标志\n2、实验安全注意的问题:(1)遵守实验室规则(2)了解安全措施(3)掌握正确的操作方法①不用口接触实验室的仪器和药品。②加热液体的试管不准对着人,加热过程中的实验仪器不能直接放在实验台上,应放在石棉网上。怎样稀释浓硫酸?③稀释浓硫酸时一定要将浓硫酸缓慢注入水中并不断搅拌以散发热量。\n④若用加热的方法制取气体、用排水法收集气时,应先撤导管,再熄灯。(以免倒吸)氧气是如何制取的?收集的方法?实验结束时,是先撤导管还是先熄酒精灯?⑤做有毒气体实验时,应在通风橱中进行,并对尾气处理(吸收或点燃)。进行易燃易爆气体的实验应注意验纯,尾气应点燃或适当处理.\n3.化学实验过程中意外事故的处理①浓酸洒在实验台上,先用Na2CO3(或NaHCO3)中和,后用水冲洗;浓酸溅到皮肤上,先用干抹布拭去,再用水冲洗。严重的须就医。浓硫酸洒在实验台,或溅到皮肤上,如何处理?②浓碱洒在实验台上,先用稀醋酸中和,然后用水冲洗干净。浓碱沾在皮肤上,宜先用水冲洗,再涂硼酸溶液。严重时要就医。\n③酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑灭,烫伤(灼伤)要就医。④金属钠、非金属磷等失火要用沙土扑盖。\n广口瓶——一般存放固体试剂;细口瓶——一般存放液态试剂;棕色试剂瓶——一般存放一些见光易分解的物质;橡皮塞做瓶塞的试剂瓶——一般存放碱性物质。试剂瓶对所存放药品的要求:AgNO3HNO3HClO等\n二、混合物的分离和提纯\n自然界中的物质的存在形式纯净物(很少数)混合物(绝大多数)化学研究的物质的性质是研究纯净物的性质.分离、提纯混合物纯净物\n分离和提纯有什么不同?分离:是通过适当的方法,把混合物中的几种物质分开,每一组分都要保留下来,并恢复到原状态,得到比较纯的物质。提纯:指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去。\n水洗:用水冲洗利用物质的密度不同碎石、沙子:密度=2.5~3.5g/cm3金:密度=19.3g/cm3思考与交流:P5(铁的密度:7.7g/cm3)1、用手拣2、用水淘3、用磁铁4、用盐酸\n在分离和提纯物质时,要除掉杂质。化学上所指的杂质都是有害和无价值的吗?你能举例说明吗?\n我们在初中科学里也学过一些简单的实验方法,可用于混合物的分离和提纯,请同学们回忆一下,你了解哪些分离、提纯的方法?过滤、蒸发等【问题】\n粗盐成分:NaCl[CaCl2、MgCl2、硫酸盐、不溶性杂质]粗盐提纯:操作过程:溶解——过滤——蒸发\n▲过滤操作:操作时注意:一贴:滤纸要贴低于漏斗;二低:滤纸要低于漏斗边缘;溶液要低于滤纸.三靠:烧杯要紧在玻璃棒上;玻璃棒紧靠在滤纸三层处;漏斗下端紧靠在烧杯内壁.:通常用来分离液体和不溶的固体。一贴、二低、三靠\n▲蒸发操作:操作时注意:玻璃棒要不停的搅拌,防止局部沸腾;出现较多固体时停止加热,利用蒸发皿的余热使滤液蒸干.原理:利用加热的方法,使溶剂不断挥发而析出溶质的过程\n步骤现象1、溶解:搅拌溶解后,静置,沉淀,观察2、过滤:3、蒸发:溶解开始时,液体混浊,静置一段时间后,上层较清,下层较混浊,有沉淀物滤纸折好,放好安装仪器,慢慢过滤过滤后,滤液较澄清,滤纸上有沉淀物把所得滤液倒入蒸发皿,用酒精灯加热,同时用玻棒不断搅拌,待蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干得到较白净的固体(但质量比粗盐时少了些)\n思考:P6你认为通过上述操作得到的是比较纯的氯化钠吗?可能还有什么杂质没有除去?如何证明得到的盐中还含有硫酸根?还有CaCl2、MgCl2、硫酸盐\n可溶性物质在水溶液中以离子形式存在——————————————————溶液中有Na+、Cl-、SO42-、Mg2+、Ca2+对离子进行检验是利用离子间的特征反应,如利用生成气体,沉淀,溶液的颜色变化等明显的实验实验现象进行离子的确定.P7实验1-2SO42-离子的检验原理:\n先加入稀酸化,再加入可溶性钡盐溶液,如果出现不溶于稀酸的白色沉淀,则存在硫酸根离子。注意排除CO32-等离子的干扰,酸和钡盐的选择应该视具体情况而定,不能一成不变表述时应说明:选用什么试剂+出现什么现象+得出什么结论\n先加入稀HNO3酸化,再加入AgNO3溶液,如果出现不溶于稀硝酸的白色沉淀,则存在氯离子。\n有CaCl2、MgCl2、硫酸盐,怎样除去这些可溶性杂质?\n化学方法除杂的原则:不增(不引入新的杂质)、不减(不损耗样品)、易分(容易分离)、变化后再回到目标物.除杂的思路:选择那些易与杂质反应生成气体或沉淀的物质为试剂,然后再根据不增的原则确定加入试剂的顺序.为将杂质除尽,所加除杂试剂一般过量,过量的除杂试剂也要必须除尽.P7思考与交流\n杂质加入的试剂化学方程式硫酸盐MgCl2CaCl2NaOH+HCl=NaCl+H2ONa2CO3+2HCl=2NaCl+H2O+CO2↑BaCl2过量的处理:1、加入Na2CO3BaCl2+Na2CO3=BaCO3↓+2NaCl2、加入盐酸Na2CO3+2HCl=2NaCl+H2O+CO2↑BaCl2Na2SO4+BaCl2=BaSO4↓+2NaClNaOHMgCl2+2NaOH=Mg(OH)2↓+2NaClNa2CO3CaCl2+Na2CO3=CaCO3↓+2NaCl\n思考除了上述加试剂顺序外,还能不能有其他的顺序?\n二、混合物的分离和提纯1、蒸馏和萃取:(1)蒸馏:利用混合物中各组成成分的沸点不同,用加热的方法将其分离的过程。对象:沸点不同液态混合物;目的:分离(或除去)难挥发(或不挥发)的杂质。如:利用自来水制备蒸馏水\n蒸馏烧瓶冷凝管温度计尾接管冷水热水使用前要检查装置的气密性!\n投放沸石或瓷片温度计水银球处于支管口处水,下入上出操作注意:1、先通水,再加热2、全程严格控制好温度溶液体积不超过烧瓶体积2/3\n实验现象1、在试管中加入少量自来水,滴入几滴AgNO3(硝酸银)溶液和几滴稀硝酸。2、在烧瓶中加入约1/3体积的自来水,再加入几粒沸石,按图1-4连接好装置,向冷凝管中通入冷却水。加热烧瓶,弃去开始馏出的部分液体,用锥形瓶收集约10mL液体,停止加热。3、取少量蒸馏出的液体加入试管中,然后加入几滴AgNO3溶液和几滴稀硝酸。(得到的液体中含有Cl-吗?)加AgNO3后有白色沉淀生成,再加稀硝酸,白色沉淀不溶解,证明样品含有Cl-烧瓶中的水变成水蒸气,水蒸气经过冷凝管后变成液态水,流到锥形瓶里。加AgNO3和稀硝酸,没有白色沉淀生成,说明经蒸馏冷凝后得到的液体没有Cl-\n2、分离互不相溶、密度不同的混合物的方法一部分有机物溶剂Vs无机溶剂汽油煤油水植物油苯四氯化碳水密度比水小上层(密度比水大,下层)1、仪器——分液漏斗\n分液注意事项:(1)分液漏斗在使用前须检验是否漏水。(2)把盛有待分液体的分液漏斗放在铁架台的铁圈上,使漏斗颈末端紧贴在烧杯内壁,静置片刻。(3)下层液体从漏斗颈流出,上层液体须从漏斗上口倾倒出。\n(3)萃取:原理:利用混合物中一种溶质在互不相溶的两种溶剂中的溶解性不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来的方法。A和C组成溶液,加一种溶剂B,A易溶于B,A难溶于C,所以B可以把A在A和C组成的溶液中萃取出来.▲萃取剂的选择条件:1、萃取剂与原溶剂不混溶、不反应2、溶质在萃取剂中有较大的溶解度3、溶质不与萃取剂发生任何反应\n萃取实验步骤:装液---振荡---静置---分液主要仪器:分液漏斗P9实验1-4\n注意事项:(1)振荡时,须不断放气,以减少分液漏斗内的气压。(2)萃取原则:少量多次。(3)选择萃取剂的要求:与原溶剂不相溶;溶质在其中的溶解度要比在原溶剂中大;溶质、原溶剂、萃取剂之间均不反应。\n练习:选择萃取剂将碘水中的碘萃取出来,这种萃取剂具备的性质是( )A.不溶于水,且必须易与碘发生化学反应.B.不溶于水,且比水更容易使碘溶解C.不溶于水,且必须比水密度大D.不溶于水,且必须比水密度小B\n升华法:分离易升华的物质。碘、萘的提纯要提取食盐中的单质碘,你设计的最佳方法是什么?【问题】\n在实验里进行分液操作,下列仪器中用不着的是A.锥形瓶 B.分液漏斗 C.玻璃棒 D.温度计D已知丙酮通常是无色液体,不溶于水,密度小于1g/mL,沸点约为55℃.要从水与丙酮的混合物里将丙酮分离出来,下列方法最合理的是( )A.蒸馏 B.分液 C.过滤 D.蒸发B3.检验某未知溶液是否含有SO42-,下列操作最合理的是( )A. 先加稀硝酸酸化,再加Ba(NO3)2溶液.B. 加BaCl2溶液即可.C. 先加稀盐酸酸化,再加BaCl2溶液.D. 加Ba(NO3)2溶液即可C