- 543.50 KB
- 2022-08-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
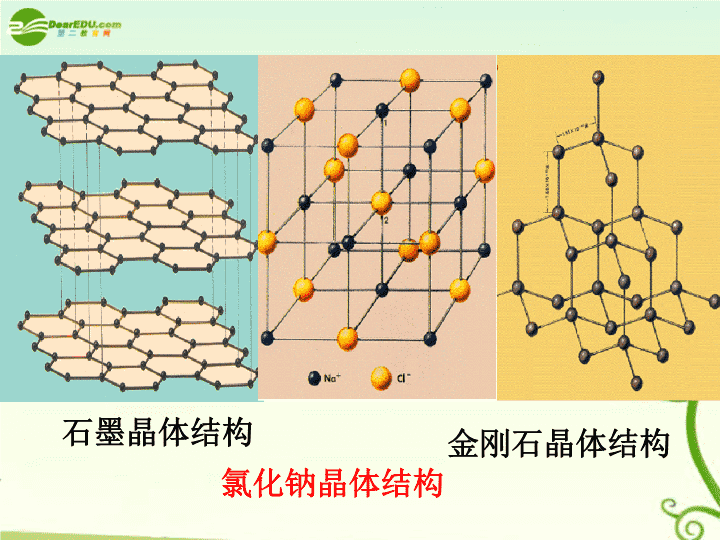
微粒之间的相互作用\n石墨晶体结构金刚石晶体结构氯化钠晶体结构\n直接相邻的两个或多个原子或离子之间强烈的相互作用,叫做化学键。化学键离子键共价键注意:⑴指直接相邻的原子或离子⑵强烈的相互作用金属键\n探究实验2Na+Cl22NaCl点燃鈉在氯气中燃烧实验方程式\neeeeeeCleNa-+e像这样阴阳离子通过静电作用结合在一起的化合物即离子化合物静电作用静电引力(阴阳离子间)静电斥力(原子核之间、电子之间)小动画\n离子键定义:阴阳离子间通过静电作用所形成的化学键叫做离子键。\n小结离子键成键微粒成键过程作用力成键元素阴阳离子得失电子形成阴阳离子静电作用活泼金属和活泼非金属化合物类型离子化合物组成物质大多数的盐、强碱、活泼金属氧化物\n说一说1.下列物质中含有离子键的是()A.H2OBCaCl2C.HClD.Cl22、下列叙述中正确的是()A.使阴阳离子结合成化合物的静电引力叫做离子键B.只有活泼金属与活泼非金属之间才能形成离子键C.离子化合物只有离子键D.离子所带电荷的符号和数目与原子成键时得失电子有关BD\n判断下列化合物哪些是离子化合物练习离子化合物CaCl2SO2H2ONa2ONaOHNH3CuSO4HCl\n在元素符号周围用“·”或“×”来表示原子最外层电子的式子,叫电子式。请写出11到18号元素原子的电子式和钠镁铝硫氯离子电子式\n⑶非金属阴离子的电子式要标[]及“电荷数”⑵简单金属阳离子的电子式就是其离子符号,而铵根离子因为是原子团需要加[]及“电荷数”注意⑴原子的书写要上下左右四面对称⑷离子化合物的书写就是阴阳离子的结合,但要注意离子要分开写,不可合并。\n[练习]写出下列微粒的电子式:硫原子,溴离子,氯化钠,氧化钠·S·····[Br]-····::用电子式可以直观地看到原子结构特点与化学键间的关系。表示出原子之间是怎样结合的NaCl∶∶·×[]∶-+Na+Na+O∶·×[]2-×·∶\n用电子式表示离子化合物形成过程:金属原子的电子式非金属原子电子式离子化合物电子式+例如:用电子式表示氯化钠的形成过程Cl·······[Cl]-····::Na·+→Na+\n·O·····[O]2-····::[练习]⑴用电子式表示氧化镁的形成过程·Mg·+→Mg2+⑵用电子式表示硫化钾的形成过程·S·····2K·+→K+[S]2-····::箭号左方相同的原子可以合并,箭号右方相同的离子不可以合并。K+注意\n本节总结:直接相邻的两个或多个原子或离子之间强烈的相互作用,叫做化学键。阴阳离子间通过静电作用所形成的化学键叫做离子键。含有离子键的化合物一定是离子化合物区分:用电子式表示物质用电子式表示物质形成过程