- 431.45 KB
- 2022-08-15 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
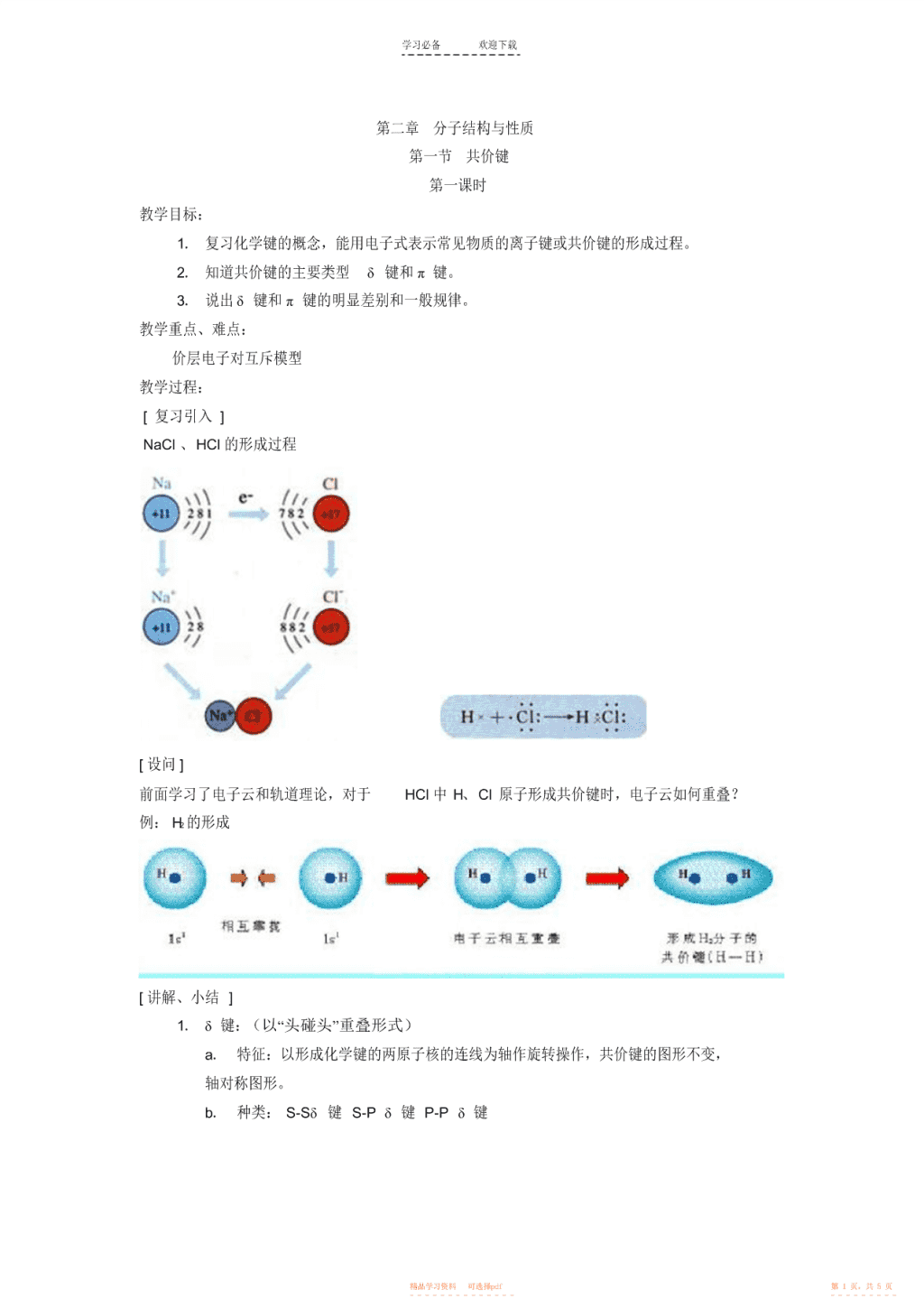
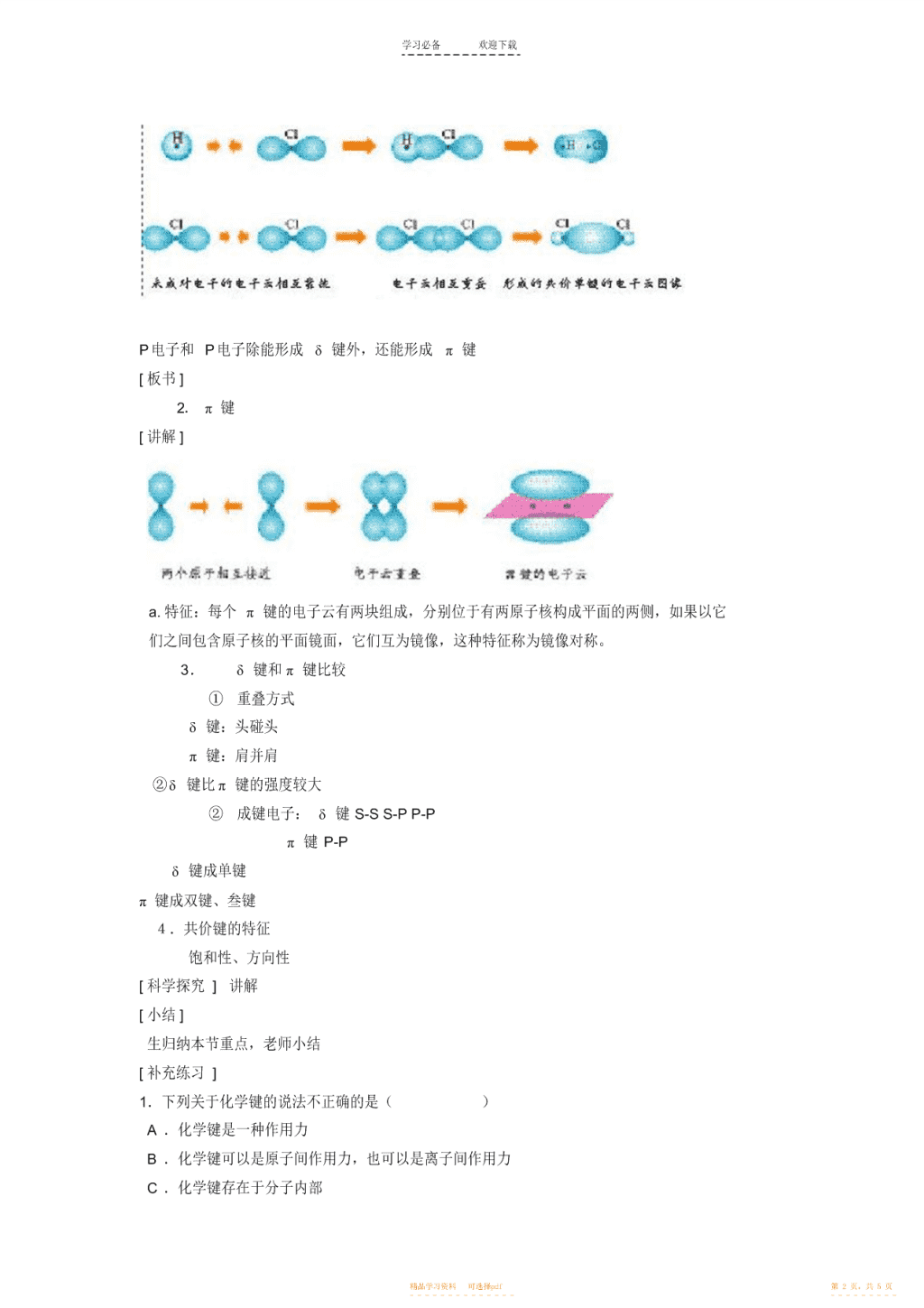
学习必备欢迎下载第二章分子结构与性质第一节共价键第一课时教学目标:1.复习化学键的概念,能用电子式表示常见物质的离子键或共价键的形成过程。2.知道共价键的主要类型δ键和π键。3.说出δ键和π键的明显差别和一般规律。教学重点、难点:价层电子对互斥模型教学过程:[复习引入]NaCl、HCl的形成过程[设问]前面学习了电子云和轨道理论,对于HCl中H、Cl原子形成共价键时,电子云如何重叠?例:H2的形成[讲解、小结]1.δ键:(以“头碰头”重叠形式)a.特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键的图形不变,轴对称图形。b.种类:S-Sδ键S-Pδ键P-Pδ键精品学习资料可选择pdf第1页,共5页-----------------------\n学习必备欢迎下载P电子和P电子除能形成δ键外,还能形成π键[板书]2.π键[讲解]a.特征:每个π键的电子云有两块组成,分别位于有两原子核构成平面的两侧,如果以它们之间包含原子核的平面镜面,它们互为镜像,这种特征称为镜像对称。3.δ键和π键比较①重叠方式δ键:头碰头π键:肩并肩②δ键比π键的强度较大②成键电子:δ键S-SS-PP-Pπ键P-Pδ键成单键π键成双键、叁键4.共价键的特征饱和性、方向性[科学探究]讲解[小结]生归纳本节重点,老师小结[补充练习]1.下列关于化学键的说法不正确的是()A.化学键是一种作用力B.化学键可以是原子间作用力,也可以是离子间作用力C.化学键存在于分子内部精品学习资料可选择pdf第2页,共5页-----------------------\n学习必备欢迎下载D.化学键存在于分子之间2.对δ键的认识不正确的是()A.δ键不属于共价键,是另一种化学键B.S-Sδ键与S-Pδ键的对称性相同C.分子中含有共价键,则至少含有一个δ键D.含有π键的化合物与只含δ键的化合物的化学性质不同3.下列物质中,属于共价化合物的是()A.I2B.BaCl2C.H2SO4D.NaOH4.下列化合物中,属于离子化合物的是()A.KNO3B.BeClC.KO2D.H2O25.写出下列物质的电子式。H2、N2、HCl、H2O6.用电子式表示下列化合物的形成过程HCl、NaBr、MgF2、Na2S、CO2第二章分子结构与性质第一节共价键第二课时[教学目标]:1.认识键能、键长、键角等键参数的概念2.能用键参数――键能、键长、键角说明简单分子的某些性质3.知道等电子原理,结合实例说明“等电子原理的应用”[教学难点、重点]:键参数的概念,等电子原理[教学过程]:[创设问题情境]精品学习资料可选择pdf第3页,共5页-----------------------\n学习必备欢迎下载N2与H2在常温下很难反应,必须在高温下才能发生反应,而F2与H2在冷暗处就能发生化学反应,为什么?[学生讨论][小结]引入键能的定义二、键参数1.键能①概念:气态基态原子形成1mol化学键所释放出的最低能量。②单位:kJ/mol[生阅读书33页,表2-1]回答:键能大小与键的强度的关系?(键能越大,化学键越稳定,越不易断裂)键能化学反应的能量变化的关系?(键能越大,形成化学键放出的能量越大)③键能越大,形成化学键放出的能量越大,化学键越稳定。2.键长①概念:形成共价键的两原子间的核间距-12②单位:1pm(1pm=10m)④键长越短,共价键越牢固,形成的物质越稳定多原子分子的形状如何?就必须要了解多原子分子中两共价键之间的夹角。3.键角:多原子分子中的两个共价键之间的夹角。例如:CO2结构为O=C=O,键角为180°,为直线形分子。H2O键角105°V形CH4键角109°28′正四面体[小结]键能、键长、键角是共价键的三个参数键能、键长决定了共价键的稳定性;键长、键角决定了分子的空间构型。三、等电子原理1.等电子体:原子数相同,价电子数也相同的微粒。+如:CO和N2,CH4和NH42.等电子体性质相似[补充练习]1.下列分子中,两核间距最大,键能最小的是()A.H2B.BrC.ClD.I22.下列说法中,错误的是()A.键长越长,化学键越牢固B.成键原子间原子轨道重叠越多,共价键越牢固精品学习资料可选择pdf第4页,共5页-----------------------\n学习必备欢迎下载C.对双原子分子来讲,键能越大,含有该键的分子越稳定D.原子间通过共用电子对所形成的化学键叫共价键3.能够用键能解释的是()A.氮气的化学性质比氧气稳定B.常温常压下,溴呈液体,碘为固体C.稀有气体一般很难发生化学反应D.硝酸易挥发,硫酸难挥发-4.与NO3互为等电子体的是()A.SO3B.BF3C.CH4D.NO22-5.根据等电子原理,下列分子或离子与SO4有相似结构的是()A.PCl5B.CCl4C.NF3D.N6.由表2-1可知.H-H的键能为436kJ/mol.它所表示的意义是___________.如果要使1molH2分解为2molH原子,你认为是吸收能量还是放出能量?____.能量数值____.当两个原子形成共价键时,原子轨道重叠的程度越大,共价键的键能____,两原子核间的平均距离――键长____.7.根据课本中有关键能的数据,计算下列反应中的能量变化:(1)N2(g)+3H2(g)====2NH3(g);⊿H=(2)2H2(g)+O2(g)===2H2O(g);⊿H=精品学习资料可选择pdf第5页,共5页-----------------------