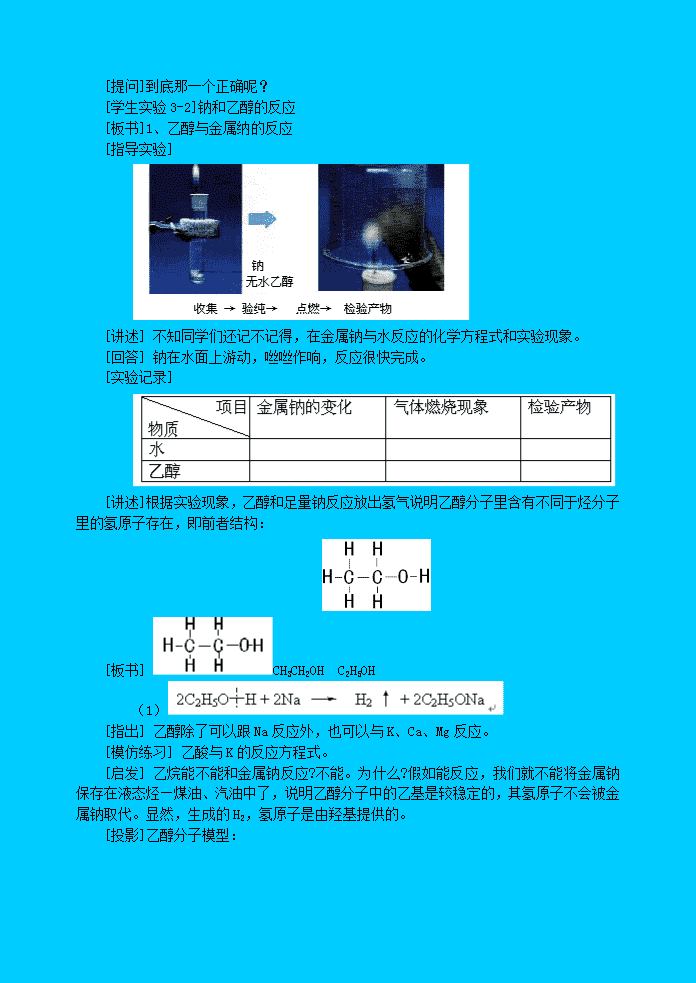
- 626.00 KB
- 2022-08-17 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
乙醇教学目标:1.结合生活经验和化学实验,了解乙醇、乙酸的组成和主要性质,加深认识这些物质对于人类日常生活、身体健康的重要性。2.从这两种衍生物的组成、结构和性质出发,让学生知道官能团对有机物性质的重要影响,建立“(组成)结构──性质──用途”的有机物学习模式。3.在学生初中知识的基础上,突出从烃到烃的衍生物的结构变化,强调官能团与性质的关系,在学生的头脑中逐步建立烃基与官能团位置关系等立体结构模型,教学重点:官能团的概念、乙醇的组成、乙醇的取代反应与氧化反应、教学难点:使学生建立乙醇和乙酸分子的立体结构模型,并能从结构角度初步认识乙醇的氧化反应。课时:乙醇1课时、教学方法:讲授、学生制作与实验、小组合作、参观、调查、实验条件控制、类比、归纳、假说、模型、讨论、科学抽象等。教学过程:[引课]成功、快乐的时候,人们会想到它——会须一饮三百杯;失败、忧愁的时候,人们也会想到它——举杯浇愁愁更愁。它就是酒,俗名酒精,学名乙醇。日常生活离不开油、盐、酱、醋,乙醇和醋是较常见的有机物。[板书]第三节生活中两种常见的有机物[过渡]我国是世界上最早学会酿酒和蒸馏技术的国家,酿酒的历史已有4000多年,我国的酒文化丰富多彩,著名诗句“借问酒家何处有,牧童遥指杏花村”、“葡萄美酒夜光杯”等早已脍炙人口。随着科学技术的进步,人们逐渐加深了对乙醇的认识,发现乙醇有相当广泛的用途(展示乙醇实物,嗅气味,学生回答,教师边问边板书)[板书]物理性质:无色、透明,具有特殊香味的液体,密度小于水沸点低于水,易挥发。[讲述]乙醇可作溶剂,溶解多种有机物和无机物,与水以任意比互溶。互溶的混合物,在分离上是比较困难的,但也是可以分离的。[设问]两种不同的液体互溶在一起时,可用什么方法分离?[讲述]用分馏的方法只能得到96%的高浓度乙醇,要得到无水乙醇还得加新制的生石灰,使水与之反应生成一种难挥发的Ca(OH)2,再蒸馏。[设疑]乙醇分子分子式C2H6O,分子中有6个氢原子,根据我们学过的碳四价的原则,谁能写出其可能的结构?[投影]乙醇可能的结构式:或者\n[提问]到底那一个正确呢?[学生实验3-2]钠和乙醇的反应[板书]1、乙醇与金属纳的反应[指导实验][讲述]不知同学们还记不记得,在金属钠与水反应的化学方程式和实验现象。[回答]钠在水面上游动,咝咝作响,反应很快完成。[实验记录][讲述]根据实验现象,乙醇和足量钠反应放出氢气说明乙醇分子里含有不同于烃分子里的氢原子存在,即前者结构:[板书]CH3CH2OHC2H5OH(1)[指出]乙醇除了可以跟Na反应外,也可以与K、Ca、Mg反应。[模仿练习]乙酸与K的反应方程式。[启发]乙烷能不能和金属钠反应?不能。为什么?假如能反应,我们就不能将金属钠保存在液态烃—煤油、汽油中了,说明乙醇分子中的乙基是较稳定的,其氢原子不会被金属钠取代。显然,生成的H2,氢原子是由羟基提供的。[投影]乙醇分子模型:\n[讲述]不知同学们还记不记得,在金属钠与水反应的化学方程式和实验现象。[实验]水和金属钠[讲述]钠在水面上游动,咝咝作响,反应很快完成。[板书]2Na+2H2O=2NaOH+H2↑[比较]1,密度2.速度[板书]乙醇较水还难电离。[讲述]乙醇可以看成是乙烷分子里的氢原子被羟基取代后的产物,一氯甲烷是甲烷分子上的一个氢原子被氯原子取代而得到。一氯甲烷可以看成是甲烷的衍生物。l,2-二溴乙烷既可以看成是乙烯的衍生物,又可以看成乙烷的衍生物。硝基苯可以看成是苯的衍生物。由此我们可以将烃的衍生物定义为:[板书]从结构上说,都可以看作是由烃衍变而来的有机物,这类有机物叫做烃的衍生物。[设疑]为什么要“从结构上说?”[解释]烃的衍生物并非一定要由烃通过取代、加成等方法来得到;例如乙醇可以由乙烯和水加成得到,也可以通过粮食发酵得到。[过渡]当烃分子上的氢原子被这些原子或原子团取代后,物质的一些性质都将发生很大变化,可以说,这些原子或原子团对烃的衍生物的性质起了决定性的作用。由于它决定了这个物质的化学特性。所以在化学上把这种原子或原子团叫做官能团。[板书](2)官能团能够决定化合物化学特性的原子或原子团,叫做官能团。例甚至[讲述]我们理解了官能团这个概念后,就应该明白这样一个道理,学习烃的衍生物不必一个一个物质地去学习,而是应该像前面研究烷烃时学习它的代表物甲烷;学习它的代表物以达到触类旁通的目的。[演示实验]将一束光亮的铜丝伸入到酒精等火焰上灼烧,观察内焰与外焰铜丝变化情况。[板书]2、乙醇的氧化反应[指出]对于乙醇的氧化反应,结合学生的日常经验,简单说明乙醇的燃烧是一个剧烈的氧化反应。当条件改变时,同样是乙醇和氧气,发生的氧化反应却大相径庭。[学生实验3-3]乙醇的催化氧化实验。提示学生注意观察以下要点:变黑的铜丝插入乙醇后,颜色如何变化?反复操作后,试管内液体的气味有何变化?[投影]\n[板书]2CH3CH2OH+O22CH3CHO+2H2O[思考](CH3)2CHOH(CH3)3COH能否被催化氧化。[阅读]P67资料卡片-生命不能承受之醉[小结]略[课堂练习]、第三节生活中两种常见的有机物第一课时教案第一课时教学目标:1.结合生活经验和化学实验,了解乙醇的组成和主要性质,加深认识这些物质对于人类日常生活、身体健康的重要性。2.从乙醇组成、结构和性质出发,让学生知道官能团对有机物性质的重要影响,建立“(组成)结构──性质──用途”的有机物学习模式。3.在学生初中知识的基础上,突出从烃到烃的衍生物的结构变化,强调官能团与性质的关系,在学生的头脑中逐步建立烃基与官能团位置关系等立体结构模型,教学重点:官能团的概念、乙醇的组成、乙醇的取代反应与氧化反应教学难点:使学生建立乙醇分子的立体结构模型,并能从结构角度初步认识乙醇的氧化反应。课时:1课时。教学方法:讲授、学生制作与实验、小组合作、参观、调查、实验条件控制、类比、归纳、假说、模型、讨论、科学抽象等。教学过程:[引课]成功、快乐的时候,人们会想到它——会须一饮三百杯;失败、忧愁的时候,人们也会想到它——举杯浇愁愁更愁。它就是酒,俗名酒精,学名乙醇。[板书]第三节生活中两种常见的有机物[过渡]我国是世界上最早学会酿酒和蒸馏技术的国家,酿酒的历史已有4000多年,我国的酒文化丰富多彩,著名诗句“借问酒家何处有,牧童遥指杏花村”、“葡萄美酒夜光杯”等早已脍炙人口。随着科学技术的进步,人们逐渐加深了对乙醇的认识,发现乙醇有相当广泛的用途\n(展示乙醇实物,嗅气味,学生回答,教师边问边板书)[板书]一:物理性质:无色、透明,具有特殊香味的液体,密度小于水沸点低于水,易挥发。[讲述]乙醇可作溶剂,溶解多种有机物和无机物,[设疑]乙醇分子分子式C2H6O,分子中有6个氢原子,根据我们学过的碳四价的原则,谁能写出其可能的结构?[投影]乙醇可能的结构式:或者[提问]到底那一个正确呢?[学生实验3-2]钠和乙醇的反应[指导实验][讲述]不知同学们还记不记得,在金属钠与水反应的化学方程式和实验现象。[回答]钠在水面上游动,咝咝作响,反应很快完成。[实验记录][讲述]根据实验现象,乙醇和足量钠反应放出氢气说明乙醇分子里含有不同于烃分子里的氢原子存在,即前者结构:[板书]二、化学性质1、分子结构[板书]CH3CH2OHC2H5OH2、乙醇与金属钠反应[启发]乙烷能不能和金属钠反应?不能。为什么?假如能反应,我们就不能将金属钠保存在液态烃—煤油、汽油中了,说明乙醇分子中的乙基是较稳定的,其氢原子不会被金属钠取代。显然,生成的H2,氢原子是由羟基提供的。[讲述]不知同学们还记不记得,在金属钠与水反应的化学方程式和实验现象。[实验]水和金属钠[讲述]钠在水面上游动,咝咝作响,反应很快完成。\n[板书]2Na+2H2O=2NaOH+H2↑[比较]1,密度2.速度[板书]乙醇较水还难电离。[讲述]乙醇可以看成是乙烷分子里的氢原子被羟基取代后的产物,一氯甲烷是甲烷分子上的一个氢原子被氯原子取代而得到。一氯甲烷可以看成是甲烷的衍生物。l,2-二溴乙烷既可以看成是乙烯的衍生物,又可以看成乙烷的衍生物。硝基苯可以看成是苯的衍生物。由此我们可以将烃的衍生物定义为:[板书]从结构上说,都可以看作是由烃衍变而来的有机物,这类有机物叫做烃的衍生物。[过渡]当烃分子上的氢原子被这些原子或原子团取代后,物质的一些性质都将发生很大变化,可以说,这些原子或原子团对烃的衍生物的性质起了决定性的作用。由于它决定了这个物质的化学特性。所以在化学上把这种原子或原子团叫做官能团。[板书]3官能团能够决定化合物化学特性的原子或原子团,叫做官能团。例甚至[讲述]我们理解了官能团这个概念后,就应该明白这样一个道理,学习烃的衍生物不必一个一个物质地去学习,而是应该像前面研究烷烃时学习它的代表物甲烷;学习它的代表物以达到触类旁通的目的。[板书]4、乙醇的氧化反应(1)燃烧C2H5OH+3O2点燃2CO2+3H2O[指出]对于乙醇的氧化反应,结合学生的日常经验,简单说明乙醇的燃烧是一个剧烈的氧化反应。当条件改变时,同样是乙醇和氧气,发生的氧化反应却大相径庭。[学生实验3-3]乙醇的催化氧化实验。提示学生注意观察以下要点:变黑的铜丝插入乙醇后,颜色如何变化?反复操作后,试管内液体的气味有何变化?[板书](2)催化氧化2CH3CH2OH+O22CH3CHO+2H2OCH3CH2OH强氧化剂2CH3COOH[阅读]P74资料卡片[小结]略[课堂练习]板书设计乙醇一:物理性质:二、化学性质1、分子结构\nCH3CH2OHC2H5OH2、乙醇与金属钠反应2Na+2H2O=2NaOH+H2↑乙醇较水还难电离可以看作是羟基代替乙烷中的一个氢原子由烃衍变而来的有机物,可以叫做烃的衍生物3官能团能够决定化合物化学特性的原子或原子团,叫做官能团。例甚至4、乙醇的氧化反应(1)燃烧C2H5OH+3O2点燃2CO2+3H2O(2)催化氧化2CH3CH2OH+O22CH3CHO+2H2OCH3CH2OH强氧化剂2CH3COOH乙醇评课提纲今天我讲解了高中化学必修2第三章第三节第一课时乙醇,现就本节课进行反思。一、教材地位和作用乙醇在有机物的相互转化中处于核心地位、起桥梁作用。学好本节内容对学习其它烃的衍生物具有指导性的作用。同时乙醇与我们的生产、生活联系非常紧密,是一种具有广泛用途的有机物。因此,本节内容是全章的重点之一。在初中化学中,已介绍了乙醇的组成、燃烧及主要用途等知识,在此基础上,本节教材首先介绍了乙醇的结构式,将后面所介绍的乙醇的化学性质与官能团联系起来,然后重点介绍乙醇与钠的反应、乙醇的催化氧化化学性质,在介绍乙醇与钠的反应时,教材将乙醇与水作了比较,说明乙醇比水更难电离出氢,这是本章教材中一系列比较有关电离出氢离子难易程度的第一例,它和苯酚与醇、碳酸、乙酸的比较,共同形成了电离理论的知识系列,这条线从另一个角度将乙醇、苯酚、乙酸串了起来。本节知识是高考必考、常考知识,常在有机推断题中出现。二、教学过程\n本节课我从古代与酒有关的诗句入手,引入新课。通过初中所学乙醇化学式和学生已具备有机物知识,引出乙醇可能结构式。再通过实验乙醇和金属钠反应,确定乙醇结构式。通过比较乙醇和金属钠反应现象与水和金属钠反应现象不同,得出乙醇比金属钠难电离的结论最后讲解乙醇的氧化反应,包括燃烧和催化氧化,重点是分析催化氧化反应。演示实验,并分析乙醇和金属钠反应、催化氧化的断键机理,为以后有机物学习打下扎实基础。三、自评新教材我没有接触过,本节课我在讲解过程中,由于紧张,实验作得不太成功,另外讲解乙醇断键过程,由于准备不足,讲解不够细致,这是本节课的最大遗憾。四、反思对于以实验为主