- 756.00 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
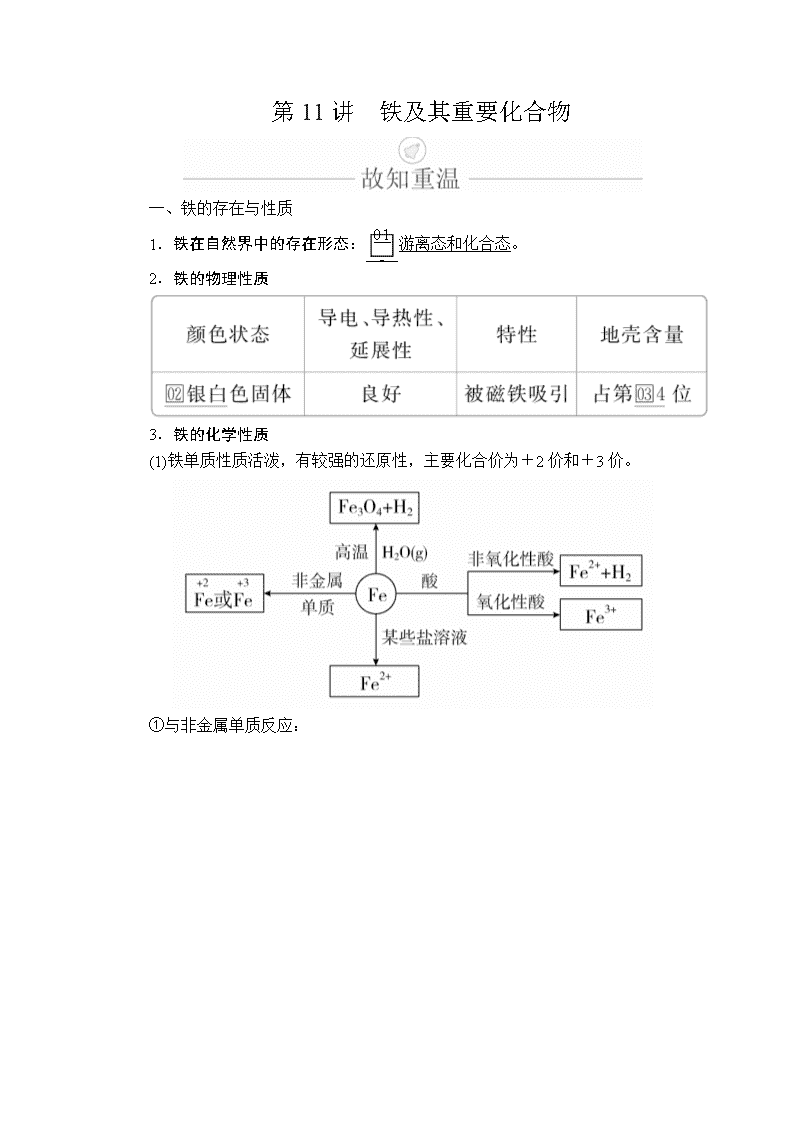
第11讲 铁及其重要化合物
一、铁的存在与性质
1.铁在自然界中的存在形态:游离态和化合态。
2.铁的物理性质
3.铁的化学性质
(1)铁单质性质活泼,有较强的还原性,主要化合价为+2价和+3价。
①与非金属单质反应:
②与水的反应:常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4H2O(g)Fe3O4+4H2。
(2)与酸的反应
(3)与某些盐溶液的反应
①与CuSO4溶液反应的离子方程式:
Fe+Cu2+===Fe2++Cu。
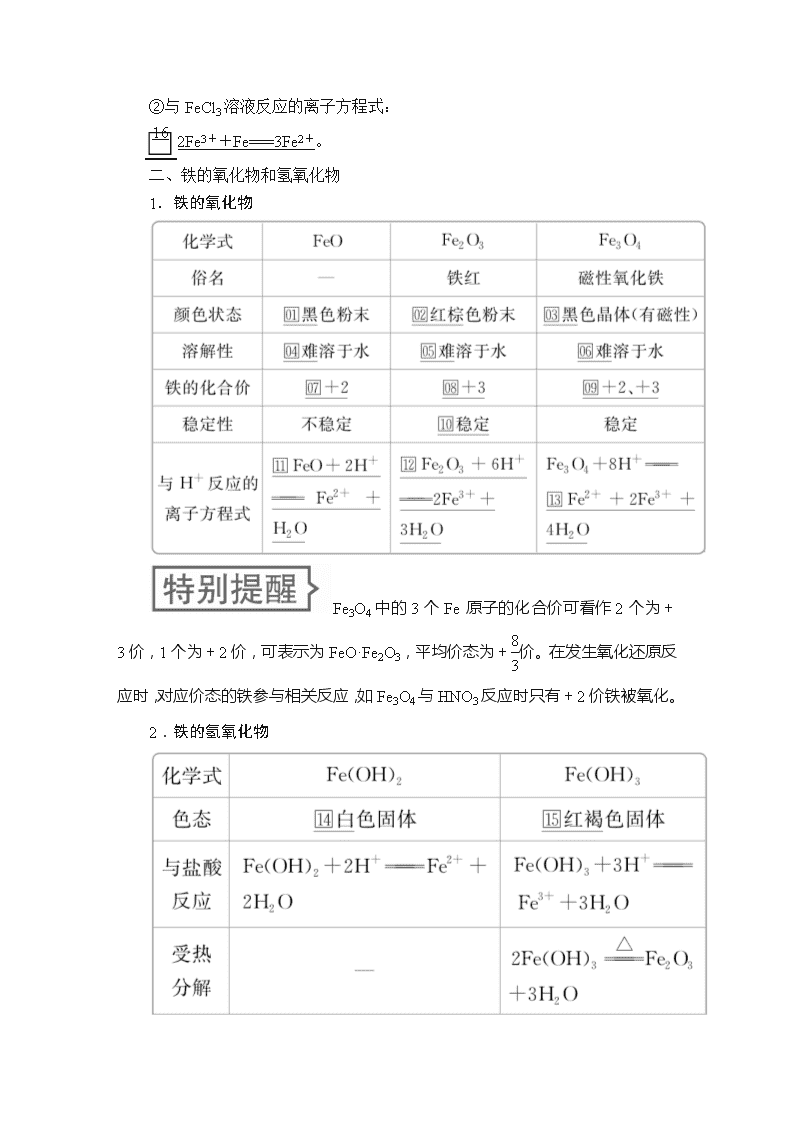
②与FeCl3溶液反应的离子方程式:
2Fe3++Fe===3Fe2+。
二、铁的氧化物和氢氧化物
1.铁的氧化物
Fe3O4中的3个Fe原子的化合价可看作2个为+3价,1个为+2价,可表示为FeO·Fe2O3,平均价态为+价。在发生氧化还原反应时,对应价态的铁参与相关反应,如Fe3O4与HNO3反应时只有+2价铁被氧化。
2.铁的氢氧化物
三、亚铁盐、铁盐的化学性质
1.亚铁盐
含有Fe2+的溶液呈浅绿色,既有氧化性,又有还原性。
(1)氧化性:Fe2+与Zn反应的离子方程式:
Zn+Fe2+===Fe+Zn2+。
(2)还原性
①向FeCl2溶液中滴入几滴KSCN溶液,再加入氯水(或通入Cl2),若溶液变红色,证明Fe2+具有还原性。反应原理:2Fe2++Cl2===2Fe3++2Cl-。
②向少量酸性KMnO4溶液中加入FeCl2溶液,若溶液紫红色褪去,证明Fe2+具有还原性。反应原理:
MnO+5Fe2++8H+===5Fe3++Mn2++4H2O。
2.铁盐
(1)特性:含有Fe3+的盐溶液遇到SCN-时变成红色。
(2)氧化性:含Fe3+的溶液呈棕黄色,Fe3+具有较强的氧化性。
①向FeCl3溶液中滴入几滴KSCN溶液,再加入过量活泼金属(如Fe),若溶液红色褪去,证明Fe3+具有氧化性。反应原理:2Fe3++Fe===3Fe2+。
②向FeCl3溶液中加入淀粉KI溶液,若溶液变成蓝色,证明Fe3+具有氧化性。反应原理:2Fe3++2I-===I2+2Fe2+。
③向FeCl3溶液中通入H2S气体,若出现黄色浑浊,证明Fe3+
具有氧化性。反应原理:2Fe3++H2S===2Fe2++S↓+2H+。
(3)FeCl3易水解:将其饱和溶液滴入沸水中制备胶体的化学方程式为FeCl3+3H2OFe(OH)3(胶体)+3HCl。
3.Fe2+、Fe3+的相互转化
Fe2+Fe3+
上述转化中标号反应的离子方程式为
①2Fe2++Br2===2Fe3++2Br-;
②2Fe3++Fe===3Fe2+。
1.判断正误,正确的画“√”,错误的画“×”,并指明错因。
(1)常温下,将铁片浸入足量浓硫酸中,铁片不溶解,说明常温下,铁与浓硫酸不发生化学反应。(×)
错因:Fe常温下遇浓H2SO4发生钝化。
(2)将铁屑放入稀HNO3中,证明Fe比H2活泼。(×)
错因:Fe与HNO3反应不产生H2。
(3)用NaOH溶液可以除去氧化铁中混有的二氧化硅。(√)
错因:___________________________________________________________
(4)Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。(×)
错因:Fe与I2反应生成FeI2。
(5)FeCl3腐蚀Cu制印刷电路板是由于铁比铜的金属性强。(×)
错因:Fe3+与Cu反应生成Fe2+和Cu2+,证明Fe3+的氧化性大于Cu2+,不能证明Fe的金属性比Cu强。
(6)Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+===2Fe3++2H2O。(√)
错因:___________________________________________________________
2.教材改编题
(人教必修一P63T7)要证明某溶液中不含Fe3+而可能含Fe2+,进行如下实验操作时,最佳顺序是( )
①加足量氯水 ②加足量KMnO4溶液 ③加少量KSCN溶液
A.①② B.③②
C.③① D.①②③
答案 C
考点 铁的性质和用途
[典例1] 在一定量的稀HNO3中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。请将正确答案的序号填在相应的横线上。
①Fe3+ ②Fe2+ ③Fe、Fe2+ ④Fe2+、Fe3+
(1)AB段铁元素以________形式存在。
(2)BC段铁元素以________形式存在。
(3)CD段铁元素以________形式存在。
解析 向稀HNO3中加入铁粉,开始时稀HNO3过量应生成Fe3+,随加入铁粉量的增加,HNO3反应完全后,发生反应2Fe3++Fe===3Fe2+,最后全部转化为Fe2+。
答案 (1)① (2)④ (3)③
名师精讲
1.铁与稀硝酸反应产物中铁元素价态的判断方法
(1)当HNO3过量时:反应原理:Fe+4HNO3===Fe(NO3)3+NO↑+2H2O,铁元素的存在形式为Fe3+,铁元素的价态为+3价。
(2)当Fe过量时:铁被硝酸氧化为Fe3+,然后Fe3+被剩余的铁还原为Fe2+,也就是说最终得到亚铁盐,总方程式:3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O。
(3)当<<时:铁元素的存在形式为Fe2+和Fe3+,铁元素的价态为+2、+3价。
(4)用数轴法表示,铁与硝酸的用量比与反应产物的关系:
2.铁与硫酸、硝酸的混酸反应顺序总结
足量铁与稀硫酸、稀硝酸的混合溶液反应,则可利用离子反应分析,依次发生反应:Fe+NO+4H+===Fe3++NO↑+2H2O、2Fe3++Fe===3Fe2+、Fe+2H+===Fe2++H2↑(若H+量不足,该反应不再发生)。
1.下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,纯铁易被腐蚀
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④铁能在氧气中剧烈燃烧
⑤铁与硝酸反应的产物仅是Fe(NO3)3
⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④
C.②⑤ D.④⑥
答案 B
解析 纯铁的抗腐蚀能力较强;铁位于元素周期表的第Ⅷ族,而不是第ⅧB族;铁与强氧化剂反应,能被氧化为Fe3+,但若铁过量,则Fe3+被Fe还原为Fe2+,所以,Fe与HNO3反应的产物可能因铁过量而生成Fe(NO3)2;FeCl2、Fe(OH)3可分别通过化合反应Fe+2FeCl3===3FeCl2、4Fe(OH)2+O2+2H2O===4Fe(OH)3制得。故B正确。
2.向含有1 mol HNO3和1 mol H2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是( )
A.a表示Fe3+的关系曲线
B.n1=0.75
C.P点时,n(Fe2+)=0.5625 mol
D.向P点溶液中加入铜粉,最多可溶解14.4 g
答案 C
解析 该反应可以看作两步:①Fe+4H++NO===Fe3++NO↑+2H2O,硝酸根离子过量,氢离子不足;②2Fe3++Fe===3Fe2+。a表示Fe3+的关系曲线,故A正确;溶液中共有3 mol H+参加反应,消耗铁为0.75 mol,B正确;P点n(Fe2+)=n(Fe3+),二者均为0.45 mol,C错误;剩余0.45 mol Fe3+,消耗0.225 mol铜,质量为14.4 g,D正确。
考点 铁的氧化物、氢氧化物
[典例2] 用下面两种方法可以制得白色的Fe(OH)2沉淀。
Ⅰ.方法一:用FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)除去蒸馏水中溶解的O2常采用________的方法。
(2)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是_________________。
Ⅱ.方法二:在如图所示装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
(1)在试管Ⅰ里加入的试剂是____________。
(2)在试管Ⅱ里加入的试剂是____________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_______________________________________________
_____________________________________________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是______________________________________________________________________
____________________________________________________________________。
解析 Ⅰ.方法一:(1)气体的溶解度是随温度升高而降低的,所以煮沸后的蒸馏水中溶解的O2变少。
(2)避免生成的Fe(OH)2被空气(氧气)氧化。
Ⅱ.方法二:试管Ⅱ是开口式的,无法用产生的气体将溶液压入试管Ⅰ中,所以应在试管Ⅰ中制取FeSO4,而在试管Ⅱ中盛NaOH溶液。将Fe与稀H2SO4放入试管Ⅰ后,产生的H2可从试管Ⅰ内短管处排出试管Ⅰ内的空气,经过止水夹进入试管Ⅱ内的NaOH溶液中,再排尽NaOH溶液和试管Ⅱ内的空气,然后关闭止水夹,试管Ⅰ内产生的H2无法逸出,压强增大,将FeSO4溶液通过长导管压入试管Ⅱ内的NaOH溶液中,在此过程中,液体都处于H2环境中,从而避免了空气中的O2将反应生成的Fe(OH)2氧化成Fe(OH)3。
答案 Ⅰ.(1)煮沸
(2)避免生成的Fe(OH)2沉淀接触O2
Ⅱ.(1)稀H2SO4、铁屑
(2)NaOH溶液
(3)检验试管Ⅱ出口处排出H2的纯度,当排出的H2纯净时,要夹紧止水夹
(4)试管Ⅰ中反应生成的H2将所用溶液和装置内的空气排尽,且外界空气不容易进入装置,可防止白色的Fe(OH)2沉淀被氧化
名师精讲
1.制备Fe(OH)2的关键与方法
由于Fe(OH)2具有很强的还原性,易被氧化为Fe(OH)3,在实验室中制备Fe(OH)2,并使Fe(OH)2长时间保持白色沉淀状态,成为物质制备实验探究的热点。
制备原理:Fe2++2OH-===Fe(OH)2↓。
(1)成功关键:①溶液中不含Fe3+和O2等氧化性物质;
②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气的体系中。
(2)制备Fe(OH)2时常采用的方法
①采用新制备的纯亚铁盐溶液;
②将溶解亚铁盐的蒸馏水煮沸(除去溶解的氧气);
③将碱直接加到亚铁盐溶液的底部[使生成的Fe(OH)2与空气隔离];
④在亚铁盐溶液的液面上加隔氧剂(如加入苯等密度比水小而又不溶于水的有机溶剂)。
2.确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为Fe2O3;
若a∶b=3∶4,则铁的氧化物是Fe3O4或FeO与Fe2O3按物质的量比1∶1的混合物或FeO、Fe2O3、Fe3O4的混合物(其中FeO、Fe2O3物质的量之比为1∶1,Fe3O4为任意值)。
3.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣。上述沉淀和残渣分别是( )
A.Fe(OH)3 Fe2O3 B.Fe(OH)2 Fe2O3
C.Fe(OH)2 Fe(OH)3 D.Fe(OH)2 Fe3O4
答案 B
解析 铁与稀硫酸反应生成FeSO4,再与过量氨水反应生成白色沉淀Fe(OH)2,在空气中加热Fe(OH)2,铁元素被氧化为+3价,最后所得红棕色残渣为Fe2O3。
4.(2018·营口质检)有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025 mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe2O3 B.Fe3O4
C.Fe4O5 D.Fe5O7
答案 D
解析 根据2Fe2++Cl2===2Fe3++2Cl-,可知铁的“氧化物”样品用盐酸溶解后所得溶液中n(Fe2+)=0.025 mol×2=0.05 mol,根据电荷守恒得2n(Fe2+)+3n(Fe3+)=n(Cl-),则n(Fe3+)=0.2 mol,故n(Fe2+)∶n(Fe3+)=0.05∶0.2=1∶4,故该氧化物可表示为FeO·2Fe2O3,即Fe5O7。
考点 “铁三角”及Fe3+、Fe2+的检验
[典例3] (2018·贵阳一中高三模拟)下列中学常见实验的现象或表述正确的是( )
A.过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显红色
B.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液显红色即可证明
D.向CuSO4溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加热煮沸一会,然后冷却、过滤,滤纸上的物体为“蓝色固体”
解析 过量的铁粉与一定量的稀硝酸反应最终生成的是Fe2+,A错误;制备氢氧化亚铁应避免被氧气氧化,向硫酸亚铁溶液中加氢氧化钠溶液时应把胶头滴管的下端插入液面以下且不能搅拌,B错误;CuSO4溶液中滴入过量NaOH溶液充分反应后生成Cu(OH)2沉淀,加热一段时间冷却后过滤,滤纸上留有的是CuO(黑色),D错误。
答案 C
名师精讲
1.“铁三角”
(1)“铁三角”中的转化关系
(2)Fe2+、Fe3+相互转化中的两个关系,Fe2+Fe3+
①Fe2+与强氧化剂(O2、Cl2、Br2、H2O2、Na2O2、KMnO4、HNO3、K2Cr2O7等)反应时,被氧化为Fe3+。如2Fe2++H2O2+2H+===2Fe3++2H2O、6Fe2++Cr2O+14H+===2Cr3++6Fe3++7H2O。
②Fe3+与Fe、Cu、S2-(H2S)、I-(HI)等还原剂反应时生成Fe2+。如2Fe3++H2S===2Fe2++S↓+2H+、2Fe3++Fe===3Fe2+、2Fe3++Cu===2Fe2++Cu2+(三价铁盐腐蚀印刷电路板)。
注意 氧化性:Ag+>Fe3+>Cu2+>Fe2+,还原性:S2->I->Fe2+>Br->Cl-。
(3)“铁三角”的重要应用
①物质除杂
②判断离子共存
a.发生氧化还原反应而不能大量共存
Fe2+与强氧化剂不能共存:NO(H+)、ClO-、MnO(H+)
Fe3+与强还原剂不能共存:S2-、I-、HS-、SO
b.发生非氧化还原反应不能大量共存
Fe2+、Fe3+与OH-、HCO、CO、AlO等发生复分解或相互促进水解不能大量共存。
Fe3+与SCN-发生络合反应不能大量共存。
c.盐溶液的配制和保存
含Fe2+的溶液:如配制FeSO4溶液时加入稀硫酸防止Fe2+的水解,加入铁粉防止Fe2+被氧化。
含Fe3+的溶液:如配制Fe2(SO4)3溶液,应将Fe2(SO4)3固体溶于H2SO4,再加水稀释到指定浓度。
2.Fe2+、Fe3+的检验方法
(3)含Fe2+、Fe3+的混合溶液中Fe3+、Fe2+的检验
溶液变红色,说明含有Fe3+。
KMnO4溶液紫红色褪去,说明含有Fe2+。
(4)Fe2+的特征检验方法
溶液产生蓝色沉淀,说明溶液中含有Fe2+,3Fe2++2[Fe(CN)6]3-===Fe3[Fe(CN)6]2↓。
5.下列说法正确的是( )
A.将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,反应现象是有气体产生,溶液呈红色,原因是稀硝酸将Fe氧化为Fe3+
B.将铜粉加入1.0 mol/L Fe2(SO4)3溶液中,会有溶液变蓝、黑色固体出现的现象,这是因为金属铁比铜活泼
C.FeCl3溶液可用于铜质印刷线路板制作是因为FeCl3能从含Cu2+的溶液中置换出铜
D.室温下,能将浓硫酸盛放在铁桶中
答案 D
解析 A项,过量铁粉与稀硝酸充分反应后铁元素转化为Fe2+
,滴加KSCN溶液后不出现红色;B项,铜粉与Fe2(SO4)3溶液发生反应2Fe3++Cu===2Fe2++Cu2+,溶液变蓝但不会有黑色固体出现;C项,FeCl3与Cu2+不反应,制作线路板的原理为Fe3+能腐蚀铜,发生反应为2Fe3++Cu===2Fe2++Cu2+,解释错误;D项,常温下,Fe遇浓H2SO4钝化,可用铁桶盛放浓H2SO4,正确。
6.已知下述三个实验中均能发生化学反应。
①
②
③
将铁钉放入CuSO4溶液中
向FeSO4溶液中滴入几滴浓硝酸
将铜丝放入FeCl3溶液中
下列判断正确的是( )
A.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
B.实验①中铁钉只作还原剂
C.实验②中Fe2+既显氧化性又显还原性
D.实验③中发生的是置换反应
答案 B
解析 ①中发生反应Fe+Cu2+===Fe2++Cu,②中发生反应3Fe2++4H++NO===3Fe3++NO↑+2H2O,③中发生反应Cu+2Fe3+===Cu2++2Fe2+。A项,根据氧化性:氧化剂>氧化产物,可知氧化性:Fe3+>Cu2+>Fe2+;C项,实验②中Fe2+化合价升高,只显还原性;D项,实验③中无单质生成,不是置换反应。
相关文档
- 2020届高考化学一轮复习化学工艺流2021-07-0236页
- 2019届高考化学一轮复习化学反应与2021-07-0211页
- 2020届高考化学一轮复习化学能与热2021-07-0214页
- 2019届高考化学一轮复习化学反应中2021-07-0213页
- 2020届高考化学一轮复习化学反应速2021-07-0212页
- 2020届高考化学一轮复习化学实验方2021-07-0219页
- 2019届高考化学一轮复习化学与自然2021-07-028页
- 2020届高考化学一轮复习化学反应速2021-07-0235页
- 2020届高考化学一轮复习化学反应速2021-07-0217页
- 2020届高考化学一轮复习化学能与热2021-07-0210页