- 100.94 KB
- 2021-07-03 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第1课时 认识同周期元素性质的递变规律
1.下列比较金属性相对强弱的方法或依据正确的是( )
A.根据金属失电子的多少来确定,失电子较多的金属性较强
B.用Na来置换MgCl2溶液中的Mg,来验证Na的金属性强于Mg
C.根据Mg不与NaOH溶液反应而Al能与NaOH溶液反应,说明金属性:Al>Mg
D.根据碱性:NaOH>Mg(OH)2>Al(OH)3,可说明钠、镁、铝的金属性依次减弱
答案D
解析A项应该根据金属失电子的难易来比较,易失电子的金属性较强,错误;B项中钠首先要跟MgCl2溶液中的水反应,不能置换出Mg,错误;C项判断依据错误,D项正确。
2.X、Y、Z三种元素位于周期表中同一周期,它们的最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则三种元素原子序数的大小顺序为( )
A.X>Y>Z B.Y>Z>X
C.X>Z>Y D.Z>X>Y
答案C
解析根据X、Y、Z三种元素的最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物可知,Y为金属元素,X为非金属元素,Z处于X和Y之间。同周期元素随着原子序数的递增,元素的金属性逐渐减弱,非金属性逐渐增强,则三种元素在周期表中的位置关系是
Y
……
Z
……
X
,故原子序数关系为X>Z>Y。
3.X、Y为同周期元素,如果X的原子半径大于Y的原子半径,则下列判断不正确的是( )
A.若X、Y均为金属元素,则X失电子的能力强于Y
B.若X、Y均为金属元素,则X的阳离子氧化性比Y的阳离子氧化性强
C.若X、Y均为非金属元素,则Y的气态氢化物比X的气态氢化物稳定
D.若X、Y均为非金属元素,则最高价含氧酸的酸性Y的强于X的
答案B
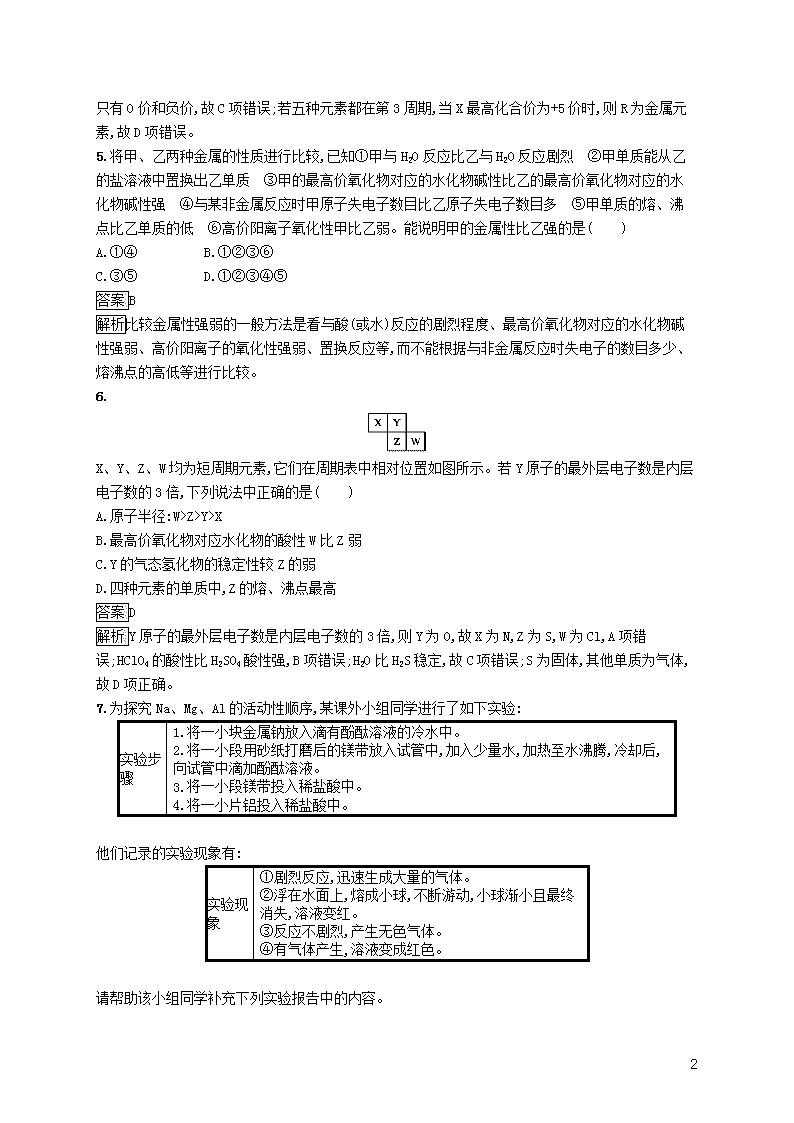
解析由原子半径X>Y可知,同周期中X在Y的左边。当X、Y为金属元素时,失电子能力X>Y,阳离子的氧化性XZ>Y>X
B.最高价氧化物对应水化物的酸性W比Z弱
C.Y的气态氢化物的稳定性较Z的弱
D.四种元素的单质中,Z的熔、沸点最高
答案D
解析Y原子的最外层电子数是内层电子数的3倍,则Y为O,故X为N,Z为S,W为Cl,A项错误;HClO4的酸性比H2SO4酸性强,B项错误;H2O比H2S稳定,故C项错误;S为固体,其他单质为气体,故D项正确。
7.为探究Na、Mg、Al的活动性顺序,某课外小组同学进行了如下实验:
实验步骤
1.将一小块金属钠放入滴有酚酞溶液的冷水中。
2.将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液。
3.将一小段镁带投入稀盐酸中。
4.将一小片铝投入稀盐酸中。
他们记录的实验现象有:
实验现象
①剧烈反应,迅速生成大量的气体。
②浮在水面上,熔成小球,不断游动,小球渐小且最终消失,溶液变红。
③反应不剧烈,产生无色气体。
④有气体产生,溶液变成红色。
请帮助该小组同学补充下列实验报告中的内容。
8
(1)在下表中填写与实验步骤相对应的实验现象的序号:
实验步骤
1
2
3
4
实验现象
(2)写出钠与水反应的化学方程式: 。
(3)实验结论是 。
(4)用原子结构理论对上述实验结论进行解释,同周期主族元素从左至右,原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐 ,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,因此 逐渐减弱。
答案(1)② ④ ① ③
(2)2Na+2H2O2NaOH+H2↑
(3)Na、Mg、Al金属性逐渐减弱 (4)减小 金属性
解析(1)金属钠、镁、铝位于同一周期,按照从左到右的顺序失电子能力逐渐减小,与水及酸反应置换出氢气的程度是越来越难。所以,1对应的现象为②,2对应的现象为④,3对应的现象为①,4对应的现象为③。
(2)钠与水反应生成氢氧化钠与氢气,反应的化学方程式为2Na+2H2O2NaOH+H2↑。
(3)根据金属和酸以及水反应的剧烈程度,可以知道金属活动性顺序为Na>Mg>Al,即实验结论是Na、Mg、Al金属性逐渐减弱。
(4)同周期主族元素从左到右核电荷数逐渐增多,原子半径逐渐减小,原子核对核外电子的吸引力逐渐增强,失电子能力逐渐减弱,金属性逐渐减弱。
提升能力·跨越等级
1.下列事实能说明氯元素原子得电子能力比硫元素强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强
③HCl的稳定性比H2S强 ④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧还原性:Cl-S,元素的非金属性越强,其氢化物的还原性就越弱,因此HCl的还原性比H2S弱,④错误;⑤元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,因此HClO4的酸性比H2SO4强,HClO的酸性比H2SO4弱,⑤错误;⑥元素非金属性越强,能把变价金属氧化为高价态,元素的非金属性越弱,则把变价金属氧化为低价态。Cl2与铁反应生成FeCl3,而S与铁反应生成FeS,说明氯元素原子得电子能力比硫元素强,⑥正确;⑦元素非金属性强的单质能够把元素非金属性弱的单
8
质从化合物中置换出来。Cl2能与H2S反应生成S,说明氯元素原子得电子能力比硫元素强,⑦正确;⑧元素的非金属性越强,则其简单离子的还原性就越弱。因此还原性Cl-W
B.单质沸点:Y>Z>W
C.离子半径:X2->W->Y+>Z-
D.结合H+的能力:X2->W-
答案D
解析W、X、Y、Z均为短周期主族元素,W、X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构,则X、Y、Z分别为S、Na、F;W和Z的最外层电子数相同,则W为氯元素。W、X的最高价氧化物对应水化物的酸性为高氯酸>硫酸,A项错误;单质沸点:硫>氯气>氟气,B项错误;电子层数越多的离子,其半径越大,电子层数相同的离子,核电荷数越小的半径越大,所以离子半径:S2->Cl->F->Na+,C项错误;因为硫化氢为弱电解质,氯化氢为强电解质,故结合H+的能力S2->Cl-,D项正确。
3.下列叙述不能说明氮和氧非金属性相对强弱的是( )
A.氨气在氧气中燃烧生成氮气
B.沸点:H2O>NH3
C.NO中N为+2价,氧为-2价
D.热稳定性:H2O>NH3
答案B
解析氨气在氧气中燃烧生成氮气,氧元素的化合价降低,氧元素的化合价升高,则氧得电子能力强,说明非金属性O>N,故A不符合题意;H2O的沸点比NH3高,沸点的高低与元素的非金属性强弱没有关系,故B符合题意;NO中N为正价,O为负价,则氧得到电子能力强,说明非金属性O>N,故C不符合题意;非金属性越强,对应气态氢化物越稳定,则热稳定性H2O>NH3,说明非金属性O>N,故D不符合题意。
4.(双选)同周期三种元素X、Y、Z,它们的最高价氧化物的水化物分别是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
A.含氧酸的酸性:H3ZO4>H2YO4>HXO4
B.非金属性:X>Y>Z
C.气态氢化物的稳定性按X、Y、Z顺序减弱
D.元素的最低化合价的绝对值按X、Y、Z顺序减小
答案BC
解析解本题的依据是同一周期元素性质的递变规律,关键是确定X、Y、Z在周期表中的位置,突破口是最高价氧化物的水化物的化学式。具体分析如下:
8
HXO4H2YO4H3ZO4+7+6+5ⅦAⅥAⅤA分析各选项。根据最高化合价可知,X、Y、Z的负价分别为-1、-2、-3,原子序数为X>Y>Z,元素的非金属性X>Y>Z,B项正确。气态氢化物的稳定性:X>Y>Z,C项正确。
5.X、Y、Z均为元素周期表中前20号元素,Xa+、Yb-、Z(b+1)-简单离子的电子层结构相同。下列说法正确的是( )
A.已知mXa+与nYb-,则m+a=n-b
B.离子半径:Yb->Z(b+1)->Xa+
C.Z(b+1)-的还原性一定强于Yb-
D.气态氢化物的稳定性Hb+1Z一定强于HbY
答案C
解析原子失去电子形成阳离子,原子获得电子形成阴离子。由于mXa+、nYb-简单离子的电子层结构相同,所以m-a=n+b,A项错误;对于电子层结构相同的微粒来说,核电荷数越多,离子半径就越小。因此离子半径为Z(b+1)->Yb->Xa+,B项错误;对于电子层结构相同的离子来说,离子的核电荷数越大,离子半径就越小,离子的还原性就越弱,故Z(b+1)-的还原性一定强于Yb-,C项正确;核电荷数Y>Z,则气态氢化物的稳定性Hb+1Za,c和d的气态氢化物的还原性d>c,e为金属元素。五种元素的原子得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
A.baedc B.edabc C.abdce D.ebadc
答案A
解析a和b的最高价氧化物对应水化物呈碱性,则a、b为金属,因其最高价氧化物对应水化物的碱性b>a,则金属性b>a。c和d的气态氢化物的还原性d>c,即c、d为非金属元素,且非金属性d”、“<”或“=”填空。
离子半径
酸性
还原性
得电子能力
N3- Al3+
H2SO4 HClO4
O2- S2-
35Cl 37Cl
8
(3)黑火药爆炸时发生反应的化学方程式为S+2KNO3+3CK2S+3CO2↑+N2↑,该反应的生成物中,属于非电解质的是 (写化学式);K2S中阴、阳离子的半径大小关系是 (用化学式表示)。
(4)在(3)中化学反应方程式涉及的元素中,属于同周期元素的非金属性由强到弱的顺序为 ,能证明其递变规律的事实是 。
A.氧化物对应水化物的酸性
B.气态氢化物的沸点
C.氢化物的稳定性
答案(1)第2周期ⅣA族 14C (2)> < < =
(3)CO2 S2->K+ (4)O>N>C C
解析(1)碳元素位于元素周期表第2周期ⅣA族,14C可以测定文物年代。
(2)N3-、Al3+为核外电子排布相同的离子,离子核电荷数越大,半径越小,则N3-半径大于Al3+;非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;氧气的氧化性大于硫单质,则O2-的还原性小于S2-;35Cl与37Cl属于同一种元素,同种元素得电子能力相同。
(3)二氧化碳属于非电解质,K2S由K+和S2-构成,K+与S2-的核外电子排布相同,S2-的半径大于K+。
(4)C、N、O同周期,同周期随原子序数增大元素的非金属性增强,故非金属性O>N>C;氧元素没有含氧酸,不能通过含氧酸的酸性比较元素的非金属性,故A错误;沸点属于物理性质,不能比较元素的非金属性强弱,故B错误;气态氢化物越稳定,对应元素的非金属性越强,故C正确。
8.A、B、C、D、E、F六种短周期元素在元素周期表中的位置如图所示。
回答下列问题:
(1)在周期表中,E位于第 周期 族。
(2)在E、F的气态氢化物中,热稳定性较强的是 (填化学式,下同),还原性较强的是 。
(3)A、C、D、E组成两种酸式盐X、Y,将X、Y溶液混合发生复分解反应,写出离子方程式: 。
(4)常用(BA4)2E2C8检验废水中的Mn2+,若观察到无色溶液变紫红色,可判断废水中含Mn2+,还原产物与盐酸酸化的BaCl2溶液混合产生白色沉淀。写出无色溶液变紫红色溶液的离子方程式: 。
答案(1)3 ⅥA
(2)HCl H2S (3)HSO3-+H+SO2↑+H2O
(4)5S2O82-+2Mn2++8H2O10SO42-+2MnO4-+16H+
解析根据各元素在周期表中的位置可知,A、B、C、D、E、F分别为H、N、O、Na、S、Cl。
(1)在周期表中,E(硫元素)位于第3周期第ⅥA族。
(2)S、Cl的非金属性相比,S镁>铝,所以相同条件下与盐酸反应最剧烈的是钠,反应速率最慢的是铝;生成1 mol氢气需要得到2 mol电子,1 mol钠都失去1 mol电子,1 mol镁失去2 mol电子,而1 mol铝失去3 mol电子,所以生成氢气最多的是金属铝。
(2)氯气的氧化性强于硫单质,所以氯气能够与硫离子反应生成单质硫,反应的离子方程式为S2-+Cl2S↓+2Cl-。
Ⅱ.(3)由图知a为分液漏斗。
(4)高锰酸钾与浓盐酸反应较为剧烈,无需加热即可进行,应选装置A。
8
(5)检验氯气的性质时,不能先通过NaOH溶液,否则会消耗氯气,且起不到尾气吸收的作用,因为①处为NaBr溶液、②处为NaOH溶液,所以应从X端进氯气。①处Cl2与NaBr溶液反应生成Br2,反应的离子方程式为Cl2+2Br-2Cl-+Br2。②处主要为Cl2与NaOH溶液反应,其反应的离子方程式为Cl2+2OH-Cl-+ClO-+H2O。
8