- 1.10 MB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第
3
章 自然界中的元素
第
1
节 碳的多样性
学习目标
1
、了解同素异形体的概念,知道碳的三种同素异形体和其物理性质的差异及其原因。
2
、知道含碳化合物种类及其分类,认识碳酸钠和碳酸氢钠的性质并体会其差异
。
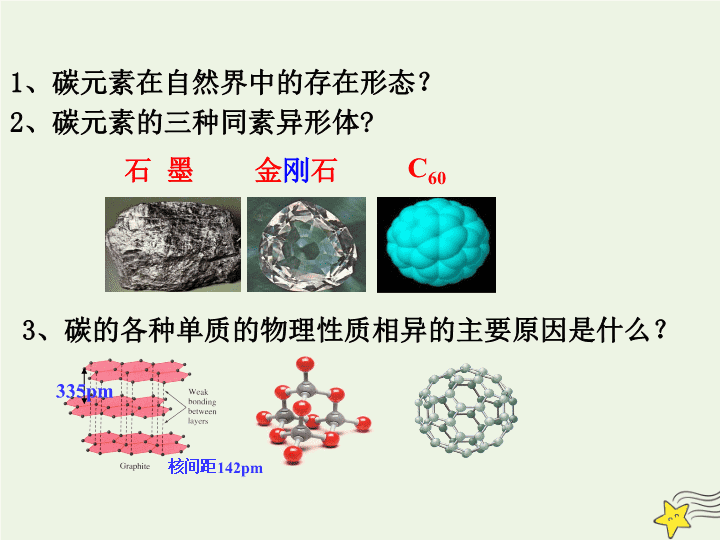
石 墨
金
刚
石
C
60
2
、碳元素的三种同素异形体
?
1
、碳元素在自然界中的存在形态?
3
、碳的各种单质的物理性质相异的主要原因是什么?
335pm
核间距
142pm
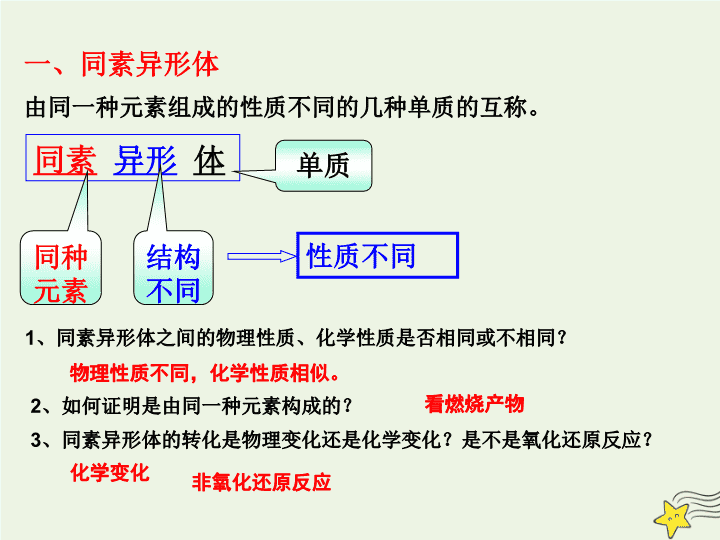
同素
异形
体
同种元素
结构
不同
单质
性质不同
一、同素异形体
由同一种元素组成的性质不同的几种单质的互称。
物理性质不同,化学性质相似。
看燃烧产物
化学变化
非氧化还原反应
2
、如何证明是由同一种元素构成的?
3
、同素异形体的转化是物理变化还是化学变化?是不是氧化还原反应?
1
、同素异形体之间的物理性质、化学性质是否相同或不相同?
碳酸钠与碳酸氢钠可能与哪些物质反应?
碳酸钙的化学性质:
1
、与盐酸反应:
CaCO
3
+2HCl ==== CaCl
2
+CO
2
↑+H
2
O
2
、受热分解:
CaCO
3
==== CaO+CO
2
↑
高温
盐酸
受热分解
某些盐溶液、碱溶液
Na
2
CO
3
NaHCO
3
问题
:
碳酸钠和碳酸氢钠都易与酸反应,为什么等质量的碳酸钠与碳酸氢钠和足量的盐酸反应时,
碳酸氢钠产生的气体多,且反应剧烈
呢?
Na
2
CO
3
+2HCl====2NaCl+ H
2
O+CO
2
↑
CO
3
2 -
+2H
+
====H
2
O + CO
2
↑
NaHCO
3
+HCl====NaCl+ H
2
O + CO
2
↑
HCO
3
-
+ H
+
====H
2
O+CO
2
↑
1
、与酸反应
Na
2
CO
3
+2HCl=2NaCl+
H
2
O+CO
2
NaHCO
3
+HCl=NaCl+ H
2
O + CO
2
106g
44g
0.3g
m
1
84g
44g
0.3g m
2
为什么与
足量
相同的稀盐酸反应
,
等质量
NaHCO
3
比
Na
2
CO
3
生成气体
更多
?
CO
3
2-
H
+
HCO
3
-
H
+
H
2
O+CO
2
一步完成
2H
+
二步完成
为 什 么与
足量
相同的稀盐酸反应,
NaHCO
3
比
Na
2
CO
3
更剧烈
?
对
NaHCO
3
:
HCO
3
-
+ H
+
= H
2
O + CO
2
即
对
Na
2
CO
3
:
先
:CO
3
2 -
+ H
+
= HCO
3
-
再
:HCO
3
-
+ H
+
= H
2
O + CO
2
(
总
:CO
3
2-
+ 2H
+
= H
2
O + CO
2
)
与
H
+
的量有关
思考:
①分别向
Na
2
CO
3
和
NaHCO
3
的溶液中逐滴滴加盐酸,会观察到什么现象、对应什么反应?
Na
2
CO
3
:
开始无气泡,一段时间后产生气泡
NaHCO
3
:立即产生气泡
先:
CO
3
2-
+ H
+
==== HCO
3
-
后:
HCO
3
-
+H
+
==== H
2
O+CO
2
↑
HCO
3
-
+H
+
==== H
2
O+CO
2
↑
不一样。
将盐酸逐滴滴入到
Na
2
CO
3
溶液中开始无现象,后产生气泡。将
Na
2
CO
3
溶液逐滴滴入到盐酸中开始就产生气泡。
②
将盐酸逐滴滴入到
Na
2
CO
3
溶液中,与将
Na
2
CO
3
溶液逐滴滴入到盐酸中的现象是否一样?
③
不用其它试剂能否鉴别
Na
2
CO
3
溶液与稀盐酸?
能。互滴法:逐滴滴加
Na
2
CO
3
NaHCO
3
碳酸钠受热
不分解
2NaHCO
3
==== Na
2
CO
3
+H
2
O+CO
2
↑
△
2
、热稳定性
证明:碳酸钠的热稳定性
大于
碳酸氢钠
【
例
1】
下列物质中性质稳定,受热难分解的是( )
A CuSO
4
·5H
2
O B Na
2
CO
3
C NaHCO
3
D HClO
B
Na
2
CO
3
NaHCO
3
Na
2
CO
3
+CaCl
2
====CaCO
3
↓
+2NaCl
与可溶性的钙盐、钡盐反应生成沉淀
3
、与可溶性的
钙
盐、
钡
盐反应
不反应
可以用来鉴别碳酸钠与碳酸氢钠
Na
2
CO
3
NaHCO
3
Na
2
CO
3
+Ca(OH)
2
====CaCO
3
↓+2NaOH
NaHCO
3
+NaOH====Na
2
CO
3
+H
2
O
和氢氧化钠不反应
4
、与碱反应
Ca(OH)
2
+2NaHCO
3
== 2H
2
O+CaCO
3
↓
+Na
2
CO
3
氢氧化钙、氢氧化钡、氢氧化钠
都不能用来鉴别碳酸钠和碳酸氢钠
注意:
HCO
3
-
与
H
+
、
OH
-
的反应
HCO
3
-
+ H
+
====
HCO
3
-
+ OH
-
====
H
2
O + CO
2
↑
H
2
O + CO
3
2-
根据电荷是否守恒来检验产物是否对应
【
例
2】
可以用来判断
NaHCO
3
粉末中
混有
Na
2
CO
3
的实验方法是( )
A
溶于水后,滴加澄清石灰水,有白色沉淀生成
B
滴加稀盐酸时有气泡产生
C
加热时有无色气泡产生
D
溶于水后,滴加
CaCl
2
稀溶液,有白色沉淀生成
D
同分异构体