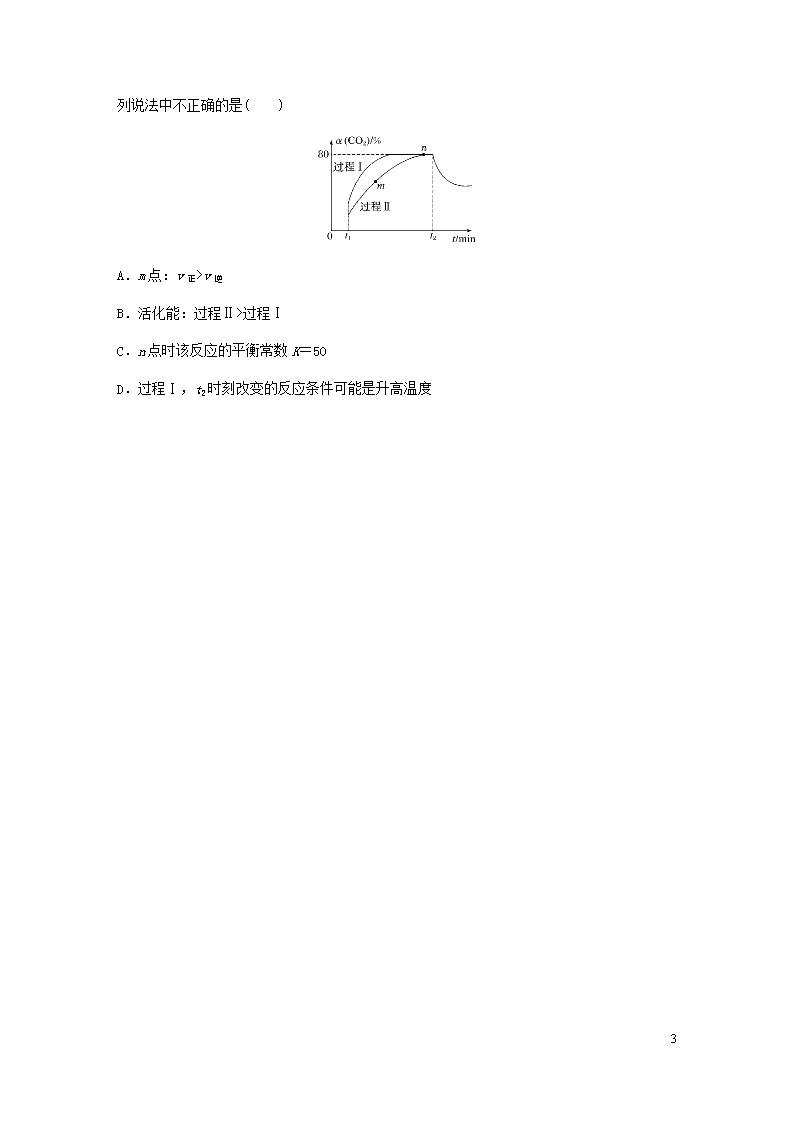- 180.71 KB
- 2021-07-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
微考点59 有关速率平衡的常规图像
1.(2019·天津质检)向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是( )
A.Y的起始物质的量为0.5mol
B.该反应的化学方程式为2X(g)+Y(g)3Z(g) ΔH<0
C.若t0=0,t1=10s,则t0~t1阶段的平均反应速率为v(Z)=0.03mol·L-1·s-1
D.反应物X的转化率t6点比t3点高
2.如图是温度和压强对反应X+Y2Z影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
A.X、Y、Z均为气态
B.恒容时,混合气体的密度可作为此反应是否达到化学平衡状态的判断依据
C.升高温度时v正增大,v逆减小,平衡向右移动
D.使用催化剂Z的产率提高
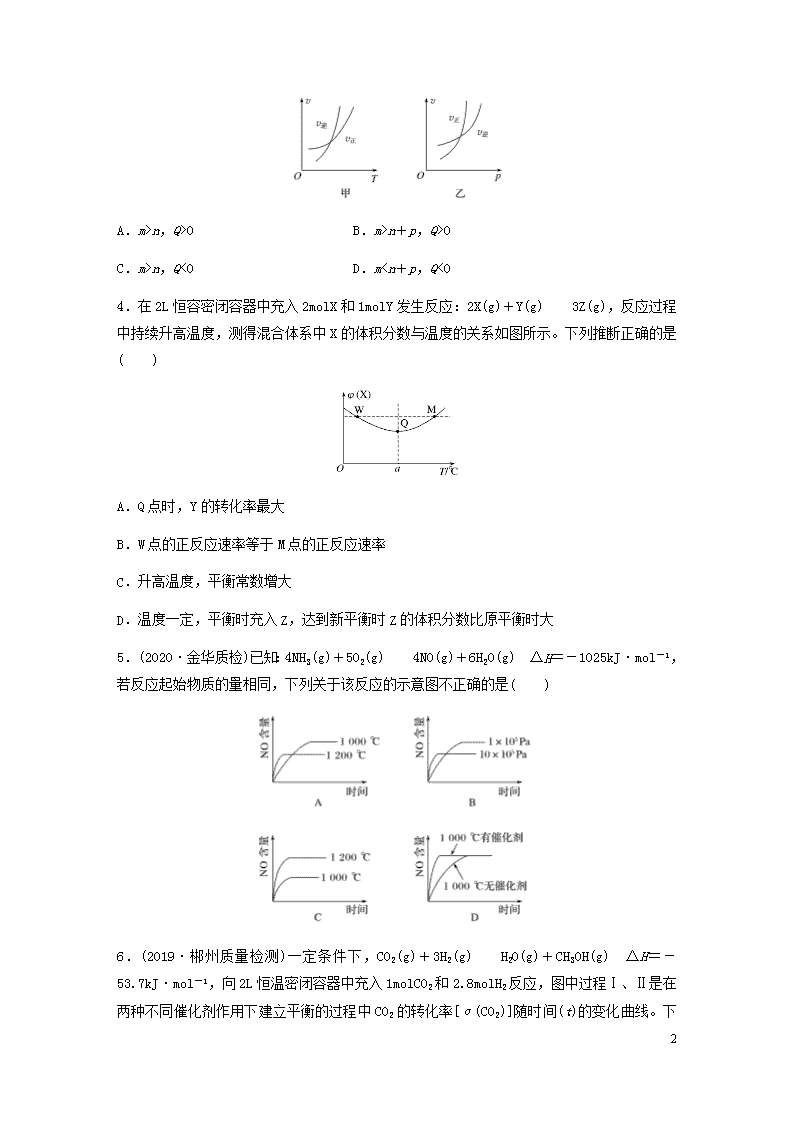
3.(2019·新余质检)可逆反应mA(g)nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图像,以下叙述正确的是( )
4
A.m>n,Q>0 B.m>n+p,Q>0
C.m>n,Q<0 D.mv逆
B.活化能:过程Ⅱ>过程Ⅰ
C.n点时该反应的平衡常数K=50
D.过程Ⅰ,t2时刻改变的反应条件可能是升高温度
4
答案精析
1.B 2.B
3.C [由图像可知,正反应速率与逆反应速率的交叉点为平衡状态;达到平衡时,升高温度,v正、v逆都增大,且v逆>v正,平衡向逆反应方向移动,逆反应为吸热反应,故ΔH<0即Q<0;达到平衡时增大压强,v正、v逆都增大,且v正>v逆,平衡向正反应方向移动,正反应为气体体积减小的反应,故m>n,C项正确。]
4.A [由图可知,Q点X的体积分数φ(X)最小,则最低点Q为平衡点,Q点后升高温度,φ(X)增大,平衡逆向移动,Y的转化率降低,故Q点时Y的转化率最大,A正确;M点的温度高于W点的温度,故M点的正反应速率较大,B错误;升高温度,平衡逆向移动,平衡常数减小,C错误;该反应前后气体分子数不变,温度一定,平衡时充入Z,达到新平衡时与原平衡是等效平衡,故达到平衡时Z的体积分数不变,D错误。]
5.C [由于该反应的正反应为放热反应,温度升高平衡逆向移动,NO的含量降低,故A项正确,C项错误;该反应的正反应是气体体积增大的反应,压强减小平衡正向移动,NO的含量增大,故B项正确;催化剂的使用只能改变反应速率,不能使平衡发生移动,NO的含量不变,故D项正确。]
6.C
4
相关文档
- 2021届(鲁科版)高考化学一轮复习有机2021-07-067页
- 【化学】黑龙江省哈尔滨市阿城区龙2021-07-0613页
- 河北省沧州市第一中学2019-2020学2021-07-0610页
- 2018届二轮复习化学实验综合探究课2021-07-06149页
- 2017-2018学年湖北省沙市中学高二2021-07-0611页
- 2018-2019学年福建省永安市第一中2021-07-067页
- 化学卷·2018届湖北省武汉二中高二2021-07-0610页
- 2017年四川省大教育联盟高考一模化2021-07-0615页
- 河南省重点高中2020-2021学年高二2021-07-066页
- 2021高考化学一轮复习专题1第2讲物2021-07-0675页