- 299.00 KB
- 2021-07-07 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
素养说明:化学核心素养要求考生能认识科学探究是进行科学解释和发现、创造和应用的科学实践活动;对于教材实验的迁移与创新,能提高学生实验探究能力和创新能力。
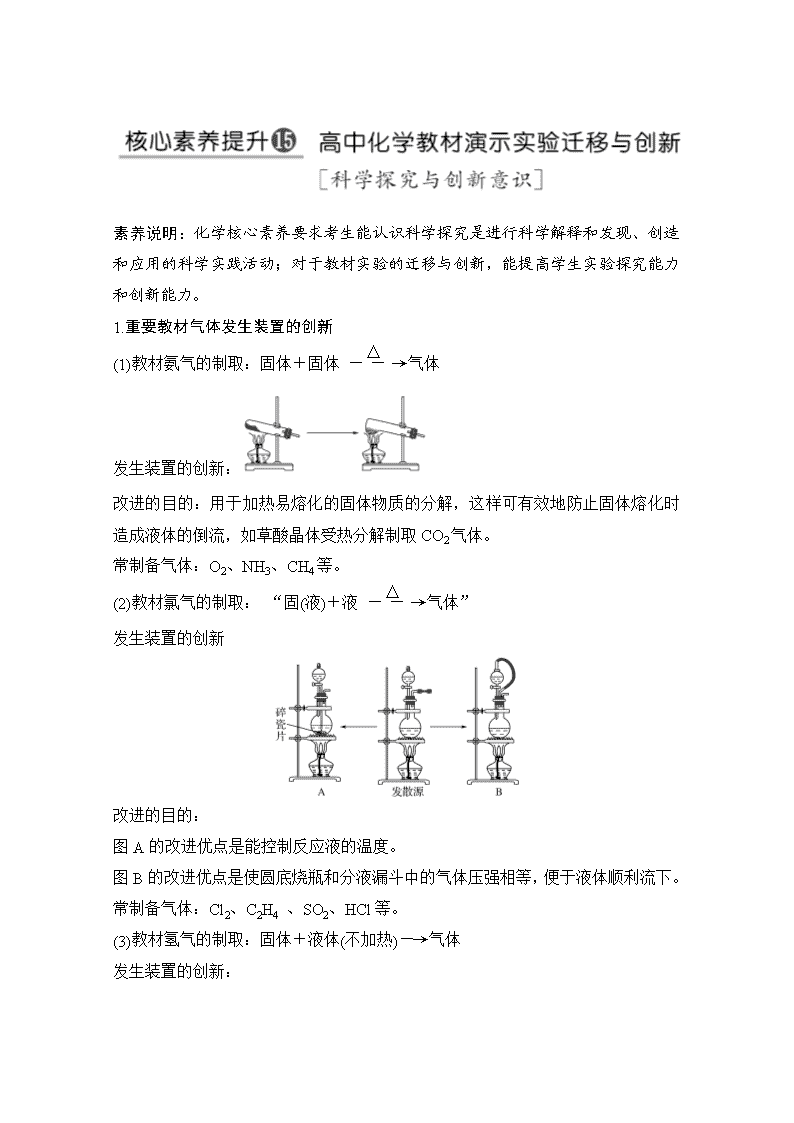
1.重要教材气体发生装置的创新
(1)教材氨气的制取:固体+固体气体
发生装置的创新:
改进的目的:用于加热易熔化的固体物质的分解,这样可有效地防止固体熔化时造成液体的倒流,如草酸晶体受热分解制取CO2气体。
常制备气体:O2、NH3、CH4等。
(2)教材氯气的制取: “固(液)+液气体”
发生装置的创新
改进的目的:
图A的改进优点是能控制反应液的温度。
图B的改进优点是使圆底烧瓶和分液漏斗中的气体压强相等,便于液体顺利流下。
常制备气体:Cl2、C2H4 、SO2、HCl等。
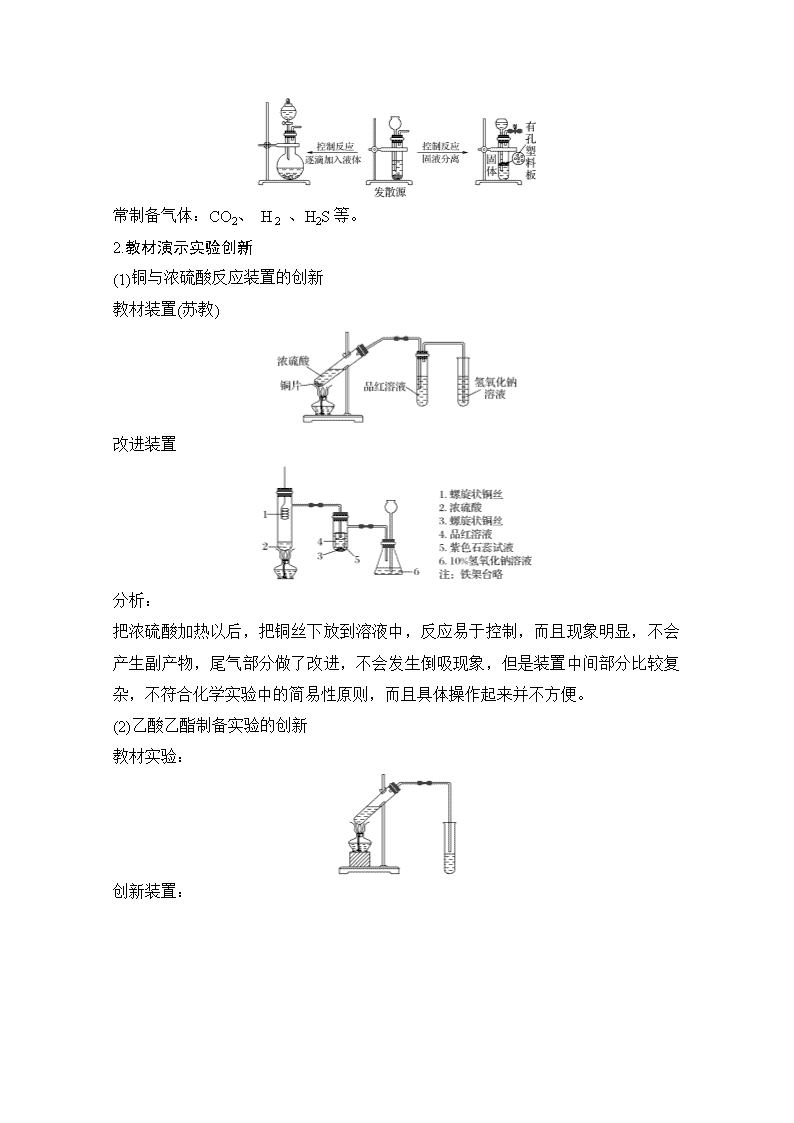
(3)教材氢气的制取:固体+液体(不加热)―→气体
发生装置的创新:
常制备气体:CO2、 H 2 、H2S等。
2.教材演示实验创新
(1)铜与浓硫酸反应装置的创新
教材装置(苏教)
改进装置
分析:
把浓硫酸加热以后,把铜丝下放到溶液中,反应易于控制,而且现象明显,不会产生副产物,尾气部分做了改进,不会发生倒吸现象,但是装置中间部分比较复杂,不符合化学实验中的简易性原则,而且具体操作起来并不方便。
(2)乙酸乙酯制备实验的创新
教材实验:
创新装置:
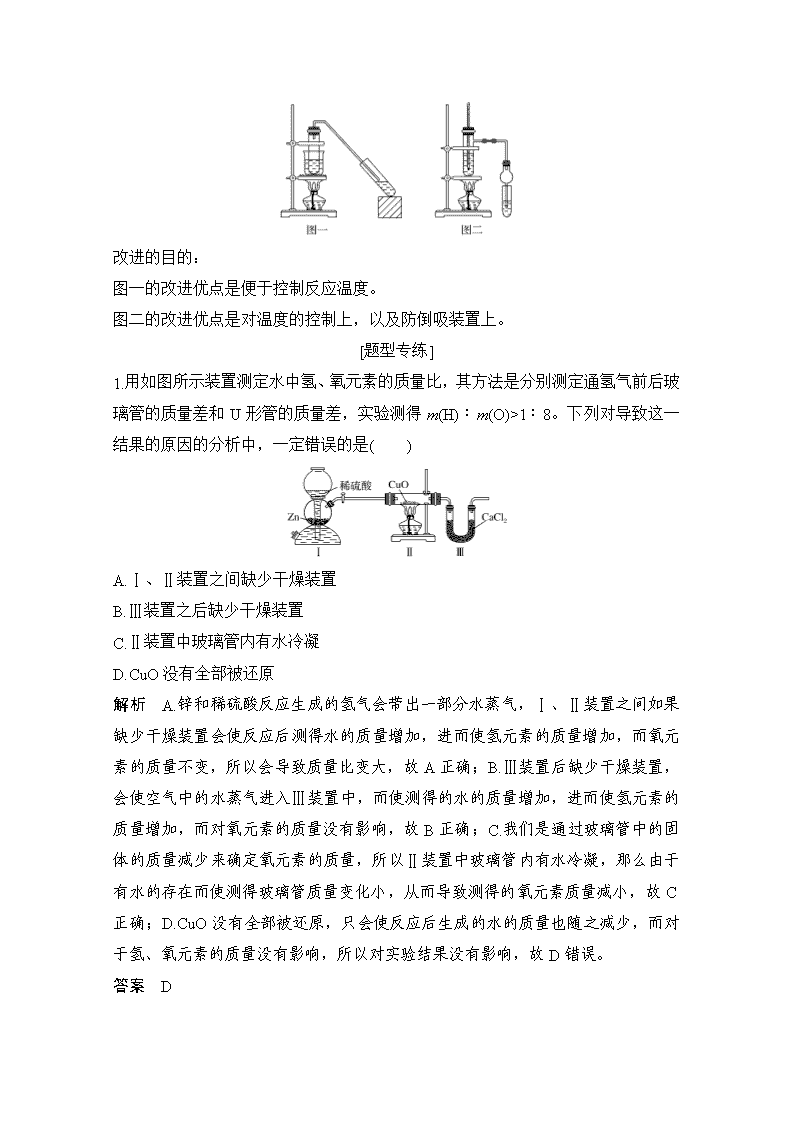
改进的目的:
图一的改进优点是便于控制反应温度。
图二的改进优点是对温度的控制上,以及防倒吸装置上。
[题型专练]
1.用如图所示装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是( )
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置之后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
解析 A.锌和稀硫酸反应生成的氢气会带出一部分水蒸气,Ⅰ、Ⅱ装置之间如果缺少干燥装置会使反应后测得水的质量增加,进而使氢元素的质量增加,而氧元素的质量不变,所以会导致质量比变大,故A正确;B.Ⅲ装置后缺少干燥装置,会使空气中的水蒸气进入Ⅲ装置中,而使测得的水的质量增加,进而使氢元素的质量增加,而对氧元素的质量没有影响,故B正确;C.我们是通过玻璃管中的固体的质量减少来确定氧元素的质量,所以Ⅱ装置中玻璃管内有水冷凝,那么由于有水的存在而使测得玻璃管质量变化小,从而导致测得的氧元素质量减小,故C正确;D.CuO没有全部被还原,只会使反应后生成的水的质量也随之减少,而对于氢、氧元素的质量没有影响,所以对实验结果没有影响,故D错误。
答案 D
2.1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如图,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1丁醇的转化率
解析 该酯化反应需要的温度为115~125 ℃,水浴的最高温度为100 ℃,A项正确;长导管可以起到冷凝回流酸和醇的作用,B项正确;乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错;在可逆反应中,增加一种反应物的浓度可以提高另一种反应物的转化率,D项正确。
答案 C
3.某同学对教材中铜与浓硫酸的实验作了如下改进。实验装置如图所示(加热和夹持装置已略去)。
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是___________________________________________________________________
__________________________________________________________________。
(2)仪器A的名称是________,仪器B的作用是__________________________________________________________________,
仪器D中所盛药品是_______________________________________________。
(3)A中发生反应的化学方程式为____________________________________
___________________________________________________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是__________________________________________________________________。
(5)实验后仪器A中有白色固体产生,将仪器A中固液混合物缓慢转移至盛有少量水的烧杯中,可观察到的现象是
____________________________________________________________________。
不可直接向仪器A中加水的原因是_______________________________________
___________________________________________________________________。
解析 (2)SO2在水中的溶解度较大,所以仪器B的作用是防止倒吸;仪器D的作用是吸收尾气中的SO2,防止污染空气,所以应盛装碱性固体。
(4)SO2的密度比空气大,所以反应后装置A、B、C中都会残留有一定量的SO2,可通过不断鼓入空气的方法将残留的SO2全部赶入装置D中被吸收。
答案 (1)关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变
(2)三颈烧瓶(或三口烧瓶) 防倒吸 碱石灰(或NaOH等合理答案均可) (3)2H2SO4(浓)+CuCuSO4+SO2↑+2H2O (4)打开旋塞E,从E管口向A中鼓入大量空气 (5)混合时放热,白色固体溶解,溶液变蓝色 水加入浓硫酸中,放出大量热使液体飞溅
相关文档
- 2021届(鲁科版)高考化学一轮复习化学2021-07-0711页
- 2020届高考化学一轮复习化学反应中2021-07-0617页
- 2020届高考一轮复习化学反应的方向2021-07-0630页
- 2020届高考化学一轮复习化学能与热2021-07-0642页
- 2021届高考化学一轮复习化学平衡图2021-07-068页
- 2020届高考化学一轮复习化学平衡常2021-07-0612页
- 2021届(鲁科版)高考化学一轮复习化学2021-07-0614页
- 2020届高考化学一轮复习化学反应速2021-07-069页
- 2020届高考化学一轮复习化学能与热2021-07-0616页
- 2020届高考化学一轮复习化学有关计2021-07-0618页