- 211.54 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
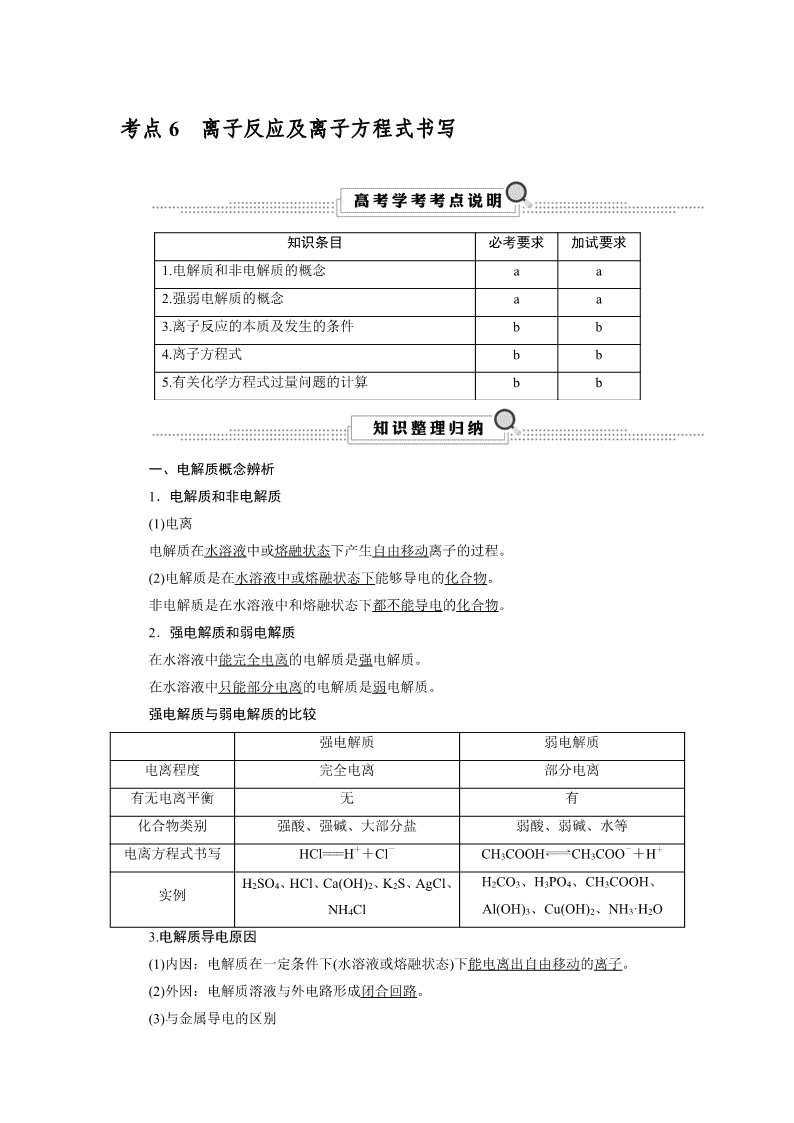
考点6 离子反应及离子方程式书写
知识条目
必考要求
加试要求
1.电解质和非电解质的概念
a
a
2.强弱电解质的概念
a
a
3.离子反应的本质及发生的条件
b
b
4.离子方程式
b
b
5.有关化学方程式过量问题的计算
b
b
一、电解质概念辨析
1.电解质和非电解质
(1)电离
电解质在水溶液中或熔融状态下产生自由移动离子的过程。
(2)电解质是在水溶液中或熔融状态下能够导电的化合物。
非电解质是在水溶液中和熔融状态下都不能导电的化合物。
2.强电解质和弱电解质
在水溶液中能完全电离的电解质是强电解质。
在水溶液中只能部分电离的电解质是弱电解质。
强电解质与弱电解质的比较
强电解质
弱电解质
电离程度
完全电离
部分电离
有无电离平衡
无
有
化合物类别
强酸、强碱、大部分盐
弱酸、弱碱、水等
电离方程式书写
HCl===H++Cl-
CH3COOHCH3COO-+H+
实例
H2SO4、HCl、Ca(OH)2、K2S、AgCl、NH4Cl
H2CO3、H3PO4、CH3COOH、
Al(OH)3、Cu(OH)2、NH3·H2O
3.电解质导电原因
(1)内因:电解质在一定条件下(水溶液或熔融状态)下能电离出自由移动的离子。
(2)外因:电解质溶液与外电路形成闭合回路。
(3)与金属导电的区别
金属导电是电子定向移动的结果,而电解质溶液导电是电离产生的自由离子定向移动的结果。
(4)电解质溶液导电能力强弱的判断
电解质溶液中自由移动的离子浓度越大、离子所带电荷数越多,则导电能力越强。如:2 mol/L的NaCl溶液导电能力强于1 mol/L的NaCl溶液,而2 mol/L的MgSO4溶液导电能力强于2 mol/L的NaCl溶液。
二、离子方程式书写及正误判断
1.离子反应
(1)概念:在水溶液中有离子参加的化学反应。
(2)反应发生的条件:
①生成难溶性的物质;②生成难电离的物质;③生成易挥发的物质;④离子间发生氧化还原反应。
(3)复分解型离子反应本质是溶液中某些物质的物质的量浓度减小。
2.离子方程式
(1)概念:用实际参与反应的离子符号表示化学反应的式子。
(2)意义:离子方程式可表示所有同一类的化学反应。而化学方程式只能表示一个化学反应。
(3)书写步骤:
①写:写出正确的化学方程式。
②拆:将可溶、完全电离的物质改写成离子形式。强酸、强碱、可溶盐需拆分,单质、氧化物、难溶物、气体、弱电解质仍写化学式。
③删:将方程式两边相等个数的同种离子和未参加反应的离子删去,并使化学计量数最简化。
④查:检查原子个数、电荷总数、得失电子数目是否守恒。
2.离子方程式书写正误判断
(1)注意物质“拆分”是否正确
氧化物、弱电解质、沉淀等在离子方程式中均不能拆分。复习时应记忆常见的弱电解质、微难溶物质等。
(2)检查“物料”“电荷”双守恒
离子方程式书写中常常只注意物料守恒(质量守恒),而忽视了电荷守恒,这也是命题中常出现的陷阱。如氯化铁溶液与铜的反应易错写成Fe3++Cu===Fe2++Cu2+,从物料角度看,是守恒的;但从电荷守恒看,等号左边是3个正电荷,右边是4个正电荷,电荷不守恒,因此错误。
(3)离子反应应符合客观事实
离子反应应当符合实际发生的客观事实。如Fe与盐酸只能生成Fe2+,而与足量HNO3反应则生成Fe3+;或者金属与氧化性酸反应不会生成H2;反应条件不同导致产物不同,如氯气与NaOH溶液,常温下反应生成NaClO和NaCl,而加热条件下反应生成NaClO3和NaCl;以及长等号与可逆符号的使用也需要注意,如H2O+COHCO+OH-,若用了长等号就是错误的。
(4)方程式与条件量不符合
在不同反应条件下,或者反应物相对量不同时,反应产物的配比可能发生变化。如,Fe3+和Cu2+均为1 mol/L的混合溶液中加入铁粉:若加入足量铁粉,则Fe3+和Cu2+均被还原,离子方程式为2Fe3++2Cu2++3Fe===5Fe2++2Cu;若加入少量铁粉,则仅有Fe3+被还原,离子方程式为2Fe3++Fe===3Fe2+。因此在审题时,仔细辨别,看清离子方程式的书写是否符合题意。
三、突破与量有关的离子方程式的书写
1.与酸式盐有关的离子反应
一般书写时,对于量不足的物质,该物质拆成离子后,实际参与反应的离子的物质的量之比一定要与它的化学式相符合,即可设为“1 mol”,然后再拆分;而足量的物质,该物质拆成离子后,实际参与反应的离子的物质的量之比不一定要与它的化学式相符合。即以不足量物质实际参加离子反应的离子完全反应为基准同足量物质反应来书写离子方程式。如:向足量的NaHCO3溶液中逐渐滴入澄清石灰水的反应。Ca(OH)2是量不足的物质,设为“1 mol”,拆成1 mol Ca2+和2 mol OH-,物质的量的比值符合化学式中的比例;继而可与2 mol HCO反应,即2 mol NaHCO3。然后写出相应的化学方程式后再改写成离子方程式。
化学方程式:Ca(OH)2+2NaHCO3===2H2O+CaCO3↓+Na2CO3
离子方程式:Ca2++2OH-+2HCO===2H2O+CaCO3↓+CO
2.产物可与过量的物质继续反应的离子反应
对于产物可与过量的物质继续反应的离子反应,可以先分步写出相应的离子方程式,再按题目的要求直接或按比例合并方程式。
例如:向NaOH溶液中通入CO2气体至过量,其离子反应分步写:
①2OH-+CO2===CO+H2O ②CO+CO2+H2O===2HCO
若向NaOH溶液中通入过量CO2气体,其离子反应一步完成,合并①②式即可:
OH-+CO2===HCO
若向足量NaOH溶液中通入少量CO2气体,则第二步反应没有发生,其离子方程式为①式:
2OH-+CO2===CO+H2O
3.混合顺序引起“量”不同的离子反应
两种反应物相互滴加的顺序不同也可能发生不同的离子反应,如碳酸钠溶液与盐酸反应:
①向盐酸中逐滴加入碳酸钠溶液至反应完全
化学方程式:Na2CO3+2HCl===CO2↑+H2O+2NaCl
离子方程式:CO+2H+===CO2↑+H2O
②向碳酸钠溶液中逐滴加入盐酸至反应完全
化学方程式:Na2CO3+HCl===NaHCO3+NaCl
离子方程式:CO+H+===HCO
4.氧化还原型、且与“量”和“反应顺序”有关的离子反应
此类离子反应方程式的书写较为复杂,不仅涉及氧化还原的先后顺序,还涉及氧化剂与还原剂物质的量的配比。书写此类离子方程式,需先理清溶液中存在的氧化剂和还原剂的种类,根据氧化性强弱和还原性强弱分别排序,以确定反应先后顺序,并写出分步的离子反应方程式;最后根据题目中相对量的关系书写总反应方程式。
例:FeBr2溶液与氯气反应的问题,溶液中存在的氧化剂为Cl2,还原剂有Fe2+、Br-,根据氧化还原性强弱排序:Fe2+>Br-,则通入Cl2时,
①Cl2不足时,只有Fe2+被Cl2氧化,
如:当n(Cl2)∶n(FeBr2)≤0.5时,发生下列反应:
化学方程式:FeBr2+1/2Cl2===1/3FeCl3+2/3FeBr3
离子方程式:2Fe2++Cl2===2Fe3++2Cl-
②当Fe2+完全反应后,即n(Cl2)∶n(Fe2+)>0.5时,Br-开始被氧化,发生反应2Br-+Cl2===2Cl-+Br2;结合反应Fe2+和Br-的物质的量之比以及①中反应方程式,书写总反应方程式。
如:当n(Cl2)∶n(FeBr2)=1∶1时,Fe2+全部被Cl2氧化,Br-部分被氧化,反应的n(Fe2+)∶n(Br-)=1∶1,则总反应式为:
即当n(Cl2)∶n(FeBr2)=1∶1时,离子方程式为2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2
③当Cl2过量时,即当n(Cl2)∶n(FeBr2)≥1.5时,Fe2+、Br-均全部被Cl2氧化,发生下列反应:
化学方程式:2FeBr2+3Cl2===2FeCl3+2Br2
离子方程式:2Fe2++4Br-+3Cl2===2Fe3++6Cl-+2Br2
【例1】 下列物质属于电解质且能导电的是( )
A.石墨 B.液态HCl C.葡萄糖 D.熔融的Na2CO3
【解析】 A项,石墨能够导电,但不是化合物,不属于电解质;
B项,液态HCl属于电解质,但该状态的HCl以分子形式存在,不存在自由移动的离子,因此不能导电;
C项,葡萄糖以分子形式存在,熔融状态或水溶液中均不能导电,故不属于电解质;
D项,Na2CO3属于电解质,且熔融状态下能够电离出自由移动的离子,故为正确答案。
【答案】 D
【提炼】 在水溶液里或熔融状态下能导电的化合物叫电解质。化合物本身导电的前提:其内部存在着自由移动的阴阳离子。离子化合物在水溶液中或熔融状态下能导电;而某些共价化合物也能在水溶液中导电(如HCl),其他为非电解质。
能导电的不一定是电解质。判断某化合物是否是电解质,不能只凭它在水溶液中导电与否,还需要进一步考察其晶体结构和化学键的性质等因素。例如,判断硫酸钡、碳酸钙和氢氧化铁是否为电解质。硫酸钡难溶于水(20 ℃时在水中的溶解度为2.4×10-4g),溶液中离子浓度很小,其水溶液不导电,似乎为非电解质。但溶于水的那小部分硫酸钡却几乎完全电离(20 ℃时硫酸钡饱和溶液的电离度为97.5%)。因此,硫酸钡是电解质。碳酸钙和硫酸钡具有相类似的情况,也是电解质。从结构看,对其他难溶盐,只要是离子型化合物或强极性共价型化合物,尽管难溶,也是电解质。
【例2】 下列叙述中,能说明某化合物一定是弱电解质的是( )
A.该化合物饱和溶液导电能力较弱
B.该化合物在熔融时不导电
C.该化合物水溶液和熔融状态均不导电
D.该化合物溶于水中发生电离,溶质离子浓度小于溶质分子浓度
【解析】 A.溶液导电能力与溶液中离子浓度大小和离子所带电荷的多少有关,若该化合物在水中的溶解度较小,则离子浓度较小,则饱和溶液导电能力较弱,如BaSO4;
B.熔融状态下不导电的化合物可能是非电解质,如蔗糖;也可能是强电解质,如HCl;
C.该化合物水溶液和熔融状态均不导电则为非电解质,不属于弱电解质;
D.若溶质离子浓度小于溶质分子浓度,说明该化合物电离时不完全,则为弱电解质。
【答案】 D
【提炼】 强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强。如浓度为4 mol/L的醋酸溶液导电能力要强于0.001 mol/L的盐酸溶液,因为前者溶液中自由移动的离子浓度更大。
【例3】 下列离子方程式正确的是( )
A.用食醋除水垢的原理:2H++CaCO3===Ca2++H2O+CO2↑
B.金属钠投入MgCl2溶液中:2Na+Mg2+===2Na++Mg
C.0.1 mol·L-1NaHSO4溶液和0.1 mol·L-1Ba(OH)2溶液等体积混合:H++SO+Ba2++OH-===BaSO4↓+H2O
D.碳酸氢铵溶液和足量氢氧化钠溶液反应:OH-+NHNH3·H2O
【解析】 A项醋酸为弱电解质,不能拆;B项金属钠投入MgCl2溶液中,钠应先与水反应,生成氢氧化钠与氢气,然后有氢氧化镁沉淀生成;C项正确;D项碳酸氢根离子也会与氢氧化钠反应。
【答案】 C
【提炼】 离子方程式书写时物质拆分注意点:1.难溶物不拆,如CaCO3、BaSO4、AgCl、Cu(OH)2、H2SiO3等在书写离子方程式时均不能拆开,应写成化学式;2.微溶物作生成物不拆,如CaSO4、Ag2SO4、MgCO3、Ca(OH)2等微溶物,若作为生成物在书写离子方程式时均不能拆开,应写成化学式。说明:微溶物作反应物,浓度较小时拆成离子式,浓度较大时应写成化学式;3.弱电解质不拆,如H2O、HF、CH3COOH等弱电解质在书写离子方程式时均不能拆开,应写成化学式;4.氧化物不拆,氧化物不论是否溶于水,在书写离子方程式时均不能拆开,应写成化学式;5.弱酸的酸式酸根不拆,如HCO、HSO、HS-、H2PO等离子在书写离子方程式时均不能拆开,应写成化学式。注意:对于强酸的酸式盐,如NaHSO4其阴离子在稀溶液中应拆开写成H+与SO形式,在浓溶液中不拆开,仍写成HSO。
【例4】 在500 mL Fe2(SO4)3、CuSO4的混合液中,金属阳离子的浓度均为2.0 mol·L-1,现加入a mol铁粉,充分振荡反应后,下列说法不正确的是( )
A.当a≤0.5时,发生的反应为2Fe3++Fe===3Fe2+
B.当a=1时,发生的反应为2Fe3++Cu2++2Fe===4Fe2++Cu
C.当0.5≤a<1.5时,溶液中Cu2+、Fe2+、SO的物质的量之比为(3-2a)∶(2+2a)∶5
D.当a≥1.5时,反应中电子转移数目大于3NA
【解析】 混合溶液中加入铁粉后,首先发生反应为2Fe3++Fe===3Fe2+,当Fe3+反应完后,铁粉还会与Cu2+继续发生反应:Cu2++Fe===Fe2++Cu,原溶液中n(Fe3+)=1 mol,n(Cu2+)=1 mol。当a≤0.5时,发生的反应为2Fe3++Fe===3Fe2+,A正确;当a=1时,0.5 mol Fe与Fe3+发生反应2Fe3++Fe===3Fe2+,剩余的0.5 mol Fe与Cu2+发生反应:Cu2++Fe===Fe2++Cu,两个方程式合在一起为2Fe3++Cu2++2Fe===4Fe2++Cu,B正确;当0.5≤a<1.5时,a mol Fe完全转化成a mol Fe2+,1 mol Fe3+转化成1 mol Fe2+,反应后溶液中n(Fe2+)=(1+a) mol,1 mol Cu2+发生部分转化,剩余的Cu2+为[1-(a-0.5)] mol,n(SO)=2.5 mol,C正确;当a≥1.5时,1 mol Fe3+、1 mol Cu2+完全反应,电子转移数目为3NA,D
错误。
【答案】 D
【提炼】 一种氧化剂多种还原剂的体系中,须先将还原剂按还原性强弱顺序排列,写出不断加入氧化剂过程中依次发生的氧化还原反应,再由此分析解答。
【例5】 为了探究不溶性盐X(仅含5种元素)的组成和性质,设计并完成如下实验(所加试剂均过量,气体体积均在标准状况下测定)。
请回答:
(1)X的组成元素为H、O和____________(用元素符号表示),气体C的电子式为________。
(2)写出反应①的离子方程式:________________________________________________________________________。
【解析】 根据实验现象结合相关物质的性质,分析判断元素种类。根据相关物质的物质的量计算X的组成。A气体使品红溶液褪色,A是SO2,物质的量是0.1 mol,说明X中含有亚硫酸根或亚硫酸氢根离子。B是红色固体,应该是铜,物质的量是0.05 mol;蓝色溶液和氢氧化钠反应生成C气体和蓝色沉淀,说明C是氨气,物质的量是0.1 mol,即X中含有铵根;蓝色沉淀灼烧生成黑色固体D,D是氧化铜,物质的量是0.05 mol。因此铜元素的物质的量是0.1 mol,则X中铜元素、铵根和亚硫酸根(或亚硫酸氢根)的物质的量之比是1∶1∶1,而0.1 mol NH4CuSO3的质量恰好是16.2 g。
(1)根据以上分析可知X的组成元素为H、O和N、S、Cu。氨气的电子式为HN··, H。
(2)根据以上分析可知反应①的离子方程式为2NH4CuSO3+4H+===Cu+Cu2++2SO2↑+2H2O+2NH。
【答案】 (1)N、S、Cu (2)HN··, H (3)2NH4CuSO3+4H+===Cu+Cu2++2SO2↑+2H2O+2NH
【提炼】 在无机推断题中也往往涉及离子方程式的书写。首先应充分利用实验流程中的信息,抓住流程中的数字、颜色、所加物质等关键信息,寻找突破口,注意联系、大胆假设,全面分析,综合判断物质的组成元素、化学式以及发生反应的化学方程式。而检查离子方程式是否正确,主要从以下几个方面检查:①检查反应能否发生;②检查反应物、生成物是否正确;③检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式;④检查是否符合守恒关系;⑤检查是否符合原化学方程式等。
相关文档
- 2021届高考化学一轮复习化学反应速2021-07-0815页
- 2019届一轮复习化学实验常用仪器和2021-07-0816页
- 2020届高考化学一轮复习化学反应速2021-07-086页
- 2020届高考化学一轮复习化学资源的2021-07-0815页
- 2020届高考化学一轮复习化学计量在2021-07-0811页
- 2020届高考化学一轮复习化学反应与2021-07-088页
- 2020届高考化学一轮复习化学反应中2021-07-089页
- 2020届高考化学一轮复习化学实验常2021-07-0828页
- 2021届(鲁科版)高考化学一轮复习化学2021-07-088页
- 2020届高考化学一轮复习化学反应与2021-07-0821页