- 188.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
高考中的新型化学电源
命题分析:以新型化学电源为命题背景考查原电池的结构和工作原理是高考的热点;涉及的新型化学电源种类繁多,如储氢电池、高铁电池、海洋电池、锂离子电池等。解答此类题,不要被新材料、新情境所吓倒,只要学会迁移运用常见化学电源工作原理,正确判断正负极,写出电极反应式就能破题。
突破方法
1.正、负极的判断
2.放电时正极、负极电极反应式的书写
(1)首先分析物质得失电子的情况。
(2)然后再考虑电极反应生成的物质是否跟电解质溶液中的离子发生反应。
(3)对于较为复杂的电极反应,可以利用“总反应式-较简单一极的电极反应式=较复杂一极的电极反应式”的方法解决。
3.充电时阴极、阳极的判断
(1)首先应搞明白原电池放电时的正、负极。
(2)再根据电池充电时阳极接正极、阴极接负极的原理进行分析。
(3)电极反应式:放电时的负极与充电时的阴极、放电时的正极与充电时的阳极分别互逆。
4.可充电电池的分析
(1)“正正负负”——原电池的正极充电时要与外接电源的正极相连,原电池的负极充电时要与外接电源的负极相连。
(2)“颠颠倒倒”——原电池的正极反应倒过来,就是充电时电解池的阳极反应式。原电池的负极反应倒过来,就是充电时电解池的阴极反应式。
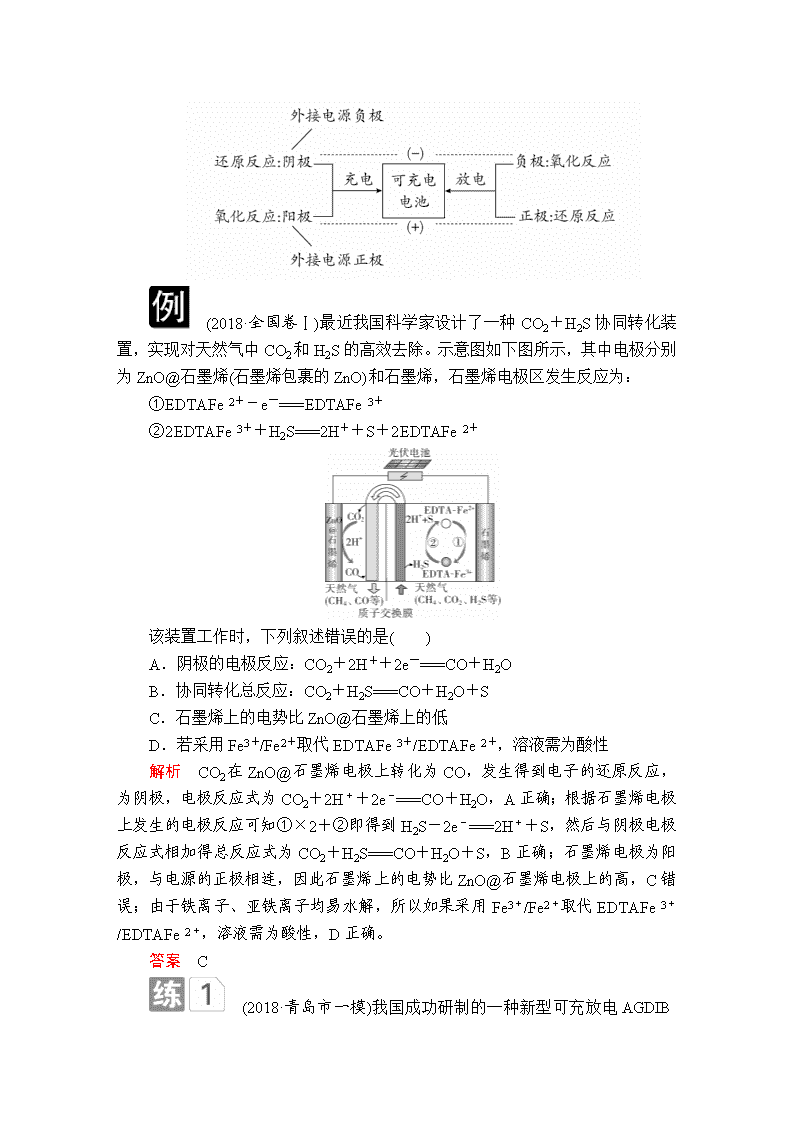
(2018·全国卷Ⅰ)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如下图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTAFe2+-e-===EDTAFe3+
②2EDTAFe3++H2S===2H++S+2EDTAFe2+
该装置工作时,下列叙述错误的是( )
A.阴极的电极反应:CO2+2H++2e-===CO+H2O
B.协同转化总反应:CO2+H2S===CO+H2O+S
C.石墨烯上的电势比ZnO@石墨烯上的低
D.若采用Fe3+/Fe2+取代EDTAFe3+/EDTAFe2+,溶液需为酸性
解析 CO2在ZnO@石墨烯电极上转化为CO,发生得到电子的还原反应,为阴极,电极反应式为CO2+2H++2e-===CO+H2O,A正确;根据石墨烯电极上发生的电极反应可知①×2+②即得到H2S-2e-===2H++S,然后与阴极电极反应式相加得总反应式为CO2+H2S===CO+H2O+S,B正确;石墨烯电极为阳极,与电源的正极相连,因此石墨烯上的电势比ZnO@石墨烯电极上的高,C错误;由于铁离子、亚铁离子均易水解,所以如果采用Fe3+/Fe2+取代EDTAFe3+/EDTAFe2+,溶液需为酸性,D正确。
答案 C
(2018·青岛市一模)
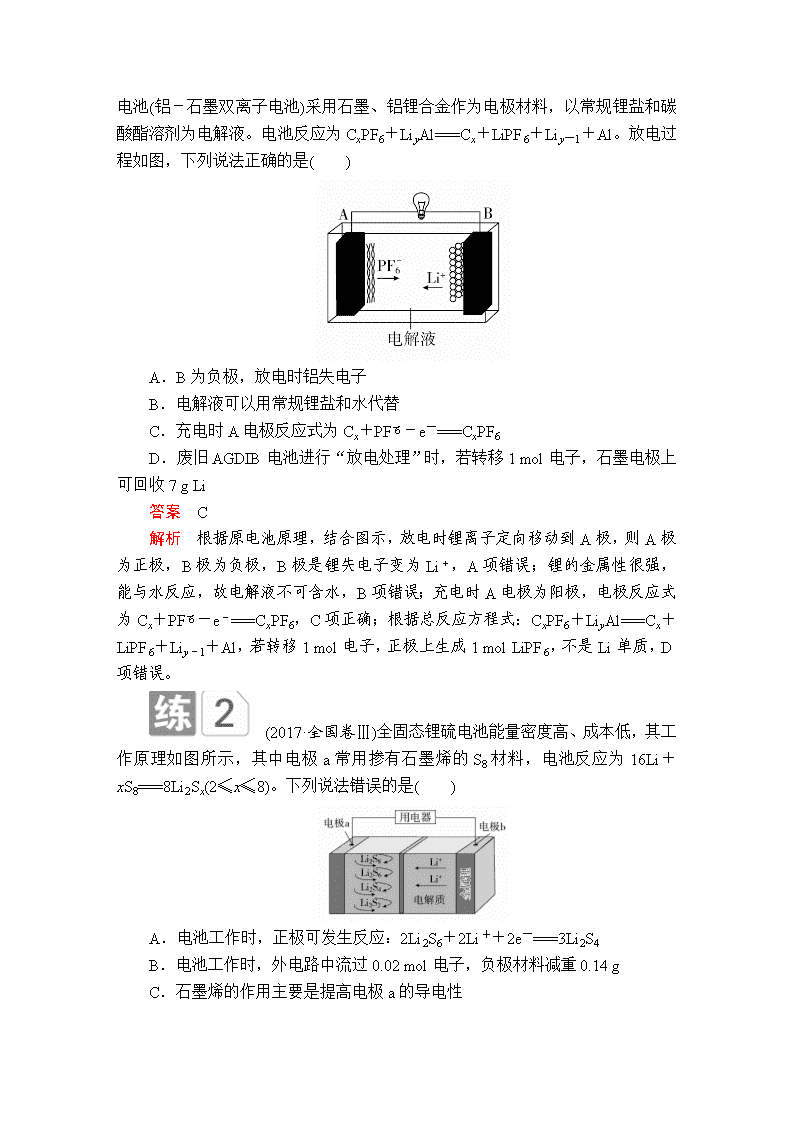
我国成功研制的一种新型可充放电AGDIB电池(铝-石墨双离子电池)采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池反应为CxPF6+LiyAl===Cx+LiPF6+Liy-1+Al。放电过程如图,下列说法正确的是( )
A.B为负极,放电时铝失电子
B.电解液可以用常规锂盐和水代替
C.充电时A电极反应式为Cx+PF-e-===CxPF6
D.废旧AGDIB电池进行“放电处理”时,若转移1 mol电子,石墨电极上可回收7 g Li
答案 C
解析 根据原电池原理,结合图示,放电时锂离子定向移动到A极,则A极为正极,B极为负极,B极是锂失电子变为Li+,A项错误;锂的金属性很强,能与水反应,故电解液不可含水,B项错误;充电时A电极为阳极,电极反应式为Cx+PF-e-===CxPF6,C项正确;根据总反应方程式:CxPF6+LiyAl===Cx+LiPF6+Liy-1+Al,若转移1 mol电子,正极上生成1 mol LiPF6,不是Li单质,D项错误。
(2017·全国卷Ⅲ)全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为16Li+xS8===8Li2Sx(2≤x≤8)。下列说法错误的是( )
A.电池工作时,正极可发生反应:2Li2S6+2Li++2e-===3Li2S4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中Li2S2的量越多
答案 D
解析 A对:原电池工作时,Li+向正极移动,则a为正极,正极上发生还原反应,a极发生的电极反应有S8+2Li++2e-===Li2S8、3Li2S8+2Li++2e-===4Li2S6、2Li2S6+2Li++2e-===3Li2S4、Li2S4+2Li++2e-===2Li2S2等。B对:电池工作时,外电路中流过0.02 mol电子时,氧化Li的物质的量为0.02 mol,质量为0.14 g。C对:石墨烯能导电,利用石墨烯作电极,可提高电极a的导电性。D错:电池充电时电极a发生反应:2Li2S2-2e-===Li2S4+2Li+,充电时间越长,电池中Li2S2的量越少。
相关文档
- 2020版高考一轮复习化学通用版学案2021-07-0821页
- 2020届高考化学一轮复习化学能与热2021-07-086页
- 2020届高考化学一轮复习化学反应与2021-07-085页
- 2020届高考化学一轮复习化学平衡学2021-07-0833页
- 2020届高考化学一轮复习化学反应原2021-07-0832页
- 2020届高考化学一轮复习化学平衡状2021-07-0830页
- 2021届高考化学一轮复习化学反应速2021-07-0818页
- 2020届高考化学一轮复习化学与自然2021-07-0823页
- 2021届高考化学一轮复习化学计算中2021-07-086页
- 2021届高考化学一轮复习化学反应速2021-07-0810页