- 806.50 KB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第29讲 电解池 金属的腐蚀和防护
1.电解池
(1)定义:电解池是把电能转变为化学能的装置。
(2)电解池的构成条件
①有外接直流电源。
②有与电源相连的两个电极。
③形成闭合回路。
④电解质溶液或熔融电解质。
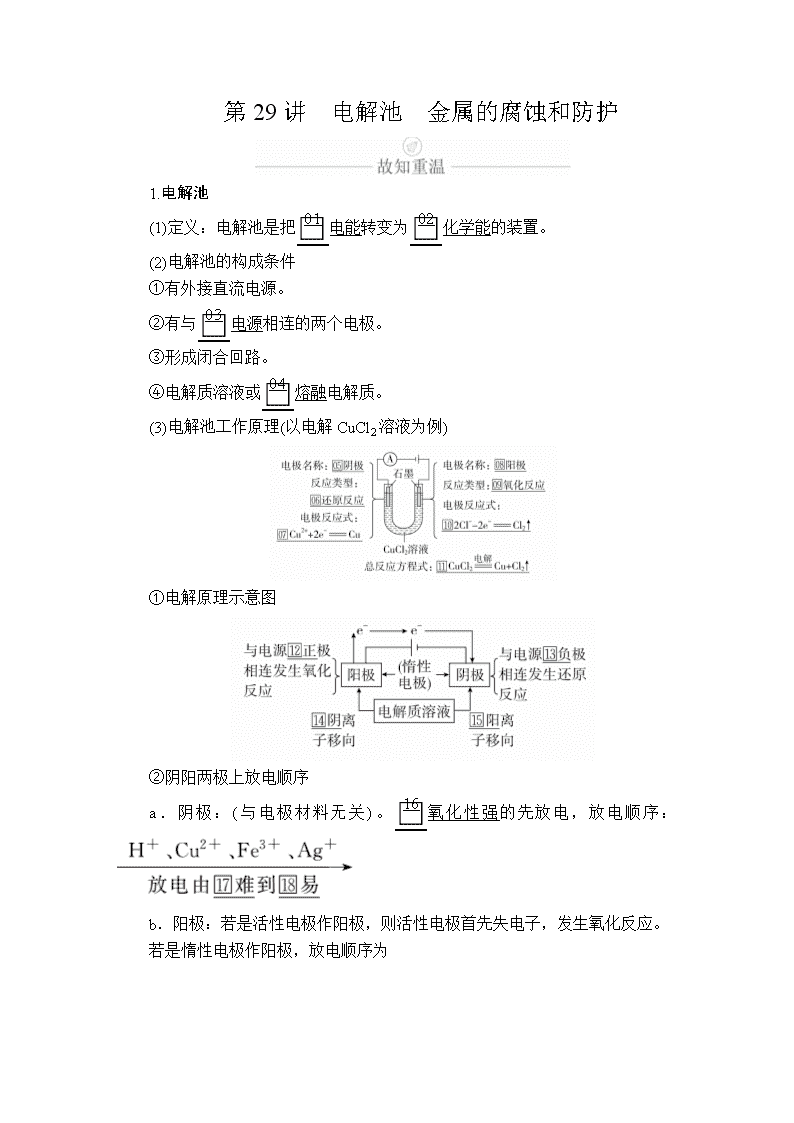
(3)电解池工作原理(以电解CuCl2溶液为例)
①电解原理示意图
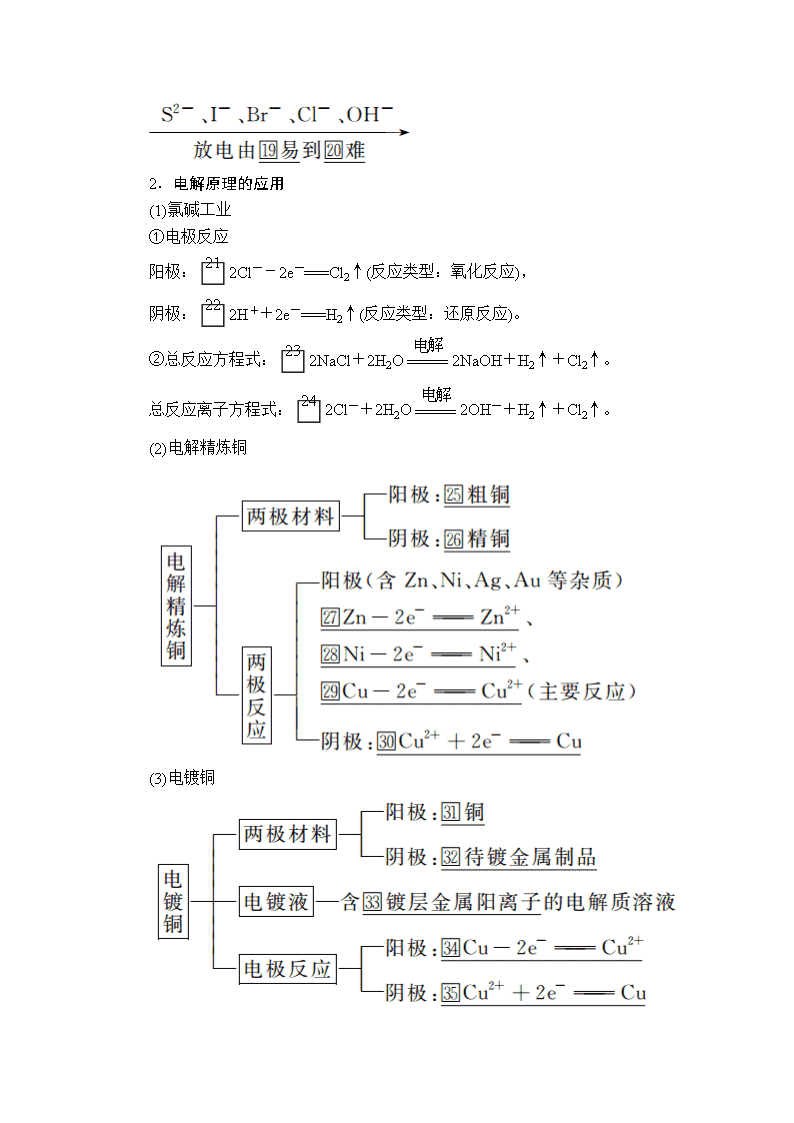
②阴阳两极上放电顺序
a.阴极:(与电极材料无关)。氧化性强的先放电,放电顺序:
b.阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应。
若是惰性电极作阳极,放电顺序为
2.电解原理的应用
(1)氯碱工业
①电极反应
阳极:2Cl--2e-===Cl2↑(反应类型:氧化反应),
阴极:2H++2e-===H2↑(反应类型:还原反应)。
②总反应方程式:2NaCl+2H2O2NaOH+H2↑+Cl2↑。
总反应离子方程式:2Cl-+2H2O2OH-+H2↑+Cl2↑。
(2)电解精炼铜
(3)电镀铜
(4)电冶金
利用电解熔融盐(或氧化物)的方法来冶炼活泼金属Na、Ca、Mg、Al等。
3.金属的腐蚀和防护
(1)金属腐蚀的本质
金属原子失去电子变成金属阳离子,金属发生氧化反应。
(2)金属腐蚀的类型
①化学腐蚀与电化学腐蚀
②析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
铁锈的形成:2Fe+O2+2H2O===2Fe(OH)2,
4Fe(OH)2+O2+2H2O===4Fe(OH)3,2Fe(OH)3+(x-3)H2O===Fe2O3·xH2O(铁锈)。
(3)金属的防护
1.判断正误,正确的画“√”,错误的画“×”,并指明错因。
(1)电解质溶液的导电过程就是电解质溶液被电解的过程。(√)
错因:_____________________________________________________________
(2)电解CuCl2溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色。(×)
错因:电解CuCl2溶液时,阴极生成Cu。
(3)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大。(×)
错因:电解H2SO4溶液是电解水,c(H+)增大,pH减小。
(4)电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变。(×)
错因:电解精炼铜时,电解质溶液中c(Cu2+)减小。
(5)用惰性电极电解饱和食盐水一段时间后,加入盐酸可使电解质溶液恢复到电解前的状态。(×)
错因:电解饱和食盐水一段时间后,通入适量的HCl会恢复到电解前的状态,加盐酸会使溶液浓度变稀。
(6)电解饱和食盐水时,两个电极均不能用金属材料。(×)
错因:电解饱和食盐水时,可用金属材料。
(7)在镀件上电镀铜时,镀件应连接电源的正极。(×)
错因:镀件上镀铜时,镀件连接电源的负极。
2.教材改编题
(据人教选修四P88 T6)下列说法不正确的是( )
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比纯铁容易生锈
C.铁质器件附有铜质配件,在接触处不易生铁锈
D.用锡焊接的铁质器件,焊接处易生锈
答案 C
考点 电解原理及应用
[典例1] (2016·全国卷Ⅰ)三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的SO离子向阳极迁移,阳极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.阴极反应为2H2O-4e-===O2+4H+,阴极区溶液pH降低
D.当电路中通过1 mol电子的电量时,会有0.5 mol的O2生成
解析 阳极区域水电离出的OH-放电,溶液中c(H+)增大,pH减小,中间隔室的SO透过cd膜移到阳极区可得产品H2SO4;阴极区水电离出的H+放电:2H++2e-===H2↑,溶液中c(OH-)增大,溶液pH增大,中间隔室的Na+透过ab膜移入阴极区,可得产品NaOH;由得失电子守恒,结合电极反应4OH--4e-===2H2O+O2↑可知,通过1 mol e-会有0.25 mol O2产生。
答案 B
名师精讲
1.以惰性电极电解电解质溶液的规律
2.电极反应式的书写步骤与方法
3.电解原理应用的注意事项
(1)阳离子交换膜(以电解NaCl溶液为例),只允许阳离子(Na+)通过,而阻止阴离子(Cl-、OH-)和分子(Cl2)通过,这样既能防止H2和Cl2混合发生爆炸,又能避免Cl2和NaOH溶液作用生成NaClO影响烧碱的质量。
(2)电解或电镀时,电极质量减少的电极必为金属电极——阳极;电极质量增加的电极必为阴极,即溶液中的金属阳离子得电子变成金属吸附在阴极上。
(3)电解精炼铜,粗铜中含有的Zn、Fe、Ni等活泼金属失去电子,变成金属阳离子进入溶液,其他活泼性弱于铜的杂质以阳极泥的形式沉积。电解过程中电解质溶液中的Cu2+浓度会逐渐减小。
(4)电镀时,阳极(镀层金属)失去电子的数目跟阴极镀层金属离子得到电子的数目相等,因此电镀液中电解质的浓度保持不变。
1.用图甲装置电解一定量的CuSO4溶液,M、N为惰性电极。电解过程实验数据如图乙所示。横轴表示电解过程中转移电子的物质的量,纵轴表示电解过程产生气体的总体积。下列说法不正确的是( )
A.A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态
B.电解过程中N电极表面先有红色物质生成,后有气泡产生
C.Q点时M、N两电极上产生的总气体在相同条件下体积相同
D.若M电极材料换成Cu,则电解过程中CuSO4溶液的浓度不变
答案 A
解析 惰性材料作电极,在阳极上H2O先放电,即阳极的电极反应式为2H2O-4e-===O2↑+4H+,在阴极,Cu2+先放电,即阴极的电极反应式为Cu2++2e-===Cu,P点后,气体体积突然增大,说明P点Cu2+消耗完全,P点后,阴极的电极反应式是2H++2e-===H2↑,即A点是电解完CuSO4后,又电解了一部分水,应加入CuO和H2O,才能恢复到原来的状态,故A说法错误;N极接电源的负极,N极作阴极,根据选项A的分析,先有红色铜析出,然后出现气体,故B说法正确;Q点的气体来自两个阶段,第一阶段:阳极电极反应式为2H2O-4e-===4H++O2↑,阴极电极反应式为Cu2++2e-===Cu,第二阶段:阳极电极反应式为2H2O-4e-===4H++O2↑,阴极反应式为2H++2e-===H2↑,P点产生的气体为氧气,其体积为b L,从P点到Q点,第二阶段,阴极产生的气体体积为2b L,阳极产生的气体体积为b L,阳极气体总体积为(b+b) L=2b L,故C说法正确;若M电极换成Cu,阳极上发生反应Cu-2e-===Cu2+,阴极反应式为Cu2++2e-===Cu,因此电解过程中CuSO4溶液的浓度不变,故D说法正确。
2.氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
(1)写出电解饱和食盐水的离子方程式:_____________________________________________________________________。
(2)离子交换膜的作用为___________________________________________________________________________________________________________________________________________、
________________________________________________________________________。
(3)精制饱和食盐水从图中________位置补充,氢氧化钠溶液从图中________(选填“a”“b”“c”或“d”)位置流出。
答案 (1)2Cl-+2H2OCl2↑+H2↑+2OH-
(2)阻止OH-进入阳极室与Cl2发生副反应:2NaOH+Cl2===NaCl+NaClO+H2O,以便得到纯度更高的氢氧化钠溶液 阻止阳极产生的Cl2和阴极产生的H2混合发生爆炸
(3)a d
解析 (1)电解饱和食盐水时,溶液中的阳离子H+在阴极得到电子变为H2逸出,使附近的水溶液显碱性,溶液中的阴离子Cl-在阳极失去电子产生Cl2。该电解反应的离子方程式是2Cl-+2H2OCl2↑+H2↑+2OH-。
(2)图中的离子交换膜是阳离子交换膜,可以允许阳离子通过,不能使阴离子通过,这样就可以阻止阴极溶液中的OH-进入阳极室与氯气发生反应,阻止Cl-进入阴极室,使在阴极区产生的NaOH纯度更高。同时可以阻止阳极产生的Cl2和阴极产生的H2混合发生爆炸。
(3)随着电解的进行,溶质NaCl不断消耗,所以应该及时补充。精制饱和食盐水从阳极补充,即从图中a位置补充,由于阴极H+不断放电,附近的溶液显碱性,氢氧化钠溶液从图中d位置流出;从c位置流出的是稀的NaCl溶液。
考点 金属的电化学腐蚀与防护
[典例2] (2017·全国卷Ⅰ)支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
解析 外加强大的电流可以抑制金属电化学腐蚀产生的电流,A正确;被保护的钢管桩作阴极,高硅铸铁作阳极,电解池中外电路电子由阳极流向阴极,即从高硅铸铁流向钢管桩,B正确;高硅铸铁为惰性辅助阳极,其主要作用是传递电流,而不是作为损耗阳极,C错误;保护电流要抑制金属电化学腐蚀产生的电流,应根据环境条件变化进行调整,D正确。
答案 C
名师精讲
1.判断金属腐蚀快慢的规律
(1)对同一电解质溶液来说,腐蚀速率的快慢:电解池原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐措施的腐蚀。
(2)对同一金属来说,在同浓度的不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液中。
(3)活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。
2.金属腐蚀的防护
(1)电化学保护法
①牺牲锌(负极)保护铁(正极),习惯上叫做牺牲阳极的阴极保护法。如船壳上钉上锌块形成原电池。
②外加电流的阴极保护法:钢铁外接电源负极形成电解池,使之成为阴极而被保护。如钢闸门接低压直流电负极,石墨接电源正极作阳极,浸入水中。
(2)两种保护方法的比较
外加电流的阴极保护法保护效果大于牺牲阳极的阴极保护法。
3.铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图所示。下列说法不正确的是( )
A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C.铜极上的反应是2H++2e-===H2↑、O2+4e-+4H+===2H2O
D.在金属表面涂一层油脂,能防止铁铆钉被腐蚀
答案 B
解析 铁、铜和水膜形成原电池,因为铁的金属性比铜强,所以铁为负极,铁铆钉被氧化而腐蚀,A正确;若水膜中溶解了SO2,则发生析氢腐蚀,铁铆钉腐蚀的速率加快,B错误;铜极发生还原反应,根据题图知铜电极吸收了氧气且生成氢气,所以发生两个电极反应:2H++2e-===H2↑、O2+4e-+4H+===2H2O,C正确;在金属表面涂一层油脂,可隔绝空气和水,能防止铁铆钉被腐蚀,D正确。
4.(2016·浙江高考)在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生的总化学方程式为2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如下图。下列说法正确的是( )
A.铁片发生还原反应而被腐蚀
B.铁片腐蚀最严重的区域应该是生锈最多的区域
C.铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-===4OH-
D.铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
答案 D
解析 铁失去电子变为Fe2+,发生氧化反应而被腐蚀,A错误;由于得失电子在不同的区域,所以铁片腐蚀最严重的区域与生锈最多的区域是不同的区域,B错误;铁片腐蚀中正极发生的电极反应为2H2O+O2+4e-===4OH-,C错误;D正确。
考点 有关电解的计算
[典例3] (2018·兰州质检)将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为( )
A.4×10-3 mol·L-1 B.2×10-3 mol·L-1
C.1×10-3 mol·L-1 D.1×10-7 mol·L-1
解析 根据2CuSO4+2H2O2Cu+2H2SO4+O2↑,得n(H+)=2n(H2SO4)=2n(Cu)=2×=0.002 mol,c(H+)==4×10-3 mol·L-1。
答案 A
名师精讲
电化学的有关计算方法
原电池和电解池的计算,主要包括两极产物的定量计算、相对原子质量的计算、阿伏加德罗常数测定的计算、溶液pH的计算,根据产物的量求电量及根据电量求产物的量等。在进行有关计算时,可运用以下基本方法:
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据得失电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相等。
②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒关系建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
该关系式具有总揽电化学计算的作用,熟记电极反应式,灵活运用关系式便能快速解答常见的电化学计算问题。
提示 在电化学计算中,还常利用Q=I·t和Q=n(e-)×NA×1.60×10-19 C来计算电路中通过的电量。
5.(2018·华中师大附中期末)用惰性电极电解100 mL 3 mol·L-1的Cu(NO3)2溶液,一段时间后在阳极收集到标准状况下气体1.12 L,停止电解,向电解后的溶液中加入足量的铁粉,充分作用后溶液中Fe2+浓度为(设溶液体积不变)( )
A.3 mol·L-1 B.2.75 mol·L-1
C.2 mol·L-1 D.3.75 mol·L-1
答案 B
解析 阳极反应式为2H2O-4e-===4H++O2↑,阴极反应式为Cu2++2e-===Cu,阳极生成的气体为氧气,氧气的物质的量为1.12 L÷22.4 L·mol-1=0.05 mol,则
2Cu(NO3)2+2H2O2Cu↓+O2↑ + 4HNO3
2 1 4
0.1 mol 0.05 mol 0.2mol
故电解后溶液中生成的HNO3的物质的量为0.2
mol。电解后溶液中硝酸铜的物质的量为0.1 L×3 mol·L-1-0.1 mol=0.2 mol,硝酸与足量的铁反应生成硝酸亚铁,反应方程式为8HNO3+3Fe===3Fe(NO3)2+2NO↑+4H2O,故0.2 mol HNO3生成Fe(NO3)2的物质的量为0.2 mol×3/8=0.075 mol,硝酸铜与铁反应生成硝酸亚铁,离子方程式为Fe+Cu2+===Fe2++Cu,故0.2 mol硝酸铜生成Fe(NO3)2的物质的量为0.2 mol,反应后溶液中Fe2+的物质的量为0.2 mol+0.075 mol=0.275 mol,反应后溶液中Fe2+浓度为0.275 mol/0.1 L=2.75 mol·L-1,选B。
6.如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5% NaOH溶液、足量CuSO4溶液和100 g 10% K2SO4溶液,电极均为石墨电极。
(1)接通电源,一段时间后,测得丙中K2SO4溶液的溶质质量分数为10.47%,乙中c电极质量增加。则
①电源的N端为________极;
②电极b上发生的电极反应为____________________;
③计算电极b上生成的气体在标准状况下的体积为________L;
④电解前后丙中溶液的pH________(填“增大”“减小”或“不变”)。
(2)乙装置中如果电解过程中铜全部析出,此时电解能否继续进行:________(填“能”或“不能”),原因是____________________________________________。
答案 (1)①正 ②4OH--4e-===O2↑+2H2O
③2.8 ④不变
(2)能 CuSO4溶液变为H2SO4溶液,可继续电解H2SO4溶液,相当于电解水
解析 (1)①接通电源一段时间后,乙中c电极质量增加,说明c电极表面析出Cu,则该电极为阴极,从而推知M端为电源的负极,N端为电源的正极。
②电极b为阳极,用惰性电极电解NaOH溶液相当于电解水,阳极上OH-放电生成O2,电极反应式为4OH--4e-===O2↑+2H2O。
③用惰性电极电解K2SO4溶液相当于电解水,设电解过程中消耗水的质量为x g,据电解前后溶质的质量不变可得:100 g×10%=(100-x) g×10.47%,解得x≈4.5,则电解过程中消耗水的物质的量为=0.25 mol,转移电子的物质的量为0.5 mol,故电极b上生成的O2在标准状况下的体积为V(O2)=0.5 mol×
eq f(1,4)×22.4 L·mol-1=2.8 L。
④丙中用惰性电极电解K2SO4溶液相当于电解水,电解过程中c(K2SO4)增大,但溶液的pH不变。
(2)当电解过程中铜全部析出时,CuSO4溶液变为H2SO4溶液,继续电解则为电解H2SO4溶液,相当于电解水。
相关文档
- 2020届高考化学一轮复习化学反应与2021-07-0911页
- 2021届高考化学一轮复习化学反应速2021-07-099页
- 2020届高考化学一轮复习化学反应速2021-07-0913页
- 2020届高考化学一轮复习化学反应速2021-07-094页
- 2021届高考化学一轮复习化学平衡常2021-07-0916页
- 2020届高考化学一轮复习化学平衡状2021-07-099页
- 2020年高考化学一轮复习化学反应速2021-07-0913页
- 2021届(鲁科版)高考化学一轮复习化学2021-07-098页
- 2020届高考化学一轮复习化学与材料2021-07-0910页
- 2021届高考化学一轮复习化学反应速2021-07-0913页