- 323.98 KB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第二节 烃和卤代烃
[高考备考指南]
考纲定位
1.掌握烷、烯、炔和芳香烃的结构与性质。
2.掌握卤代烃的结构与性质,以及与烃的衍生物之间的相互转化。
3.了解烃类及衍生物的重要应用以及卤代烃的合成方法。
4.了解有机分子中官能团之间的相互影响。
核心素养
1.变化观念——烃和卤代烃的性质及其利用。
2.科学探究——烃和卤代烃的化学性质的实验探究。
3.模型认知——运用烃和卤代烃的分子结构模型解释对应的化学性质。
4.社会责任——烃和卤代烃对发展的贡献以及相关的环境问题和绿色化学思想。
脂肪烃
(对应复习讲义第141页)
1.组成、结构特点和通式
2.脂肪烃代表物——甲烷、乙烯、乙炔的组成和结构
名称
分子式
结构式
结构简式
电子式
立体
构型
甲烷
CH4
CHHHH
CH4
H∶CH
H ∶H
正四面体
乙烯
C2H4
CHHCHH
CH2===CH2
H∶CH__∶∶CH__∶H
平面形
乙炔
C2H2
H—C≡C—H
CH≡CH
H∶C⋮⋮C∶H
直线形
3.物理性质递变规律
状态常温下,含有1~4个碳原子的烃为气态,随碳原子数的增多,逐渐过渡到液态、固态沸点随着碳原子数增多,沸点逐渐升高;同分异构体中,支链越多,沸点越低相对密度随着碳原子数的增多,相对密度逐渐增大,密度均比水小水溶性
4.化学性质
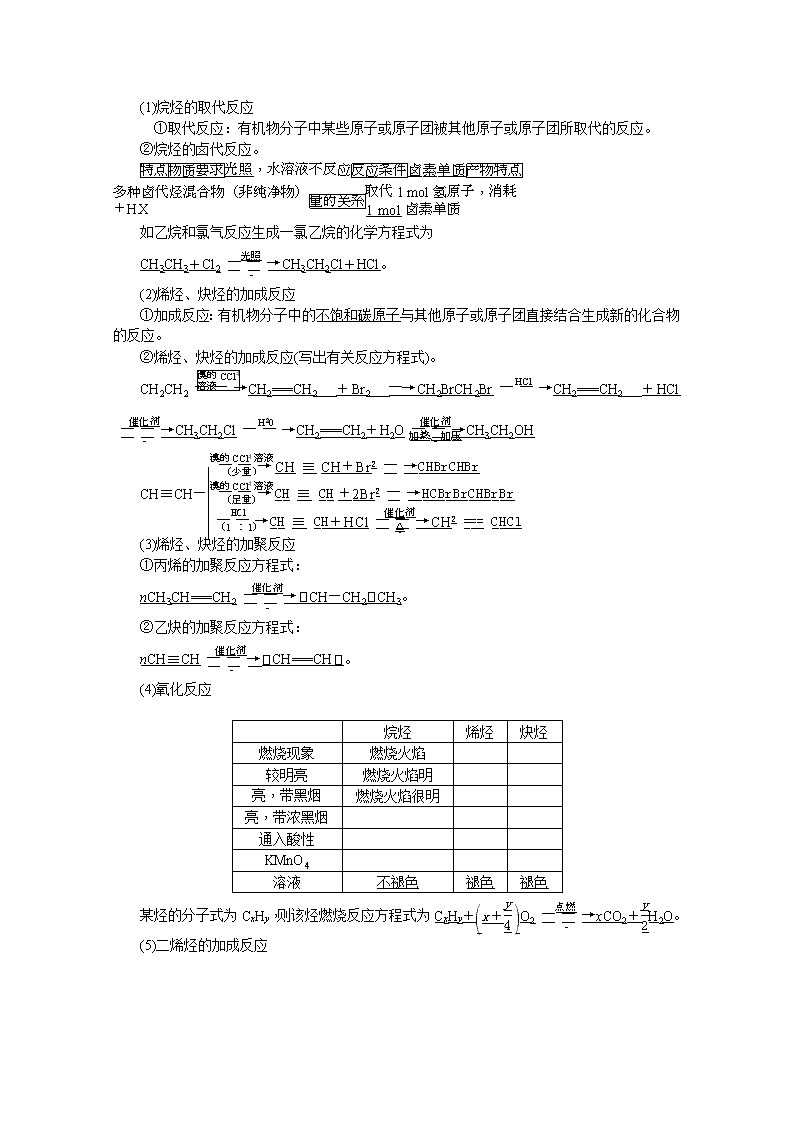
(1)烷烃的取代反应
①取代反应:有机物分子中某些原子或原子团被其他原子或原子团所取代的反应。
②烷烃的卤代反应。
如乙烷和氯气反应生成一氯乙烷的化学方程式为
CH3CH3+Cl2CH3CH2Cl+HCl。
(2)烯烃、炔烃的加成反应
①加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
②烯烃、炔烃的加成反应(写出有关反应方程式)。
CH2CH2CH2===CH2+Br2―→CH2BrCH2BrCH2===CH2+HClCH3CH2ClCH2===CH2+H2OCH3CH2OH
CH≡CH—
(3)烯烃、炔烃的加聚反应
①丙烯的加聚反应方程式:
nCH3CH===CH2CH—CH2CH3。
②乙炔的加聚反应方程式:
nCH≡CHCH===CH。
(4)氧化反应
烷烃
烯烃
炔烃
燃烧现象
燃烧火焰
较明亮
燃烧火焰明
亮,带黑烟
燃烧火焰很明
亮,带浓黑烟
通入酸性
KMnO4
溶液
不褪色
褪色
褪色
某烃的分子式为CxHy,则该烃燃烧反应方程式为CxHy+O2xCO2+H2O。
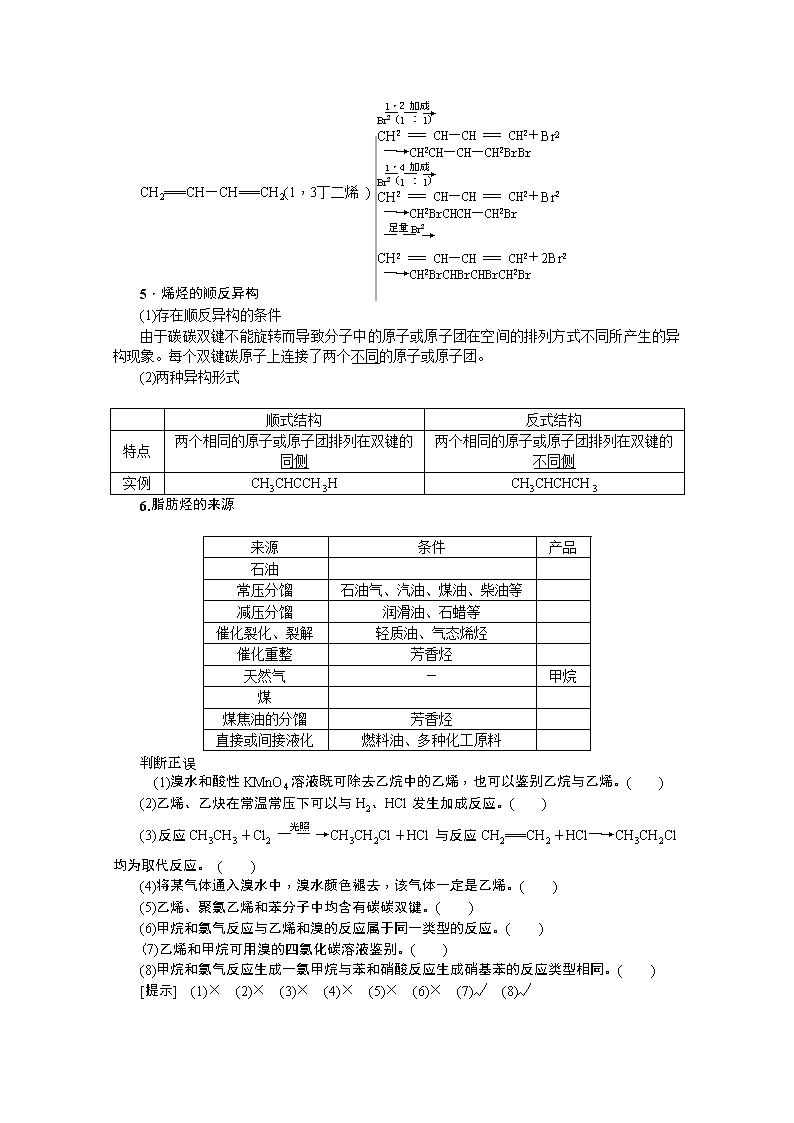
(5)二烯烃的加成反应
CH2===CH—CH===CH2(1,3丁二烯)
5.烯烃的顺反异构
(1)存在顺反异构的条件
由于碳碳双键不能旋转而导致分子中的原子或原子团在空间的排列方式不同所产生的异构现象。每个双键碳原子上连接了两个不同的原子或原子团。
(2)两种异构形式
顺式结构
反式结构
特点
两个相同的原子或原子团排列在双键的同侧
两个相同的原子或原子团排列在双键的不同侧
实例
CH3CHCCH3H
CH3CHCHCH3
6.脂肪烃的来源
来源
条件
产品
石油
常压分馏
石油气、汽油、煤油、柴油等
减压分馏
润滑油、石蜡等
催化裂化、裂解
轻质油、气态烯烃
催化重整
芳香烃
天然气
-
甲烷
煤
煤焦油的分馏
芳香烃
直接或间接液化
燃料油、多种化工原料
(1)溴水和酸性KMnO4溶液既可除去乙烷中的乙烯,也可以鉴别乙烷与乙烯。( )
(2)乙烯、乙炔在常温常压下可以与H2、HCl发生加成反应。( )
(3)反应CH3CH3+Cl2CH3CH2Cl+HCl与反应CH2===CH2+HCl―→CH3CH2Cl均为取代反应。 ( )
(4)将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯。( )
(5)乙烯、聚氯乙烯和苯分子中均含有碳碳双键。( )
(6)甲烷和氯气反应与乙烯和溴的反应属于同一类型的反应。( )
(7)乙烯和甲烷可用溴的四氯化碳溶液鉴别。( )
(8)甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同。( )
[提示] (1)× (2)× (3)× (4)× (5)× (6)× (7)√ (8)√
角度1 脂肪烃的组成、结构与性质
1.(2019·衡水模拟)下列分析中正确的是( )
A.烷烃在任何情况下均不与强酸、强碱、氧化剂反应
B.正丁烷分子中四个碳原子可能在同一直线上
C.常温常压下CH3—CH—CH—CH3CH3CH3是气态
D.含有碳元素的化合物不一定是烃
D [烷烃通常情况下均不与强酸、强碱、氧化剂反应,但点燃条件下可以燃烧,发生氧化反应,A错误;正丁烷分子中四个碳原子呈锯齿状排列不可能在同一直线上,B错误;CH3—CH—CH—CH3CH3CH3分子式是C6H14,常温常压下是液态,C错误;烃是指仅含碳、氢两种元素的化合物,所以含有碳元素的化合物不一定是烃,D正确。]
2.(2018·盐城模拟)盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去)。下列关于盆烯的说法中错误的是( )
A.盆烯是苯的一种同分异构体
B.盆烯分子中所有的碳原子不可能在同一平面上
C.盆烯是乙烯的一种同系物
D.盆烯在一定条件下可以发生加成反应
C [盆烯、苯的分子式均为C6H6,但结构不同,两者属于同分异构体,A正确;分子中含有的4个饱和碳原子,不能共面,所以盆烯分子中所有的碳原子不可能在同一平面上,B正确;盆烯含有一个碳碳双键且含有环,乙烯只含一个碳碳双键,两者的结构不相似,两者不是同系物,C错误;盆烯中含有碳碳双键可以发生加成反应,D正确。]
3.科学家最近在-100 ℃的低温下合成一种烃X,此分子的球棍模型如图所示(图中的连线表示化学键),下列说法正确的是 ( )
A.X能使溴的四氯化碳溶液褪色
B.X是一种在常温下能稳定存在的液态烃C.X分子中在同一平面上的碳原子最多5个
D.充分燃烧等质量的X和甲烷,X消耗氧气多
A [根据球棍模型书写其结构简式:CCHCHCHCH,其分子式为C5H4。由于分子内含有CC,该烃可与Br2发生加成反应,且分子中最多5个原子共面,3个C原子共面,A正确,C错误;根据题述知该烃在-100 ℃下存在,B错误;等质量的烃燃烧时,含氢量越高,消耗O2的量越多,该烃的含氢量小于CH4的含氢量,D错误。]
结构决定性质
不同的碳碳键对有机物的性质有着不同的影响:
(1)碳碳单键有稳定的化学性质,典型反应是取代反应;
(2)碳碳双键中有一个化学键易断裂,典型反应是氧化反应、加成反应和加聚反应;
(3)碳碳三键中有两个化学键易断裂,典型反应是氧化反应、加成反应和加聚反应;
(4)苯的同系物支链易被酸性高锰酸钾溶液氧化,是因为苯环对取代基的影响。而苯不能被酸性高锰酸钾溶液氧化。
角度2 脂肪烃的反应类型
4.根据下列流程图提供的信息,判断下列说法中错误的是( )
、
A.属于取代反应的有①、④
B.反应②、③均是加成反应
C.B的结构简式为CH2BrCHClCH2Br
D.A还有三种同分异构体
C [丙烯(C3H6)经反应①、②生成C3H5Br2Cl,增加了一个氯原子,两个溴原子,少了一个氢原子,可推出反应①是取代反应(氯原子取代饱和碳原子上的氢原子),反应②是加成反应,所得产物为CH2BrCHBrCH2Cl,C项说法错误;由反应③的产物可知反应③是加成反应,由C2H5—O—SO3H与H2O反应生成C2H5OH和H2SO4知,反应④是取代反应,A、B项说法均正确;A是CH2===CHCH2Cl,它的链状同分异构体还有两种,环状同分异构体有一种,D项说法正确。] 芳香烃
(对应复习讲义第143页)
1.苯及苯的同系物的组成、结构与性质
苯
苯的同系物
分
子
式
C6H6
CnH2n-6(通式,n>6)
结构特点
①苯环上的碳碳键是介于碳碳单键和碳碳双键之间的一种独特的化学键
②分子中所有原子一定(填“一定”或“不一定”,右同)在同一平面内
①分子中含有一个苯环;与苯环相连的是烷烃基
②与苯环直接相连的原子在苯环平面内,其他原子不一定在同一平面内
主要化学性质
(1)取代:
①硝化:
+HNO3
NO2+H2O
②卤代:+Br2Br+HBr
(2)加成:+3H2
(3)可燃烧,难氧化,不能使酸性KMnO4溶液褪色
(1)取代:
①硝化:CH3+3HNO3
NO2O2NCH3NO2+3H2O
②卤代:
CH3+Br2
CH3Br+HBr
CH3+Cl2
CH2Cl+HCl
(2)加成
(3)可燃烧,易氧化,能使酸性KMnO4溶液褪色,
C2H5COOH
2.苯环与取代基的相互影响
(1)侧链对苯环的影响
①苯的同系物比苯更易发生苯环上的取代反应,苯主要发生一元取代,而苯的同系物能发生邻、对位取代,如苯与浓硝酸、浓硫酸混合加热主要生成硝基苯,甲苯与浓硫酸、浓硝酸在一定条件下生成2,4,6三硝基甲苯(TNT)。
②苯的同系物发生卤代反应时,在光照和催化剂的不同条件下,卤素原子取代氢原子的位置不同。
如CH3+Cl2CH2Cl+HCl,CH3+Cl2CH3Cl+HCl。
(2)苯环对侧链的影响
烷烃不易被氧化,但苯环上的烷基易被氧化。苯的同系物能使酸性KMnO4溶液褪色,而苯不能,用此法可鉴别苯和苯的同系物。
3.苯的同系物的同分异构体
(1)C8H10
名称
乙苯
邻二甲苯
间二甲苯
对二
甲苯
结构简式
CH2CH3
CH3CH3
CH3CH3
CH3CH3
一氯
代物
种数
烃基
2
1
1
1
苯环
3
2
3
1
总和
5
3
4
2
续表
名称
乙苯
邻二甲苯
间二甲苯
对二
甲苯
氢原
子类
型及
比值
类型
5
3
4
2
比值
3∶2∶2∶2∶1
3∶1∶1
1∶6∶2∶1
3∶2
(2)C9H12
①丙苯类:CH2CH2CH3、HCCH3CH3;
②甲乙苯类:CH2CH3CH3、CH2CH3CH3、CH2CH3CH3;
③三甲苯类:CH3CH3CH3、CH3CH3CH3、H3CCH3CH3。
4.其他芳香烃——苯乙烯(CHCH2)、萘()、蒽()等。
(1)苯环是平面正六边形结构,说明苯分子中的碳碳键不是单双键交替连接结构。( )
(2)苯的邻二取代物不存在同分异构体。( )
(3)苯分子是环状结构,只有6个碳原子在同一平面上。( )
(4)苯与溴水充分振荡后,溴水褪色说明苯分子中的碳原子没有饱和。( )
(5)乙烯和甲苯都能使酸性KMnO4溶液褪色,说明二者分子中都含有碳碳双键。( )
[提示] (1)√ (2)√ (3)× (4)× (5)×
角度1 芳香烃的性质及应用
【例1】 (2018·赣州模拟)以苯为原料合成F,转化关系如下:
CH(CH3)2BCDEF①
F是一种具有重要工业价值的芳香化合物,含有C、H、O、N四种元素,其蒸气密度是相同状况下氢气密度的74.5倍,分子中有两个互为对位的取代基②。C能与碳酸氢钠溶液反应,试剂②为Fe/HCl。
已知:①RCOOH;
②NO2NH2(苯胺:弱碱性,易被氧化);
③RCOClRCOR′。③
请回答下列问题:
(1)反应①为加成反应④,写出A的分子式:________。
(2)B中所含官能团的名称为________;生成B时,常伴有副反应发生,反应所得产物除B外可能还含有________(写出一种产物的结构简式)。
(3)试剂①是________;试剂①和试剂②的顺序能否互换:________(填“能”或“不能”);为什么?________________________________________________________________________
________________________________________________________________________。
(4)E生成F的化学方程式为________________________________________________________________________
________________________________________________________________________。
[思路点拨] ①注意转化的特征反应条件,根据反应条件推导物质转化关系;
②F的相对分子质量为74.5×2=149,分子中有两个取代基;
③认真读懂已知信息,并正确迁移至转化关系中,并推出相应物质;
④―→CH(CH3)2为加成反应,则支链由CH2===CHCH3加成得到。
[解析] 已知合成流程中,苯与A发生加成反应[题(1)提示],通过反应①生成异丙基苯,因此反应物A是一种烯烃,结合产物可知A为CH2===CHCH3。CH(CH3)2在第二步发生硝化反应,由于最终的F分子中有两个互为对位的取代基,所以该硝化反应只在对位取代,即B为O2NCH(CH3)2。C能与NaHCO3溶液反应,所以C分子中含有—COOH,结合已知①,B→C是O2NCH(CH3)2被酸性KMnO4溶液氧化生成O2NCOOH(过程)。根据已知③,E→F为RCOCl与CH3CH2MgCl的取代反应,生成RCOCH2CH3,D →E是通过已知反应②将—NO2还原成—NH2,试剂②是Fe/HCl,C→D为—COOH转变成—COCl的取代反应,则D为O2NCOCl,E为H2NCOCl,F是H2NCCH2CH3O,相对分子质量恰好为149。
(2)B是O2NCH(CH3)2,官能团是—NO2(硝基)。由于—CH(CH3)2对苯环的活化作用,所以苯环上—CH(CH3)2的邻、对位都可能发生取代,所以产物包括仅取代邻位、对位的1个位置,各1种,取代邻位、对位的两个位置,共2种,取代邻位、对位的3个位置,有1种,一共是5种,除去B本身,还可能有4种产物。
(3)试剂①是将—CH(CH3)2氧化生成—COOH,应当选择酸性高锰酸钾溶液。由于苯胺容易被氧化,所以必须先氧化—CH(CH3)2,然后再通过还原反应将
—NO2转变成—NH2,以防止得到的—NH2被酸性高锰酸钾氧化。
(4)E(H2NCOCl)与CH3CH2MgCl反应生成F(H2NCCH2CH3O),另一产物为MgCl2。
[答案] (1)C3H6 (2)硝基 O2NCH(CH3)2NO2、NO2O2NCH(CH3)2NO2、CH(CH3)2NO2、NO2CH(CH3)2NO2(任写一种)
(3)KMnO4(H+) 不能 如果先还原后氧化,则还原生成的氨基又会被氧化
(4)H2NCClO+CH3CH2MgCl
H2NCCH2CH3O+MgCl2
苯的同系物被强氧化剂氧化
苯的同系物(与苯环相连的碳原子上有氢原子)能被酸性KMnO4溶液等强氧化剂氧化而使溶液褪色。
[对点训练]
1.(2019·怀化模拟)下图为有关甲苯的转化关系图:
以下说法中正确的是( )
A.反应①为取代反应,反应③为加成反应
B.反应②的现象是火焰明亮并带有浓烟
C.反应④的产物所有原子在同一平面上
D.反应④中1 mol甲苯最多与3 mol H2发生加成反应,是因为甲苯分子中含有三个碳碳双键
B [A项,①、③均为取代反应;B项,分子中含碳量高,燃烧火焰明亮并带有浓烟;C项,—CH3中四原子不会共面;D项,苯环中不含碳碳双键或单键。]
2.(2019·厦门模拟)已知(异丙烯苯)(异丙苯),下列说法错误的是( )
A.该反应属于加成反应
B.异丙苯的一氯代物共有6种
C.可用溴水鉴别异丙烯苯和异丙苯
D.异丙苯是苯的同系物
B [(异丙烯苯)(异丙苯)是碳碳双键与氢气加成,发生的是加成反应,故A正确;异丙苯分子中含5种氢原子,一氯代物共有5种,故B错误;异丙烯苯中含碳碳双键,溴水中的溴单质可和碳碳双键发生加成反应,溴水褪色,异丙苯和溴水发生萃取分层,可用溴水鉴别异丙烯苯和异丙苯,故C正确;异丙苯只含一个苯环,与苯组成上相差3个CH2原子团,是苯的同系物,故D正确。]
角度2 有机物分子中原子的共面、共线判断
1.熟练掌握四种典型结构
(1)甲烷型:正四面体结构,碳原子与四个原子形成四个共价键时,立体构型都是正四面体结构,五个原子中最多有三个原子共平面。
(2)乙烯型:平面结构,位于乙烯型结构上的六个原子一定共平面。
(3)乙炔型:直线形结构,位于乙炔型结构上的四个原子一定在一条直线上,也一定共平面。
(4)苯型:平面六边形结构,位于苯环上的十二个原子一定共平面。
2.注意键的旋转
(1)在分子中,形成单键的原子可以绕键轴旋转,而形成双键、三键等其他键的原子不能绕轴旋转。
(2)若平面间靠单键相连,所连平面可以绕轴旋转,可能旋转到同一平面上,也可能旋转后不在同一平面上。
(3)若平面间被多个点固定,则不能旋转,一定共平面。如分子中所有环一定共面。
3.恰当地拆分复杂分子
观察复杂分子的结构,先找出类似于甲烷、乙烯、乙炔和苯分子的结构,再将对应的立体构型及键的旋转等知识进行迁移即可解决有关原子共面、共线的问题。
特别要注意的是,苯分子中处于对位的两个碳原子以及它们所连的两个氢原子,这四个原子是在一条直线上的。
【例2】 (2019·长春模拟)有关
CHCHF2—CHCC—CH3①分子结构的下列叙述中正确的是( )
①除苯环外的其余碳原子②有可能③都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上
A.①② B.②③
C.①③ D.②④
[思路点拨] ①该分子可以看作由—CH3、CC、和—C≡C—为主干组合而成,明确四种典型结构;
②看清楚是碳原子还是所有原子;
③审清题目要求,如“可能”“一定”“最少”“最多”等关键词。
D [乙烯是平面结构,不是直线结构,除苯环外的其余碳原子不可能都在一条直线上,故①错误,②正确;CHCHF2—CHCC—CH3分子中,甲基中C原子与—C≡C—共直线,—CHF2中C原子与CC共面,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线形结构,所以12个C原子可能都在同一平面上,故③错误,④正确。]
快速判断有机物分子中共线、共面问题。
(1)只要含有—CH3,所有原子不可能共平面;
(2)只要含有CC,所有原子不可能共直线;
(3)2134中四个原子一定在一条直线上。
[对点训练]
1.某烃的结构简式为CC2H5CH3—CH2—CHCCH,分子中含有四面体结构的碳原子数为a,一定在同一直线上的碳原子数为b,一定在同一平面内的碳原子数为c,则a、b、c分别可能为 ( )
A.4、3、5 B.4、3、6
C.2、5、4 D.4、6、4
B [该有机物结构为C3C7H2—C8H3C6H3—C5H2—C4HC2C1H。
若碳原子同时连有4个其他原子或基团,则该碳原子就是具有四面体结构的碳原子,这样的碳原子共有4个,分别是5、6、7、8号;由乙炔结构可知,1、2、3号碳原子在同一条直线上,共3个;3、4号碳原子也在同一直线上,共2个;由乙烯结构可知,2、3、4、5、7号碳原子一定在同一平面内,再结合1、2、3号碳原子在同一直线上,得1、2、3、4、5、7号碳原子一定在同一平面内,共6个。]
2.已知碳碳单键可以绕键轴自由旋转。某烃的结构简式如图所示,下列关于该烃的说法中正确的是( )
CHCCH3CH3CH3
A.分子中处于同一直线上的碳原子最多有6个
B.分子中至少有12个碳原子处于同一平面上
C.该烃苯环上的一氯代物共有3种
D.该烃苯环上的一氯代物共有5种
B [甲基与苯环平面结构通过单键相连,甲基的碳原子处于苯环这个平面上;两个苯环相连,与苯环相连的碳原子也处于另一个苯环平面上,C1HCCH334CH3C6H35中的1、2、3、4、5、6号碳原子及与1号碳原子相连的碳碳三键上的碳原子总共7个碳原子处于一条直线上,且至少有12个碳原子共面,故A错误,B正确;该有机物分子中,苯环上所有氢原子所处化学环境都不相同,所以苯环上总共有6种氢原子,故其苯环上一氯代物有6种,故C、D错误。]
卤代烃的性质及应用
(对应复习讲义第145页)
1.定义
烃分子里的氢原子被卤素原子取代后生成的产物。官能团为—X,饱和一元卤代烃的通式为CnH2n+1X。
2.物理性质
3.化学性质
(1)水解反应
①反应条件为强碱(如NaOH)的水溶液,加热。
②CH3CH2CH2Br在碱性条件(NaOH水溶液)下水解的化学方程式为CH3CH2CH2Br+NaOHCH3CH2CH2OH+NaBr。
(2)消去反应
①消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HBr等),从而生成含不饱和键(如CC)化合物的反应。
②反应条件为强碱(如NaOH)的醇溶液,加热。
③1溴丙烷(NaOH的乙醇溶液)发生消去反应的化学方程式为CH3CH2CH2Br+NaOHCH3CH===CH2↑+NaBr+H2O。
4.卤代烃对环境、健康产生的影响
含氯、氟的卤代烷是造成臭氧层空洞的主要原因。
5.卤代烃的获取方法
(1)取代反应(写出反应的化学方程式)
甲烷与氯气反应生成一氯甲烷:CH4+Cl2CH3Cl+HCl;
苯与溴的取代反应:
+Br2Br+HBr;
乙醇与HBr反应:CH3CH2OH+HBrCH3CH2Br+H2O。
(2)不饱和烃的加成反应
丙烯与溴的加成反应:CH3CH===CH2+Br2―→CH3CHBrCH2Br;
乙炔与HCl反应制备氯乙烯:CH≡CH+HClCH2ClHOOCClHOOCCOONaNaOOC富马酸富血铁
————————————————————①
回答下列问题:
(1)A的化学名称为________,由A生成B的反应类型为________。
(2)C的结构简式为 ________。
(3)富马酸的结构简式为________。
(4)检验富血铁中是否含有Fe3+的实验操作步骤是________________________________________________________________________
________________________________________________________________________。
(5)富马酸为二元羧酸,1 mol富马酸与足量饱和NaHCO3溶液反应可放出______L CO2(标准状况);富马酸的同分异构体中,同为二元羧酸的还有②____________(写出结构简式)。
[思路点拨] ①关注转化关系中的特征反应条件,如“Cl2、光照”发生取代反应,“NaOH、乙醇、△”为卤代烃的消去反应;“O2/N2O5+H2O”把双键氧化生成—COOH等;
②限定条件,分子中必含两个“—COOH”。
[解析] (1)由结构简式可知A的名称为环己烷。由环己烯逆向分析,可知B为环己烷的一氯取代物。
(2)环己烯与溴的四氯化碳溶液发生加成反应生成C(结构简式为BrBr)。
(3)丁二烯酸钠酸化得富马酸,其结构简式为COOHHOOC。
(4)检验富血铁中是否含有Fe3+的实验操作步骤是取少量富血铁,加入稀硫酸溶解,再滴加KSCN溶液,若溶液显红色,则产品中含有Fe3+;反之,则无。
(5)富马酸为二元羧酸,1 mol富马酸与足量饱和NaHCO3溶液反应生成2 mol CO2,标准状况下的体积为44.8 L。富马酸的同分异构体中,同为二元羧酸的还有COOHCOOH、COOHCOOH。
[答案] (1)环己烷 取代反应 (2)BrBr
(3)COOHHOOC
(4)取少量富血铁,加入稀硫酸溶解,再滴加KSCN溶液,若溶液显红色,则产品中含有Fe3+;反之,则无 (5)44.8 COOHCOOH、COOHCOOH
卤代烃在有机合成中的四大应用
(1)连接烃和烃的衍生物的桥梁
烃通过与卤素单质发生取代反应或加成反应转化为卤代烃,卤代烃在碱性条件下可水解转化为醇或酚,进一步可转化为醛、酮、羧酸和酯等;醇在加热条件下与氢卤酸反应转化为卤代烃,卤代烃通过消去反应可转化为烯烃或炔烃。
如:CH3CH2ClCH2OH―→醛和羧酸。
(2)改变官能团的个数
如:CH3CH2BrCH2===CH2CH2BrCH2Br。
(3)改变官能团的位置
如:CH2BrCH2CH2CH3CH2===CHCH2CH3CH3CHCH2CH3Br。
(4)对官能团进行保护
如在氧化CH2===CHCH2OH的羟基时,碳碳双键易被氧化,常采用下列方法保护:
CH2===CHCH2OHCH3CHCH2OHBr
CH3CHCOOHBrCH2===CH—COOH。
[对点训练]
1.(2019·哈尔滨模拟)以溴乙烷为原料制备乙二醇,下列方案合理的是( )
A.CH3CH2BrCH3CH2OH
CH2===CH2CH2BrCH2Br乙二醇
B.CH3CH2BrCH2BrCH2Br乙二醇
C.CH3CH2BrCH2===CH2
CH3CH2BrCH2BrCH2Br乙二醇
D.CH3CH2BrCH2===CH2
CH2BrCH2Br乙二醇
A [以溴乙烷为原料制备乙二醇的步骤为:CH3CH2Br在氢氧化钠水溶液、加热条件下发生取代反应生成CH3CH2OH,CH3CH2OH在浓硫酸、加热条件下发生消去反应生成CH2===CH2,乙烯与溴发生加成反应生成CH2BrCH2Br,CH2BrCH2Br在氢氧化钠水溶液、加热条件下发生水解反应生成乙二醇,故A正确;溴乙烷与溴单质发生取代反应产物不唯一,故B错误;CH3CH2Br在氢氧化钠醇溶液、加热条件下发生消去反应生成乙烯,乙烯与溴化氢生成溴乙烷,该步骤为重复步骤,且溴乙烷与溴单质发生取代反应产物不唯一,故C错误;CH3CH2Br在氢氧化钠醇溶液、加热条件下发生消去反应生成乙烯,乙烯与溴化氢发生加成反应生成溴乙烷,不生成CH2BrCH2Br,故D错误。]
2.某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为________________________________________________________________________;
(2)A中的碳原子是否都处于同一平面?________(填“是”或“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
反应②的化学方程式为________________________________________________________________________
________________________________________________________________________;
C的化学名称是________;E2的结构简式是________________;④、⑥的反应类型依次是________、
________。
[解析] (1)用商余法先求该烃的分子式,n(CH2)=84/14=6,分子式为C6H12,分子中含有一个碳碳双键,又只有一种类型的氢原子,说明分子结构很对称,结构简式为CH3CH3CC—CH3CH3。(2)由于存在碳碳双键,因此分子中所有碳原子共平面。(3)A和Cl2
发生加成反应,产物再经反应②得共轭二烯烃C(CCH3H2CCCH3CH2),D1是C和Br2发生1,2加成反应的产物,而D1和D2互为同分异构体,可知D2是C和Br2发生1,4加成的产物,生成物D1和D2分别再发生水解反应生成醇E1和E2。
[答案] (1)CH3CH3CC—CH3CH3 (2)是
(3)CCH3ClH3CCCH3ClCH3+2NaOH
CCH3H2CCCH3CH2+2NaCl+2H2O
2,3二甲基1,3丁二烯
HOH2CCCH3C—CH2OHCH3 1,4加成反应 取代反应(或水解反应)
相关文档
- 2021届高考化学一轮复习化学反应速2021-07-098页
- 2020届高考化学一轮复习化学键 分2021-07-0915页
- 2019届高考化学一轮复习化学反应中2021-07-0914页
- 2021届高考化学一轮复习化学平衡状2021-07-098页
- 2020届高考化学一轮复习化学反应与2021-07-0911页
- 2021届高考化学一轮复习化学反应速2021-07-099页
- 2020届高考化学一轮复习化学反应速2021-07-0913页
- 2020届高考化学一轮复习化学反应速2021-07-094页
- 2021届高考化学一轮复习化学平衡常2021-07-0916页
- 2020届高考化学一轮复习化学平衡状2021-07-099页