- 518.50 KB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
湖南省郴州市2019-2020学年高一4月线上考试试题
注意事项:
1.本试卷分试题卷和答题卡。试题卷共6页,有四道大题,共23道小题,满分100分。考试时间60分钟。
2.答卷前,考生务必将自己的姓名、准考证号、考场号和座位号填写在试题卷和答题卡上。将条形码横贴在答题卡左上角“条形码粘贴处”。
3.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案。信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案。答案不能答在试题卷上。
4.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液。不按以上要求作答无效。
5.考生必须保证答题卡的整洁。考试结束后,请将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 O-16 C-12 S-32 Na-23 Cu-64 Ba-137
一、选择题(每小题3分,共计54分,每小题只有一个选项符合题意)
1.化学与生活生产、可持续发展密切相关。下列说法中正确的是( )
A.14C可用于文物年代的鉴定,14C和12C互为同素异形体
B.为了消除碘缺乏病,在食用盐中加入一定量的碘单质
C.高纯度的SiO2可以制成光电池,将光能直接转化为电能,
D.Fe2O3是一种红棕色粉末,常用作红色油漆和涂料
2.19世纪中叶,俄国化学家门捷列夫的突出贡献是( )
A.提出原子学说 B.制出第一张元素周期表
C.提出分子学说 D.发现氧气
3.用NaOH固体配制250 mL 1.00 mol/L NaOH溶液时,不必用到的仪器是( )
A.试管 B.玻璃棒
C.胶头滴管 D.容量瓶
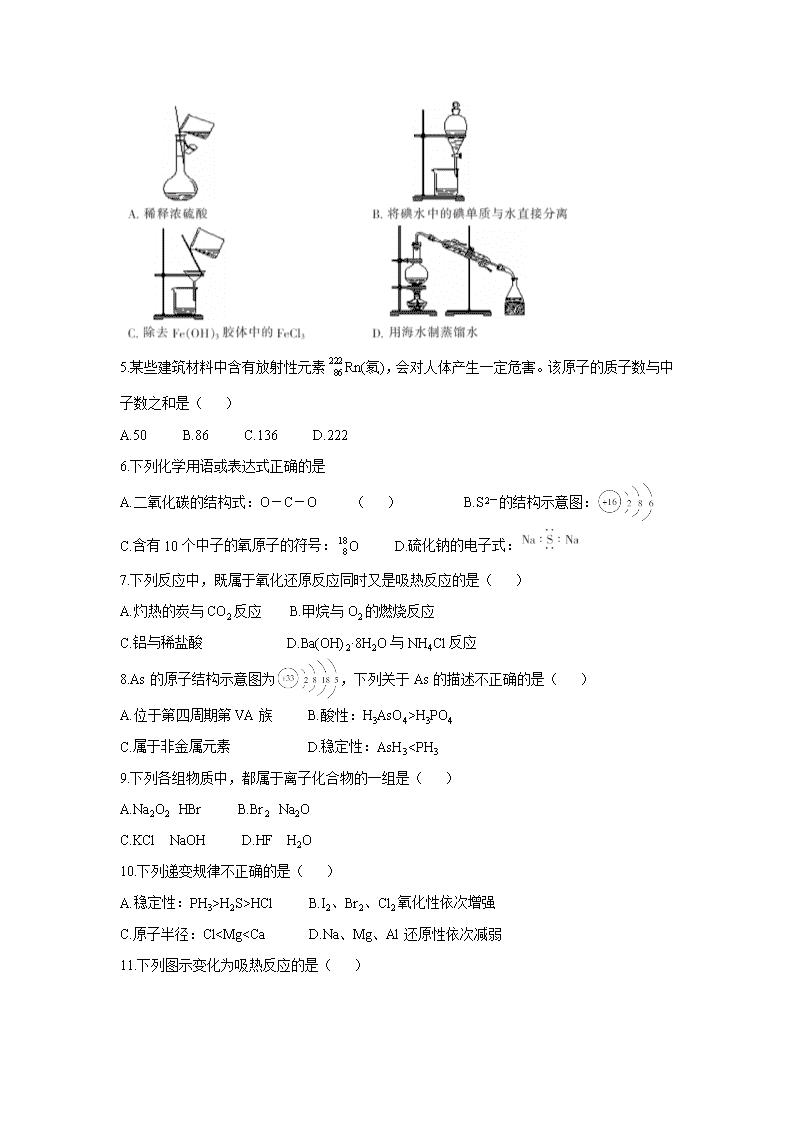
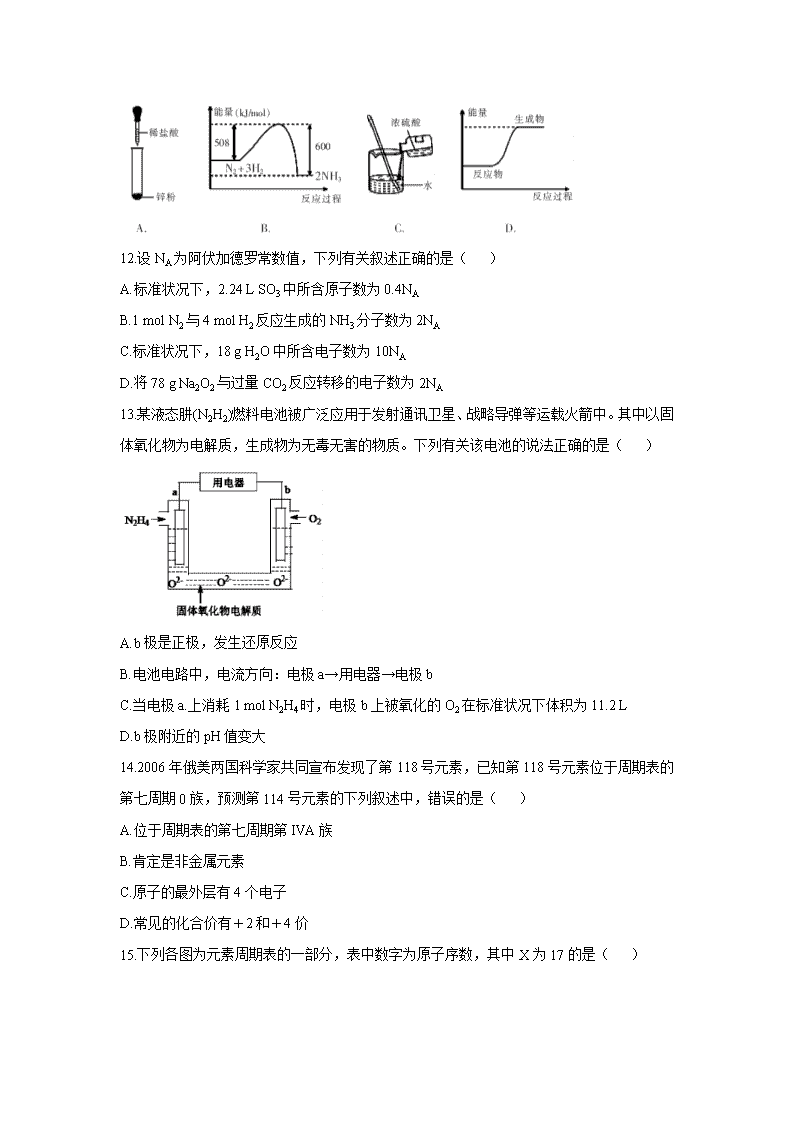
4.下列实验装置与实验目的对应的是( )
5.某些建筑材料中含有放射性元素Rn(氡),会对人体产生一定危害。该原子的质子数与中子数之和是( )
A.50 B.86 C.136 D.222
6.下列化学用语或表达式正确的是
A.二氧化碳的结构式:O-C-O ( ) B.S2-的结构示意图:
C.含有10个中子的氧原子的符号:O D.硫化钠的电子式:
7.下列反应中,既属于氧化还原反应同时又是吸热反应的是( )
A.灼热的炭与CO2反应 B.甲烷与O2的燃烧反应
C.铝与稀盐酸 D.Ba(OH)2·8H2O与NH4Cl反应
8.As的原子结构示意图为,下列关于As的描述不正确的是( )
A.位于第四周期第VA族 B.酸性:H3AsO4>H3PO4
C.属于非金属元素 D.稳定性:AsH3H2S>HCl B.I2、Br2、Cl2氧化性依次增强
C.原子半径:Cl”、“<”或“=”)。
③请写出图中构成原电池的正极电极反应式: 。
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1
(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为 。
三、实验题(共12分)
22.(12分)硫及其化合物是重要的工业原料,探究其性质具有非常重要的意义。
(1)某学习小组设计用如图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“II”或“III”);试管b中发生反应的离子方程式为 。
(2)利用下图装置可以验证硫和氯非金属性的强弱。
①仪器A的名称为 ,干燥管D的作用是 。
②实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为 、 、 ;装置C中的实验现象为有淡黄色沉淀生成,离子方程式为 。
四、计算题(共4分)
23.将64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为22.4 L。请计算(写出计算过程):
(1)NO标况下的体积;
(2)参加反应的HNO3的物质的量。
【参考答案】