- 1.58 MB
- 2021-08-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第三节 乙醇与乙酸
学习目标
1.
了解乙酸的组成、结构、物理性质和主要应用。
2.
掌握乙酸的主要化学性质。
3.
了解乙酸与人类生活和健康的知识,体会学习有机化学的意义,提高科学素养和生活质量。
第
2
课时 乙酸
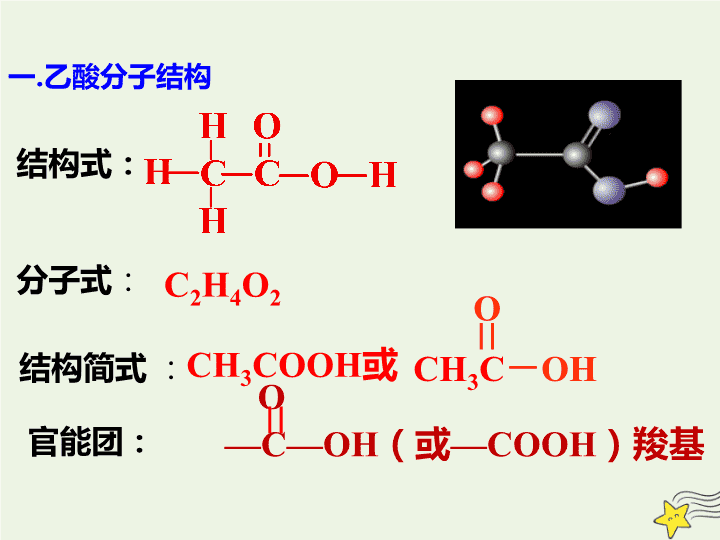
一
.
乙酸分子结构
分子式
:
C
2
H
4
O
2
结构式:
结构简式
:
CH
3
COOH
或
O
CH
3
C
-
OH
官能团:
—C—OH
(或
—COOH
)羧基
O
颜色
:
无色
气味
:
有强烈刺激性气味
挥发性:
易挥发(沸点
: 117.9℃
)
低
(16.6℃)
(
无水乙酸又称为
:
冰醋酸
)
溶解性:
易溶于水、
乙醇等溶剂
二
.
乙酸的物理性质
状态
:
液体
熔点:
请利用下列药品设计实验方案来证明乙酸具有酸性?
新制
Cu(OH)
2
悬浊液、乙酸溶液、石蕊试液、碳酸钠粉末
实验步骤
现象
1
石蕊溶液中加入乙酸
2
新制
的
Cu(OH)
2
悬浊液再加入少量的乙酸溶液
3
碳酸钠粉末
中加入乙酸
溶液变红
Cu(OH)
2
溶解,生成蓝色溶液
碳酸钠粉末溶解
有气泡产生
实验探究一:乙酸具有酸性吗?
结论:乙酸具有
酸性
(
1
)酸的通性
①
使酸碱指示剂变色
②
与碱反应
④
与活泼金属反应
⑤
与碱性氧化物反应
③
与部分盐反应
三
.
乙酸的化学性质
CH
3
COOH CH
3
COO
-
+
H
+
如何除水垢?
水垢主要成份:
CaCO
3
离子方程式:
2CH
3
COOH+CaCO
3
=Ca
2+
+2CH
3
COO
—
+H
2
O
+CO
2
↑
实验探究二:乙酸乙酯的制取
乙醇
浓硫酸
乙酸
饱和
碳酸钠
溶液
步骤:
在大试管里加入
3mL
乙醇
,
然后
边振荡
试管边慢慢
加入
2mL
浓硫酸
和
2mL
冰醋酸
;
在另一支试管中加入
饱和
Na
2
CO
3
溶液
;
按照图所示连接好装置
,
加热观察现象
。
(
1
)导管口为什么要在溶液的液面上方?
乙醇
浓硫酸
乙酸
饱和
碳酸钠
溶液
(
2
)药品的添加顺序如何?
防止倒吸
先加乙醇再加浓
H
2
SO
4
最后加乙酸
思考
乙酸乙酯
现象
:溶液分层,上层有无色透明的油状液体产生
,
并有香味。
O O
CH
3
—
C
—
OH+H
—
O
—
C
2
H
5
CH
3
—
C
—
O
—
C
2
H
5
+ H
2
O
浓
H
2
SO
4
酸脱羟基、醇脱氢
(
羟基上的
)
取代反应
实质:
反应类型:
(
2
)酯化反应
定义:
酸和醇
反应生成
酯和水
的反应叫做酯化反应。
O O
CH
3
—
C
—
OH+H
—
O
—
C
2
H
5
CH
3
—
C
—
O
—
C
2
H
5
+ H
2
O
浓
H
2
SO
4
CH
3
COOCH
3
+ H
2
O
CH
3
COOH + HOCH
3
浓
H
2
SO
4
乙酸甲酯
试一试:请同学们试着写出乙酸和甲醇反应的化学方程式。
练习
下列物质中,能与醋酸发生反应的是( )
①乙醇 ②金属铝 ③甲烷
④碳酸钙 ⑤氢氧化钠⑥ 氧化镁
A.①③④⑤⑥ B.②③④⑤
C. ①②④⑤⑥ D.
全部
C
O
CH
3
—C—O—H
课堂小结
一
.
乙酸分子结构
二
.
乙酸的物理性质
三
.
乙酸的化学性质
(
1
)酸的通性
CH
3
COOH
CH
3
COO
-
+ H
+
(
2
)酯化反应
CH
3
COOH + HOC
2
H
5
CH
3
COOC
2
H
5
+H
2
O
浓
H
2
SO
4
△
酸性
酯化反应
相关文档
- 高中化学第七章有机化合物第二节第2021-08-0647页
- 2020高中化学 研究有机化合物的一2021-08-065页
- 2019高中化学 第一章 认识有机化合2021-08-064页
- 高中化学《有机化学基础》1_4研究2021-08-0611页
- 高中化学课件必修二《第三章 第一2021-08-0635页
- 有机化合物的分类教案(1)2021-08-063页
- 高中化学 第三章 有机化合物单元检2021-08-067页
- 2020高中化学 第三章 有机化合物 2021-08-064页
- 高中化学:人教版必修一 第三章《重2021-08-067页
- 人教版化学选修5课件:1-4-2《研究有2021-08-0619页