- 217.50 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
1
课题 2 氧气
答案:
(1)略大 (2)不易 (3 )氧化 (4)复燃 (5)二氧化碳 (6)二氧化硫 (7)四氧化三
铁 (8)化合
1.氧气的物理性质
(1)在标准状况下,氧气是无色、无味气体,密度为 1.429 g/L,比空气的密度(1.293 g/L)
略大。它不易溶于水(1 L 水能溶解 30 mL 氧气)。
气态――→101 kPa
-183 ℃
液态
淡蓝色 ――→101 kPa
-218 ℃
雪花状固体
淡蓝色
工业生产的氧气一般通过降温加压,变为液态氧气后贮存在蓝色钢瓶中。
释疑点 氧气转变为液氧发生了什么变化
氧气变为淡蓝色液体或淡蓝色雪花状固体时发生了物理变化。因为无论是哪种状态的氧
气,都属于同种物质。可见,有颜色改变的变化不一定是化学变化。
【例 1】下列关于氧气物理性质的叙述,错误的是( )
A.在标准状况下,氧气的密度比空气略大
B.氧气不溶于水
C.在通常状况下,氧气是无色、无味的气体
D.液态氧是淡蓝色液体
解析:
A √ 标准状况下氧气的密度比空气略大
B × 不易溶于水,不是不溶于水,应理解成氧气在水中溶解得不够多
C √ 通常状况下氧气是无色、无味的气体
D √ 液态氧是淡蓝色液体
答案:B
2.氧气的化学性质
氧气是一种化学性质比较活泼的气体,一定条件下,能与多种物质发生化学反应。氧气
具有氧化性和助燃性。氧气具有助燃性,但不能认为氧气可燃烧。
(1)氧气能使带火星的木条复燃
如图,将带火星的木条伸到盛有氧气的集气瓶中,观察到木条复燃,说明氧气能支持燃
烧(助燃)。
2
点技巧 验证一瓶无色气体是氧气的方法
将带有火星的木条伸入瓶中,若木条复燃,证明该气体是氧气。
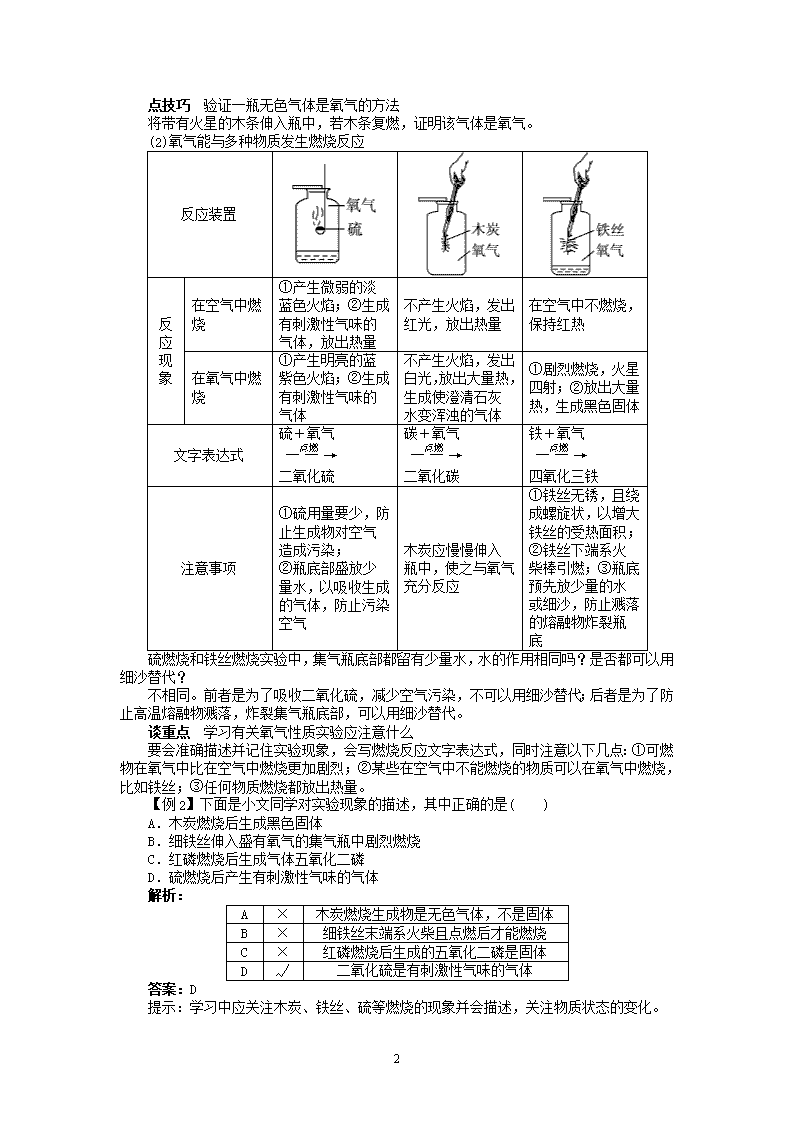
(2)氧气能与多种物质发生燃烧反应
反应装置
反
应
现
象
在空气中燃
烧
①产生微弱的淡
蓝色火焰;②生成
有刺激性气味的
气体,放出热量
不产生火焰,发出
红光,放出热量
在空气中不燃烧,
保持红热
在氧气中燃
烧
①产生明亮的蓝
紫色火焰;②生成
有刺激性气味的
气体
不产生火焰,发出
白光,放出大量
热,生成使澄清石
灰水变浑浊的气
体
①剧烈燃烧,火星
四射;②放出大量
热,生成黑色固体
文字表达式 硫+氧气――→点燃
二氧化硫
碳+氧气――→点燃
二氧化碳
铁+氧气――→点燃
四氧化三铁
注意事项
①硫用量要少,防
止生成物对空气
造成污染;
②瓶底部盛放少
量水,以吸收生成
的气体,防止污染
空气
木炭应慢慢伸入
瓶中,使之与氧气
充分反应
①铁丝无锈,且绕
成螺旋状,以增大
铁丝的受热面积;
②铁丝下端系火
柴棒引燃;③瓶底
预先放少量的水
或细沙,防止溅落
的熔融物炸裂瓶
底
硫燃烧和铁丝燃烧实验中,集气瓶底部都留有少量水,水的作用相同吗?是否都可以用
细沙替代?
不相同。前者是为了吸收二氧化硫,减少空气污染,不可以用细沙替代;后者是为了防
止高温熔融物溅落,炸裂集气瓶底部,可以用细沙替代。
谈重点 学习有关氧气性质实验应注意什么
要会准确描述并记住实验现象,会写燃烧反应文字表达式,同时注意以下几点:①可燃
物在氧气中比在空气中燃烧更加剧烈;②某些在空气中不能燃烧的物质可以在氧气中燃烧,
比如铁丝;③任何物质燃烧都放出热量。
【例 2】下面是小文同学对实验现象的描述,其中正确的是( )
A.木炭燃烧后生成黑色固体
B.细铁丝伸入盛有氧气的集气瓶中剧烈燃烧
C.红磷燃烧后生成气体五氧化二磷
D.硫燃烧后产生有刺激性气味的气体
解析:
A × 木炭燃烧生成物是无色气体,不是固体
B × 细铁丝末端系火柴且点燃后才能燃烧
C × 红磷燃烧后生成的五氧化二磷是固体
D √ 二氧化硫是有刺激性气味的气体
答案:D
提示:学习中应关注木炭、铁丝、硫等燃烧的现象并会描述,关注物质状态的变化。
3
3.化合反应和氧化反应
(1)化合反应
①定义:两种或两种以上物质生成另一种物质的反应叫化合反应。
②特点:多变一,即无论反应物有多少种,生成物只有一种。
③表示式:A+B―→AB 或 A+B+C―→ABC
【例 3—1】下列反应属于化合反应的是( )
A.水――→通电 氢气+氧气
B.碳+氧化铜――→加热 铜+二氧化碳
C.磷+氧气――→点燃 五氧化二磷
D.过氧化氢――→二氧化锰水+氧气
解析:化合反应的特点是“多变一”, A 、B、D 的生成物有两种,都不属于化合反应。
C 的生成物是一种,属于化合反应。
答案:C
(2)氧化反应
①定义:物质跟氧发生的反应叫氧化反应。
②特点:有氧参加,氧体现氧化性。
③一类特殊的氧化反应:有些氧化反应进行得很缓慢,不易被人察觉到,称为缓慢氧化,
如钢铁生锈、食物腐烂、呼吸作用等。
(3)氧化反应和缓慢氧化属于包含关系。氧化反应分为剧烈的氧化反应(简称剧烈氧化)
和缓慢的氧化反应(简 称缓慢氧化)两种。燃烧属于剧烈的氧化反应。剧烈氧化、缓慢氧化
和氧化反应的关系如图所示。
正确理解氧化反应
应注意理解氧化反应定义中“氧”的含义。这里的“氧”可以是“氧气”,也可以是
含“氧”的物质。氧化反应不一定都是物质跟氧气发生的反应。有些含氧化合物与物质发生
的反应也是氧化反应。
【例 3—2】生活中有关缓慢氧化的 实例很多,下列反应中不属于缓慢氧化的是( )
A.牛奶变酸
B.钢铁生锈
C.铁丝在氧气中燃烧
D.呼吸作用
解析:A、B、D 都是很缓慢的氧化反应,不易观察到,属于缓慢氧化;C 反应剧烈,属
于剧烈氧化反应。
答案:C
4.化合反应与氧化反应的关系
化合反应不一定是氧化反应,氧 化反应也不一定是化合反应,二者属于交叉关系。如
图。
其中,A 表示化合反应,如二氧化碳+水―→碳酸;
B 表示既是氧化反应又是化合反应,如碳+氧气――→点燃 二氧化碳;
4
C 表示氧化反应,如石蜡+氧气――→点燃 二氧化碳+水。
【例 4】(综合题)下列反应中属于氧化反应的是________,属于化合反应的是________,
既属于化合反应又属于氧化反应的是________。
A.铜+氧气――→加热 氧化铜
B.氨气+氧气――→催化剂 一氧化氮+水
C.氢气+氧气――→点燃 水
D.甲烷+氧气――→点燃 二氧化碳+水
E.氨气+氯化氢―→氯化铵
F.一氧化碳+氧气――→点燃 二氧化碳
解 析:本题考查对化合反应和氧化反应的理解。多种物质生成一种物质的反应叫化合
反应;物质与氧发生的反应是氧化反应,这里的“氧”可以是“氧气”,也可以是含“氧”
的物质,两个特征都具备的既是化合反应又是氧化反应。
答案:ABCDF ACEF ACF
5.剧烈氧化与缓慢氧化的对比
比较 剧烈氧化 缓慢氧化
相同点 均与氧气反应,均有热量放出
不同点 反应快,现象明显,发光 反应缓慢,不易察觉,不发光
实例 碳、硫等的燃烧 动植物呼吸,食物腐烂
辨误区 物质燃烧一定需要点燃吗
一般情况下,物质燃烧需要点燃,以使可燃物温度达到其着火点。有些着火点较低的物
质(如白磷,着火点为 40 ℃)在空气中发生缓慢氧化时产生的热量若来不及散失,会引起物
质自发燃烧,这种现象叫自燃。
【例 5—1】既包含缓慢氧化,又包含剧烈氧化的变化是( )
A.食物腐败
B.铁生锈
C.酒精遇火燃烧
D.白磷在空气中自发燃烧
解析:
A × 食物腐败、铁生锈进行得很缓慢,属于缓慢氧化B ×
C × 酒精遇火燃烧进行得很快,属于剧烈氧化
D √ 白磷自燃是由白磷缓慢氧化而引起的剧烈氧化
答案:D
【例 5—2】生活中常 见的下列变化没有氧气参加的是( )
A.电灯发光
B.动植物的新陈代谢
C.食物腐烂
D.煤炭燃烧
解析:电灯发光没有新物质生成,属于物理变化,没有氧气参加。动植物的新陈代谢、
食物腐烂属于缓慢氧化,有氧气参加。煤炭燃烧属于剧烈氧化,也有氧气参加。
答案:A
6.正确描述氧气性质实验的现象
(1)区分“光与火焰”“烟与雾”
光≠火焰。光强烈,火焰俗称火苗,相对柔和。像氢气、甲烷等可燃性气体和熔、沸点
较低且易汽化的物质酒精、硫、蜡烛燃烧时可产生火焰。木炭、铁丝、镁条等高沸点的固体
燃烧时只发光,不产生火焰。并不是所有的物质燃烧都会产生火焰。
烟≠雾。烟是固体小颗粒分散形成的;雾是小液滴分散形成的。如磷燃烧时生成白烟;
早晨的雾是小液滴。
(2)区分“实验现象与实验结论”
5
实验现象是实验过程中看到的、听到的、摸到的、闻到的等。如铁丝在氧气中燃烧的实
验现象是“剧烈燃烧,火星四射、生成黑色固体、放出大量的热”。实验结论是分析实验现
象得出的结果或原理,如上述实验中,生成四氧化三铁是实验结论,非实验现象。
辨误区 描述实验现象时不能指出生成物
实验现象一般是观察或感受到的物质的色、态、味、光、火焰、烟、雾、热等。描述实
验现象常犯的错误是指出生成物,从而错把实验结论当成实验现象。
【例 6—1】下面是某研究性小组的一位同学对氧气性质有关实验现象的描述,其中正
确的是( )
A.碳在氧气中燃烧放出白烟
B.红磷在空气中燃烧冒白烟
C.铁丝在氧气中燃烧生成四氧化三铁
D.硫在氧气中燃烧发出淡蓝色的火焰
解析:
A × 白烟是白色固体小颗粒。碳在氧气中燃烧产生无色气体,红磷燃
烧产生白色固体B √
C × 生成四氧化三铁是实验结论非实验现象
D × 硫在氧气中燃烧发出蓝紫色火焰
答案:B
【例 6—2】下列关于实验现象的描述中,正确的是( )
A.铁丝在空气中剧烈燃烧,火星四射
B.红磷在空气中燃烧产生大量白色烟雾
C.硫在空气中燃烧发出淡蓝色火焰
D.木炭在氧气中燃烧发出白光,生成二氧化碳
解析:描述实验现象要客观、准确,不要涉及生成物的名称。铁丝在空气中不燃烧,A
错误;红磷燃烧时产生大量白烟,不是产生白色烟雾,B 错误;生成二氧化碳是木炭在氧气
中燃烧的实验结论,不是实验现象。
答案:C
【例 6—3】下列有关实验现象的描述错误的是( )
A.红磷在空气中燃烧时产生大量白烟
B.硫黄在氧气中燃烧,产生蓝紫色火焰,生成无色无味的气体
C.细铁丝在纯氧气中燃烧,火星四射,生成黑色固体
D.在空气中加热铜片,铜片表面有黑色固体生成
解析:硫黄在氧气中燃烧,产生蓝紫色火焰,生成无色有刺激性气味的气体。
答案:B
7.氧气令人欢喜令人忧
氧气是一种化学性质比较活泼的气体,一定条件下,可以与许多物质(不是所有的物质)
发生氧化反应,有些剧烈,有些缓慢。氧气令人欢喜令人忧 。
(1)氧气能供给呼吸、支持燃烧。正是有了氧气,才有生命,才有光明和温暖,才有生
机勃勃的地球,人类才能上天、入海,才能酿造出醇香美酒。
(2)氧气也带来一些隐患。不知不觉中,食品变质了,金属生锈了,火灾出现了,吞噬
美丽的家园甚至宝贵生命。在生产、生活中,我们应合理利用氧气,扬长避短,让它更好地
为我们服务。
【例 7】(实际应用题)氧气是一种化学性质比较活泼的气体,可以与许多物质发生反应。
由于氧气的这一特性,使氧气在工农业生产和生活中有着广泛的应用;也是由于氧气的这一
性质,人们为了生产和生活的需要,在某种情况下,要使物质与氧气隔绝。请你从两个方面
各举两例予以说明。
(1)应用氧气:
①________________________________________________________________________;
②________________________________________ ________________________________
6
。
(2)隔绝氧气:
①________________________________________________________________________;
②________________________________________________________________________。
解析:只要认真思考,从支持燃烧、供给呼吸和缓慢氧化等角度很容易找到应用氧气和
隔 绝氧气的实例。氧气具有两面性。应用氧气目的是利用氧气为人类服务,属于氧气的用
途;隔绝氧气目的是消除氧气带来的危害。
答案 :(1)潜水、登山、取暖、加热食物、富氧炼钢、气焊、气割等(任选两个)
(2)金属防锈、食物防腐、消防灭火等(任选两个)
相关文档
- 九年级化学上册 31 分子和原子教学2021-11-0623页
- 九年级化学上册 单元专题复习4 自2021-11-0612页
- 人教版九年级化学上册课件第三单元2021-11-06105页
- 2019九年级化学上册 第六单元 碳和2021-11-062页
- 2019九年级化学上册 第三章 物质构2021-11-063页
- 2019九年级化学上册 第五章 化学方2021-11-068页
- 2020九年级化学上册基础训练空气成2021-11-062页
- 2019九年级化学上册 第五单元 定量2021-11-067页
- 新人教版九年级化学上册例题精讲:第2021-11-064页
- 2020九年级化学上册 课题3 元素 32021-11-064页