- 369.00 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2018广州
相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 Fe-56 Co-59 Cu-64
一、选择题(本题包括20题,每小题2分,共40分)
1. 下列关于空气的说法正确的是( )
A. 空气中的氮气约占总体积的21% B. 空气中的氧气能支持燃烧
C. 空气中的稀有气体没有任何用途 D. 空气中的二氧化碳会造成酸雨
【答案】B
【解析】空气中的氮气约占总体积的78%,氧气占21%;氧气有助燃性,能支持燃烧;稀有气体化学性质稳定,可做保护气;通电时能发出特定颜色的光,可做电光源;二氧化碳和水反应生成碳酸,空气中的二氧化碳会导致雨水呈酸性,但不是酸雨,酸雨是由二氧化硫、二氧化氮氧化物形成的。故选B。
2. 下列属于物理变化的是( )
A. 铁锅生锈 B. 蜡烛燃烧 C. 粮食酿酒 D. 水结成冰
【答案】D
【解析】铁锅生锈铁变为氧化铁,属于化学变化;蜡烛燃烧生成二氧化碳和水,属于化学变化;粮食酿酒生成酒精,属于化学变化;水结成冰没有新的物质生成,只是水的状态发生改变,属于物理变化。故选D。
3. 生产下列物品所用的主要材料中不属于有机合成材料的是( )
A. 汽车轮胎 B. 台灯塑料底座 C. 不锈钢水龙头 D. 有机玻璃标牌
【答案】C
【解析】汽车轮胎的主要材料是合成纤维、合成橡胶、 塑料和有机玻璃是由甲基丙烯酸甲都属于有机高分子合成材料;不锈钢水龙头属于金属材料。故选C。
4. 下图为某粒子的结构示意图,下列说法正确的是( )
A. 该粒子有12个质子 B. 该粒子有2个电子层
C. 该粒子属于非金属元素 D. 该粒子已达到相对稳定结构
【答案】A
【解析】该结构示意图表示为镁原子,镁原子的质子数=核外电子数=核电荷数=12;该粒子有3个电子层;该粒子属于金属元素;该粒子失去2个电子后达到相对稳定结构。故选A。
5. 下列有关水的说法不正确的是( )
A. 水质浑浊时可加入明矾使悬浮杂质沉降除去
B. 水的硬度较大时可用过滤的方法降低水的硬度
C. 水中有异味时可加入活性炭除味
D. 可用蒸馏的方法将自来水进一步净化
【答案】B
【解析】明矾在水中会形成絮状物,能加速悬浮杂质沉降;硬水是含可溶钙镁化合物较多的水,过滤只能除掉水中的难溶性固体,不能除掉可溶性物质,水的硬度较大时可用煮沸或蒸馏的方法降低水的硬度;活性炭结构疏松多孔,能吸附色素、异味,水中有异味时可加入活性炭除味;蒸馏可除掉水中的可溶性杂质。故选B。
6. 下列有关金刚石、石墨的说法正确的是( )
A. 都是由碳元素组成 B. 都是黑色固体C. 都能导电 D. 硬度都很大
【答案】A
【解析】金刚石、石墨都是由碳元素组成,是碳的两种不同单质;石墨是黑色固体,金刚石是无色透明的晶体;石墨能导电,金刚石不能;金刚石是自然界中硬度最大的物质,石墨是自然界中硬度最小的物质。故选A。
7. 下列说法正确的是( )
A. 石油是一种混合物 B. 可燃冰是可再生能源
C. 煤燃烧时只生成二氧化碳 D. “西气东输”的“气”是指氢气
【答案】A
【解析】石油是由多种物质组成,是混合物;可燃冰是不可再生能源;煤的主要成分是碳、氢元素组成的化合物,燃烧时主要生成物有二氧化碳、水;“西气东输”的“气”是指天然气。故选A。
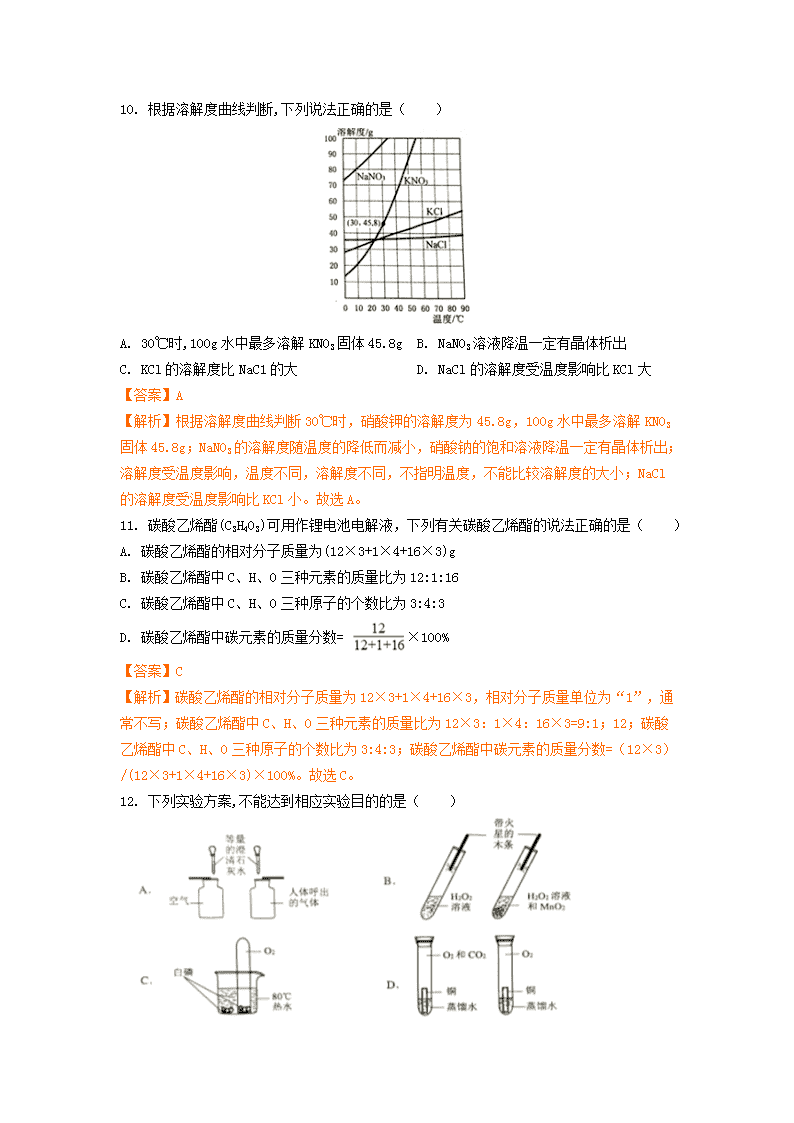
8. 下列操作中不正确的是( )
A. 熄灭酒精灯 B. 闻药品气味 C. 读出液体体积 D. 稀释浓硫酸
【答案】D
【解析】用灯帽盖灭酒精灯,吹灭酒精灯易导致灯内酒精着火,甚至引起酒精灯爆炸;闻气体气味时,应该用手在瓶口轻轻扇动,使少量气体进入鼻孔闻气味;量取液体读数时,要平视凹液面的最低处;稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌,使热量及时扩散,防止酸液飞溅,切不可将水倒入硫酸中。故选D。
9. 下列物质属于碱的是( )
A. H2O B. NaHCO3 C. Ca(OH)2 D. H3BO3
【答案】C
【解析】H2O属于氧化物;NaHCO3 属于盐;Ca(OH)2 属于碱;H3BO3属于酸。故选C。
10. 根据溶解度曲线判断,下列说法正确的是( )
A. 30℃时,100g水中最多溶解KNO3固体45.8g B. NaNO3溶液降温一定有晶体析出
C. KCl的溶解度比NaC1的大 D. NaCl的溶解度受温度影响比KCl大
【答案】A
【解析】根据溶解度曲线判断30℃时,硝酸钾的溶解度为45.8g,100g水中最多溶解KNO3固体45.8g;NaNO3的溶解度随温度的降低而减小,硝酸钠的饱和溶液降温一定有晶体析出;溶解度受温度影响,温度不同,溶解度不同,不指明温度,不能比较溶解度的大小;NaCl的溶解度受温度影响比KCl小。故选A。
11. 碳酸乙烯酯(C3H4O3)可用作锂电池电解液,下列有关碳酸乙烯酯的说法正确的是( )
A. 碳酸乙烯酯的相对分子质量为(12×3+1×4+16×3)g
B. 碳酸乙烯酯中C、H、O三种元素的质量比为12:1:16
C. 碳酸乙烯酯中C、H、O三种原子的个数比为3:4:3
D. 碳酸乙烯酯中碳元素的质量分数= ×100%
【答案】C
【解析】碳酸乙烯酯的相对分子质量为12×3+1×4+16×3,相对分子质量单位为“1”,通常不写;碳酸乙烯酯中C、H、O三种元素的质量比为12×3:1×4:16×3=9:1;12;碳酸乙烯酯中C、H、O三种原子的个数比为3:4:3;碳酸乙烯酯中碳元素的质量分数=(12×3)/(12×3+1×4+16×3)×100%。故选C。
12. 下列实验方案,不能达到相应实验目的的是( )
A. 比较空气与人体呼出的气体中CO2含量 B. 探究MnO2能否加快H2O2分解
C. 验证燃烧需要温度达到着火点 D. 探究CO2对铜生锈是否有影响
【答案】C
【解析】空气中二氧化碳含量较少,不能使澄清石灰水变浑浊,人体呼出的气体中CO2含量较高,能使澄清石灰水变浑浊;没加二氧化锰的试管中带火星的木条不复燃,加入MnO2的试管中,带火星的木条复燃,说明二氧化锰能加快H2O2分解;试管内(有氧气)的白磷燃烧,水中(没有氧气)白磷不燃烧,验证燃烧需要可燃物与氧气充分接触;两支试管中,除一个有二氧化碳,一个没有二氧化碳外,其它条件完全相同,符合控制变量的原则,可探究CO2对铜生锈是否有影响。故选C。
13. 下列反应没有明显现象的是( )
A. 氧化铁与稀盐酸反应 B. 稀盐酸与澄清石灰水反应氯化钙与水反应
C. 氧化钙与水反应 D. 铝丝与硝酸银溶液反应
【答案】B
【解析】氧化铁与稀盐酸反应生成易溶于水的氯化铁和水,现象是固体逐渐消失,溶液由无色变成黄色;;稀盐酸与澄清石灰水反应氯化钙与水反应,无明显现象;氧化钙与水反应放出大量热;铝丝与硝酸银溶液反应生成银和硝酸铝,铝丝表面开始会出现黑色物质。故选B。
14. 下列清洁用品中碱性最强的是( )
A. 厕所清洁剂pH=1 B. 牙膏pH=8 C. 肥皂pH=10 D. 炉具清洁剂pH=13
【答案】D
【解析】碱性溶液的pH大于7,pH越大碱性越强。炉具清洁剂pH最大,碱性最强。故选D。
15. 有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象X放入ZCln溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是( )
A. X>Y>Z B. Z>X>Y C. X>Z>Y D. Y>X>Z
【答案】B
【解析】X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,说明X、Z在氢前,Y在氢后;X放入ZCln溶液,没有明显现象,说明X在Z后,三种金属的活动性由强到弱的顺序是Z>X>Y。故选B。
16. 下列关于化肥的说法不正确的是( )
A. 化肥对提高农作物的产量具有重要作用
B. 氯化钾(KCl)和磷酸氢二铵[(NH4)HPO4]都属于复合肥料
C. 铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D. 化肥的过度使用会造成土壤酸化,可用熟石灰改良
【答案】B
【解析】氮、磷、钾肥对提高农作物的产量具有重要作用;只含有氮、磷、钾中的一种元素时,氮肥、磷肥、钾肥;同时含有氮磷钾中的两种或两种以上元素时为复合肥。氯化钾(KCl)属于钾肥;磷酸氢二铵[(NH4)HPO4]属于复合肥料;铵态氮肥与熟石灰混合研磨后能产生刺激性气体氨气;可用熟石灰改良酸性土壤。故选B。
17. 下列描述不正确的是( )
A. CO有毒且无色无味,使用燃气时要注意室内通风
B. CO2作为气体肥料在农业生产中有广泛应用
C. N2充入食品包装袋中可起防腐作用
D. CH4在空气中燃烧是化合反应
【答案】D
【解析】含碳燃料在氧气不足时发生不完全燃烧生成CO,一氧化碳有毒,使用燃气时要注意室内通风,防止一氧化碳中毒;CO2是植物光合作用的原料,可作为气体肥料;N2化学性质稳定,充入食品包装袋中可起防腐作用;CH4在空气中燃烧生成二氧化碳和水,不是化合反应。故选D。
18. 下列有关氢氧化钾的说法正确的是( )
A. 氢氧化钾固体露置在空气中易变质
B. 氢氧化钾溶液能使石蕊溶液变红
C. 氢氧化钾溶液与氧化铜反应生成蓝色沉淀
D. 2mL氢氧化钾溶液与1mL硫酸溶液恰好完全反应
【答案】A
【解析】A. 氢氧化钾固体露置在空气中易与空气中的二氧化碳反应变质,正确;B. 氢氧化钾溶液显碱性,能使石蕊溶液变蓝,错误;C. 氢氧化钾溶液与氧化铜不反应,能与氯化铜反应生成蓝色沉淀,错误;D. 氢氧化钾和硫酸反应的方程式为:2NaOH+ H2SO4 = Na2SO4+2H2O ,所以每2moL氢氧化钾与1moL硫酸恰好完全反应,错误。故选A。
19. 下列实验中,对应的现象和结论都正确且两者具有因果关系的是( )
实验操作
现象
结论
A
常温下,将硫放入氧气中
剧烈燃烧,发出蓝紫色火焰
硫能与氧气反应
B
向某无色溶液中滴入CaCl2溶液
有白色沉淀产生
该溶液中一定含有碳酸盐
C
向CaCO3中滴加稀盐酸
有气泡产生
盐酸易挥发
D
用氯化钠溶液进行导电性试验,观察小灯泡是否变亮
小灯泡变亮
氯化钠溶液中存在自由移动的离子
A. A B. B C. C D. D
【答案】D
【解析】点燃条件下,将硫放入氧气中,剧烈燃烧,发出蓝紫色火焰,硫能与氧气反应;向某无色溶液中滴入CaCl2溶液,有白色沉淀产生,该溶液中不一定含有碳酸盐,也可能生成氯化银沉淀;向CaCO3中滴加稀盐酸反应生成二氧化碳,产生气泡;氯化钠溶液中含有钠离子和氯离子,可使小灯泡通电变亮。故选D。
20. 除去下列物质中所含杂质(括号内为杂质)的实验,能达到目的的( )
A. NaOH(Na2CO3):加入适量稀盐酸 B. CO(CO2):通过装有浓硫酸的洗气瓶
C. CuO(C):在空气中充分灼烧 D. MgSO4(Na2SO4):溶解,过滤
【答案】C
【解析】加入适量稀盐酸,氢氧化钠和碳酸钠都与盐酸反应生成氯化钠;浓硫酸吸收水蒸气,不能除掉二氧化碳;在空气中充分灼烧,氧化铜不反应,碳燃烧生成二氧化碳逸出,剩余固体只有氧化铜;MgSO4、Na2SO4都是易溶于水的物质,过滤,不能将其分开。故选C。
二、非选择题
21. 从微观的角度回答下列问题
(1) C70表示一个_______________ (填“分子”、“原子”或“离子”)
(2) 一定条件下,6000L氧气可装入容积为40L的钢瓶中,从微观角度分析,原因是:条件改变时,___________。
【答案】(1)分子 (2)分子间隔变小
【解析】(1) C70表示一个分子;(2) 分子间是有间隔的,一定条件下,6000L氧气可装入容积为40L的钢瓶中。
22. 金属锰(Mn)及其化合物用途广泛。铁锰合金(锰钢)可用作大型体育场馆的网封架屋顶材料、铁轨、桥梁等。部分锰的化合物的颜色及溶解性见下表,回答下列问题。
物质
KMnO4
MnO2
MnSO4
Mn(OH)2
MnO(OH)2
颜色
暗紫色
黑色
白色
白色
棕色
溶解性
易溶
难溶
易溶
难溶
难溶
(1)KMnO4读作______________,广泛用作医药杀菌剂和防臭剂
(2)将适当比例的铁矿石(Fe2O3)、软锰矿(MnO2)、焦炭混合加入高炉,通入热空气熔炼,可得到铁锰合金。用化学方程式表示生成金属锰的过程:
①C + O2CO2;② _______________________;③ ________________________。
(3)已知:①MnSO4+2NaOH=Mn(OH)2↓+Na2SO4; ②2Mn(OH)2+O2=2MnO(OH)2 若向盛有MnSO4溶液的试管中加入少量NaOH溶液,静置,预测可观察到的现象是______________。
【答案】 (1)高锰酸钾 (2) C + CO2 2CO (3) 2CO + MnO2Mn + 2CO2 (4)产生白色沉淀,静置后,白色沉淀变棕色
【解析】(1)KMnO4读作高锰酸钾;(2)生成金属锰的过程:①C + O2CO2;②碳和二氧化碳高温条件下反应生成一氧化碳,产生还原剂,方程式为:C + CO2 2CO;③一氧化碳和二氧化锰在高温条件下反应生成锰和二氧化碳,反应方程式为:2CO + MnO2Mn + 2CO2;(3) Mn(OH)2↓是白色沉淀, MnO(OH)2 是棕色沉淀, 若向盛有MnSO4溶液的试管中加入少量NaOH溶液,静置,可能观察到的现象是先产生白色沉淀,静置后,白色沉淀变棕色。
23. 某固体混合物可能含有CuSO4、CaCO3、Na2CO3、KOH的一 种或两种,为了确定该混合物的成分,进行如下实验:
步骤I:取少量固体于烧杯中,加水,搅拌,固体全部溶解,得到无色溶液A。
步骤Ⅱ:取少量溶液A于试管中,滴加过量MgCl2溶液,有白色沉淀产生;再加入过量稀盐酸,沉淀消失,有气泡产生。
(1)步骤Ⅱ中产生的气泡是__________________ (填化学式)
(2)根据上述实验推断该混合物的成分,肯定含有的是________ ,可能含有的是_________。
(3)设计实验进一步确定混合物组成,依次用到的试剂是_______________。
【答案】 (1) CO2 (2)碳酸钠 (3)氢氧化钾 (4)过量氯化钡(氯化钙/硝酸钡/硝酸钙)溶液,酚酞溶液
【解析】步骤I:取少量固体于烧杯中,加水,搅拌,固体全部溶解,得到无色溶液A,说明没有碳酸钙、硫酸铜;步骤Ⅱ:取少量溶液A于试管中,滴加过量MgCl2溶液,有白色沉淀产生;再加入过量稀盐酸,沉淀消失,有气泡产生,说明有碳酸钠,碳酸钠和氯化镁生成碳酸镁沉淀,碳酸镁与盐酸反应生成氯化镁和二氧化碳、水;氢氧化钾也能与氯化镁生成氢氧化镁白色沉淀,氢氧化镁和盐酸能反应生成氯化镁而溶解。(1)步骤Ⅱ中产生的气泡是CO2;(2)根据上述实验推断该混合物的成分,肯定含有的是碳酸钠 ,可能含有的是氢氧化钾;(3)为进一步确定混合物组成,先向溶液中加入过量的氯化钡(或氯化钙等)溶液,除尽碳酸钠,然后向所得溶液中加入酚酞试液,如果酚酞试液变红,说明有氢氧化钾,反之,没有氢氧化钾。
24. 金属钴(Co)在国防工业中有重要应用。某矿石中含钻的氧化物(CoO、Co2O3)研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件。
(1)写出下列化合物中Co元素的化合价:CoO_________,Co2O3______________。
(2)酸浸时钻的氧化物发生如下反
反应I CoO+H2SO4=CoSO4+H2O
反应Ⅱ 2Co2O3+4H2SO 4=4CoSO4+O2↑+4H2O
反应Ⅲ Co2O3+2H2SO4+Na2SO3=2CoSO4+2H2O+Na2SO4
①反应后溶液中含钻元素的微粒是_________ (填化学符号)
②已知反应前矿石中CoO的质量为ag,Co2O3的质量为bg,则理论上可以生成CoSO4____g(用含a、b的式子表示)
(3)为探究最佳提取条件,将矿石在一定条件下酸浸4小时,测量钴元素的浸出率部分数据如下:
①本实验研究了哪些因素对钴元素浸出率的影响__________________________________;
②根据上表数据,其他条件不变,温度升高,钻元素的浸出率_________________________;
③工业生产中采用实验______________(填编号)的提取条件更合理。
【答案】(1)+2 (2)+3 (3)Co2+ (4)155×(a/75 + b/83) (5)硫酸用量、亚硫酸钠用量、温度 (6)增大 (7)5
【解析】(1)合物中氧元素的化合价为-2价, CoO中Co为+2价,Co2O3中Co为+3价;(2) ①由上述方程式可知,反应后钴元素以CoSO4存在于溶液中,所以溶液中含钻元素的微粒是Co2+;②设CoO生成CoSO4的质量为x,Co2O3生成CoSO4的质量为y,
CoO+H2SO4=CoSO4+H2O
75 155
ag x
75/ag=166/x x=155×ag÷75
2Co2O3+4H2SO 4=4CoSO4+O2↑+4H2O
332 155×4
bg y
332/bg= 155×4/y y= 155×4×bg÷332
则理论上可以生成CoSO4的质量为:155×(a/75 + b/83);
(3) ①由表格中数据可知,对钴元素浸出率产生影响的因素有硫酸用量、亚硫酸钠用量、温度;②根据上表数据,其他条件不变,温度升高,钻元素的浸出率增大;③工业生产中应采用实验5的方案,因为该条件下,钻元素浸出率最高。
25. 氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下
(1)推测草酸的化学式是____________;
(2)“沉锌”过程中发生复分解反应,反应的化学方程式是_______________________________
(3) “操作A”的名称是______________ 实验室常用的研磨仪器是_____________;
(4)“高温灼烧”时草酸锌分解,反应的化学方程式是______________________________。
【答案】(1)H2C2O4 (2)ZnCl2 + (NH4)2C2O4==ZnC2O4↓ + 2NH4Cl (3)过滤 (4)研钵 (5).ZnC2O4ZnO + CO↑ + CO2↑
【解析】(1)草酸根显-2价,据此推测草酸的化学式是H2C2O4 ;(2) “沉锌”过程中发生复分解反应,反应的化学方程式是ZnCl2 + (NH4)2C2O4==ZnC2O4↓ + 2NH4Cl;(3) “操作A”是将液体与难溶性固体分离,是过滤, 实验室常用的研磨仪器是研钵;(4)“高温灼烧”时草酸锌分解得气体混合物,可推知气体为一氧化碳和二氧化碳,反应的化学方程式是ZnC2O4 ZnO + CO↑ + CO2↑。
26. 下图是几项基本实验操作的示意图
(1)仪器X的名称是____________;加热液体时,液体体积不能超过试管容积的_______;
(2)蒸发结晶时,用玻璃棒搅拌,当_______________________,停止加热;
(3)测定溶液pH时,用玻璃棒蘸取待测液滴到pH试纸上,______________,读出pH。
【答案】(1)试管夹 (2) 1/3 (3)较多固体时 (4)显色与标准比色卡比较
【解析】(1)仪器X的名称是试管夹;加热液体时,液体体积不能超过试管容积的三分之一,否则易因沸腾而喷出来,导致人被烫伤或腐蚀;(2)蒸发结晶时,用玻璃棒搅拌,使液体受热均匀,防止液体飞溅;当有大量晶体析出(或少量液体剩余)时,停止加热,如果将水蒸干,会导致晶体飞溅;(3)测定溶液pH时,用玻璃棒蘸取待测液滴到pH试纸上,呈现一定的颜色,然后将显示的颜色和标准比色卡比较,读取pH。
27. 下图是实验室制备气体的部分装置
(1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验
①该方法制得O2的化学方程式是______________________________________。
②可选用_____和________(填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后_____________________,观察到有气泡冒出,说明装置气密性良好。
(2)氢气被认为是理想的清洁、高能燃料
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用_______(填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器——>检查装置气密性——>装入药品制备氢气——>_____________——>点燃。
②电解水也可制得H2。装置如图F,_________管中产生的是氢气
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_________。
A.用矿石生产锌和硫酸,再相互反应 B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水 D.利用风能、水力发电,再电解水
【答案】(1)2KClO32KCl + 3O2↑ (2)B (3) C (4)双手握住试管(5)A (6)验纯 (7)甲 (8)BD
【解析】(1)实验室用氯酸钾和二氧化锰加热制取氧气:2KClO32KCl + 3O2↑;(2)氯酸钾法制氧气应选加热固体制取气体的发生装置B:氧气的密度比空气大,可用向上排空气法收集选用装置C:检装装置气密性的方法:把导管口放入水中,然后双手握住试管,观察到有气泡冒出,或松开手后,导管内形成一段水柱,说明实近气密性;(2)①实验室制取氢气采用固、液常温型,选用装置A。实验步骤:组装仪器——>检查装置气密性——>装入药品制备氢气——>_验纯——>点燃;②电解水时,正极生成氧气,负极生成氢气;③用矿石生产锌和硫酸,再相互反应生成二氧化硫污染物;在催化剂作用下,利用太阳能光解水生成氧气和氢气,无污染;利用煤燃烧发电,生成污染物;利用风能、水力发电,再电解水,没有无污染生成。故选BD。
28. 室温为25℃时,某小组用无水氯化铜粉末制备氯化铜大晶体,制备过程如下:
步骤I:查阅资料,得到氯化铜溶解度数据如下
温度(℃)
0
20
25
40
50
60
80
溶解度(g)
69.2
74.5
76.4
81.8
85.5
89.4
98.0
步骤Ⅱ:配制少量CuCl2热饱和溶液,冷却结晶,得到晶种。
步骤Ⅲ:把晶种悬挂在新配制的CuCl2热饱和溶液中,室温下静置数天,形成大晶体。
步骤Ⅳ:取出大晶体,处理剩余的溶液(母液)。
根据以上信息,回答下列问题:
(1)用20mL蒸馏水(密度约为1g/mL)配制50℃的氯化铜饱和溶液。
①计算需称取CuCl2的质量是_______g。
②将称取的CuCl2固体和20mL水倒入烧杯中,_______________(填操作名称),直至固体完全溶解。
(2)母液中Cu2+属于重金属离子,随意排放将导致环境污染。下列方法可用于母液处理的是__________。
A.收集母液于敞口容器中,用报纸包住容器口,待水分自然蒸干后保存所得固体
B.向母液中加入适量AgNO3,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
C.向母液中加入适量NaOH,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
(3)若用铁粉置换出母液中的铜,100g母液需要铁粉的质量至少是_____________ g(只列计算式,已知CuCl2的相对分子质量为135)。
【答案】(1) 17.1 (2)搅拌 (3)A C (4)
【解析】(1)①溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。由表格中数据可知,50℃时,氯化铜的溶解度为85.5g,用20mL蒸馏水(密度约为1g/mL)配制50℃的氯化铜饱和溶液, 需称取CuCl2的质量是17.1g;②将称取的CuCl2固体和20mL水倒入烧杯中,用玻璃棒搅拌,直至固体完全溶解;(2)根据表格判断氯化铜的溶解度受温度影响不大,可用蒸发结晶法提纯。收集母液于敞口容器中,用报纸包住容器口,防止落入其他物质,引入杂质,待水分自然蒸干(蒸发结晶)后保存所得固体,则不会有含铜离子的液体排放,不会导致污染;向母液中加入适量AgNO3,充分反应后生成的沉淀是氯化银,过滤,滤渣干燥保存,滤液中仍然有铜离子,倒入下水道,仍会导致污染;向母液中加入适量NaOH,生成氢氧化铜沉淀和氯化钠,充分反应后过滤,滤渣干燥保存,滤液中只有氯化钠,没有铜离子,倒入下水道,不会因重金属导致污染;(3) 25℃时氯化铜的溶解度为76.4g,100g母液中含有氯化铜的质量为x,76.4g/176.4g=x/100g x=100g×76.4g÷176.4g;若用铁粉置换出母液中的铜,设100g母液需要铁粉的质量至少是y,
CuCl2 + Fe = FeCl2 + Cu
135 56
y 135/=56/y
29. 硫酸氢钠( NaHSO4)溶于水形成无色溶液,请预测其化学性质,说明预测的依据,并设计实验验证。限选试剂是:NaHSO4溶液、BaCl2溶液、FeSO4溶液、Na2CO3溶液、NaOH溶液、稀盐酸、酚酞溶液、紫色石蕊溶液、镁条、碳粉、氧化铜。
预测
预测的依据
验证预测的实验操作与预期现象
①能够与含Ba2+的盐反应
__________
取少量 NaHSO4溶液于试管中,滴入BaCl2溶液,如果观察到__________,则预测成立
②能够与__________(填物质类别)反应
_________________
_________________,如果观察到____________,则预测成立。
③能够与___________(填物质类别)反应
________________
________________,如果观察到_____________,则预测成立。
【答案】(1) NaHSO4电离出SO42— (2)有白色沉淀产生 (3)碳酸盐 (4)NaHSO4电离出H+ (5)取少量NaHSO4溶液于试管中,滴入Na2CO3溶液(6)有气泡产生 (7) 指示剂 (8)NaHSO4电离出H+ (9)取少量NaHSO4溶液于试管中,滴入紫色石蕊溶液(10)石蕊溶液变红色
【解析】①NaHSO4电离出SO42—,硫酸根离子和Ba2+结合生成硫酸钡沉淀,取少量 NaHSO4溶液于试管中,滴入BaCl2溶液,如果观察到有白色沉淀生成,则预测成立;②能够与碳酸盐反应,因为NaHSO4电离出H+,氢离子和碳酸根离子结合生成水、二氧化碳,如果观察到有气泡产生,则预测成立;③能够与指示剂反应,理由是NaHSO4电离出H+,溶液显酸性,验证方法是:取少量NaHSO4溶液于试管中,滴入紫色石蕊溶液,如果观察到石蕊溶液变红色,则预测成立。