- 265.71 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
中考化学最常考的知识点汇总
二、实验中的规律
1.(1)O2检验:用带火星的木条放入集气瓶中,木条立即复燃。
O2验满:用带火星的木条放在集气瓶口,木条立即复燃。
(2)CO2检验:通入澄清石灰水,振荡,澄清石灰水变混浊。
CO2验满:用燃着的木条放在集气瓶口,木条立即熄灭。
(3)碳酸盐检验:加入稀盐酸,将产生的气体通入澄清石灰水,澄清石灰水变浑浊。
(4)铵盐、铵态氮肥、NH4+检验:加碱[NaOH或Ca(OH)2]加热,产生的气体能使湿润的红色石蕊试纸变蓝。铵态氮肥不能与碱性物质混合施用,否则会降低肥效。
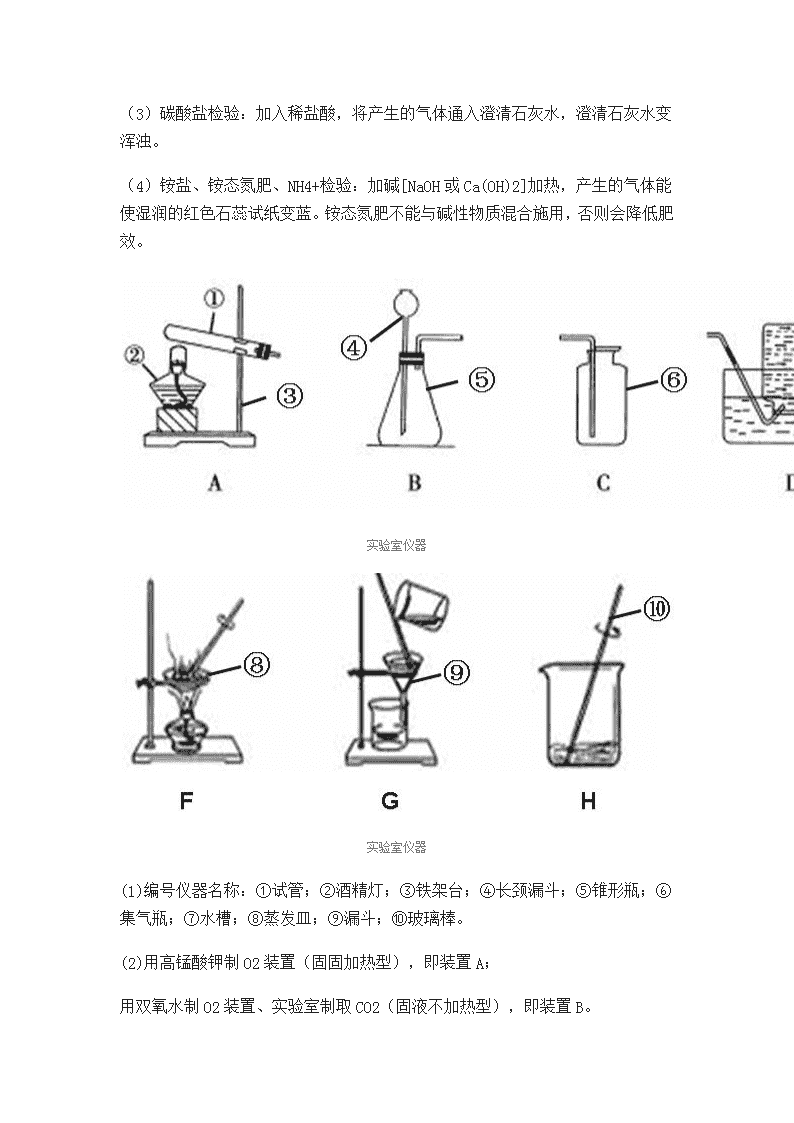
实验室仪器
实验室仪器
(1)编号仪器名称:①试管;②酒精灯;③铁架台;④长颈漏斗;⑤锥形瓶;⑥集气瓶;⑦水槽;⑧蒸发皿;⑨漏斗;⑩玻璃棒。
(2)用高锰酸钾制O2装置(固固加热型),即装置A;
用双氧水制O2装置、实验室制取CO2(固液不加热型),即装置B。
(3)装置A中,给试管中的固体加热,要先预热,试管口应略向下倾斜(防止冷凝水倒流,引起试管破裂)。
(3)装置A中,给试管中的固体加热,要先预热,试管口应略向下倾斜(防止冷凝水倒流,引起试管破裂)。
(4)生成的气体难溶于水(不与水反应)的,都可用排水法收集,即装置D(如收集氧气:应等气泡连续均匀放出时开始收集,并将收集好的集气瓶正放在桌子上)。
生成的气体密度比空气大的,都可用向上排空气法收集,即装置C。
生成的气体密度比空气小的,都可用向下排空气法收集,即装置E。
(5)制气体实验,先检查装置的气密性(如右图:将导气管一端浸入水中,用手握住试管或其他容器的外壁,若观察到导气管口有气泡冒出,松开手一段时间后导气管内形成一段水柱,则装置气密性良好;否则为漏气),铁夹应夹在距管口1/3处。
(6)装置B中,用长颈漏斗制气体实验时,漏斗的末端管口应插入液面以下(防止产生的气体从漏斗口逸出)。
(7)点燃可燃性气体(H2、CO、CH4)时,一定先要检验它的纯度。(否则与空气混合点燃可能爆炸,实际上任何可燃性气体或粉尘都有可能)。
(8)使用有毒气体做实验时,最后一定要处理尾气(防止污染空气)。
(9)蒸发为装置F,过滤为装置G,溶解为装置H。三个操作都用到玻璃棒,作用分别为搅拌使受热均匀,引流,搅拌加速溶解。玻璃棒还可用于转移固体。
3.pH测定:取一小段pH试纸于表面皿或玻璃片上,将玻璃棒蘸取的试样溶液滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照。(pH试纸不能预先用水湿润,否则可能影响检测结果。若试样溶液为酸性溶液,则结果偏大;若试样溶液为碱性溶液,则结果偏小;若试样溶液为中性溶液,则不影响。)
4.浓硫酸与水混合时,会产生大量热。稀释浓硫酸时,要把浓硫酸缓缓注入盛有水的烧杯中,用玻璃棒引流(或沿着烧杯壁缓缓倾倒)并不断搅拌。
三、常见知识点
1.常见物质的俗名及化学式
(1)天然气、沼气、瓦斯:CH4(最简单的有机物)
(2)生石灰:CaO 熟石灰、消石灰:Ca(OH)2 大理石、石灰石:CaCO3
(3)苛性钠、火碱、烧碱:NaOH (4)纯碱、碱面、苏打:Na2CO3(水溶液呈碱性)
(5)碳酸氢钠、小苏打:NaHCO3(水溶液呈碱性) (6)食盐:NaCl
(7)酒精、乙醇:C2H5OH (8)葡萄糖:C6H12O6
2.黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4 硫(硫磺):淡黄色
红色固体:Cu、红磷 Fe2O3(铁锈):红棕色 KMnO4:紫黑色
Cu2(OH)2CO3(铜绿、铜锈):绿色 铁、镁、铝为银白色(汞为银白色液态)
白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、NaHCO3、Na2CO3、KCl、NaCl
无水CuSO4为白色粉末状固体,遇水变成蓝色(常用于检验酒精中是否含水)。
3.溶液颜色:CuSO4溶液呈蓝色;FeSO4、FeCl2溶液呈浅绿色;KMnO4溶液为紫红色;
FeCl3、Fe2(SO4)3溶液呈黄色,其余溶液一般为无色。
4.沉淀:①盐(白色):CaCO3、BaCO3(溶于酸);AgCl、BaSO4(不溶于水和稀HNO3)
②碱:Cu(OH)2(蓝色) Fe(OH)3(红褐色) 白色:Mg(OH)2、Al(OH)3
5.①具有挥发性的液体:浓盐酸、浓硝酸、浓氨水
②具有吸水性的物质(作干燥剂):浓硫酸、NaOH固体、CaO、无水氯化钙
浓硫酸不能用于NH3的干燥;铁粉可作双吸剂(∵铁生锈是吸收水蒸气和氧气);
NaOH固体、CaO不能用于CO2、SO2、SO3、HCl的干燥
③在空气中放置容易变质:NaOH、CaO 、Ca(OH)2
④敞口放置:浓盐酸(∵挥发性)、浓硫酸(∵吸水性)的溶质质量分数都变小。
6.有毒:CO、NaNO2(工业用盐)、甲醇(CH3OH)。
甲醛、重金属离子(钡、铜、铅、汞等)能使蛋白质变性。
7.①最常见的溶剂、相对分子质量最小的氧化物都是水。②最轻的气体是氢气(H2)。
8.用肥皂水检验硬水和软水:泡沫多为软水,泡沫少有白色垢状物的为硬水。
9.饱和溶液变不饱和溶液有两种方法:升温、加溶剂;[注意Ca(OH)2的特殊性]