- 264.50 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2018年郴州市初中学业水平考试试卷
一、选择题(共20小题,共40分,每小题只有一个选项符合题意)
1.水晶、沙子的主要成分都是SiO2, SiO2属于
A.酸 B.碱 C.盐 D.氧化物
2.中秋节吃月饼是我国的传统习俗,某品牌月饼的配料中富含蛋白质的是[,
A.白砂糖 B.小麦粉 C. 鲜鸡蛋 D.奶油
3.下列成语涉及物质化学变化的是
A. 大浪淘沙 B.花香四溢 C. 死灰复燃 D.水乳交融
4.空气中含量较多且常在焊接金属时作保护气的是
A.氧气 B.氮气 C. 水蒸气 D.二氧化碳
5. N2O俗称笑气,早期曾在外科手术中作麻醉剂。在N2O中,N元素的化合价是A. +1 B. +2 C. +3 D. +4
6.干冰易升华,在升华过程中,发生变化的是(
A.原子数目 B.分子数目 C.分子间隔 D.元素种类
7.下列溶液能使紫色石蕊溶液变红色的是加( )
A. NaCl溶液 B.澄清石灰水 C.稀盐酸 D. KNO3溶液
8.下列物质能造成“白色污染”的是
A.工业废水 B.地沟酒 C.废弃塑料 D.废弃电池
9.“药金”是锌和铜的合金,因外形似黄金而得名。下列厨房用品可用来鉴别“药金”为假黄金的是
A. 食盐水 B.白醋 C.料酒 D.酱油
10.下列实验操作正确的是
11.2018年世界水日的主题是“借自然之力,护绿水青山”下列有关水的说法正确的是
A.水是由氢气和氧气组成的 B.含可溶性钙、锁化合物较多的水叫做软水
C.冰水混合物是纯净物 D.油脂在水中乳化后形成溶液
选项
物质(括号内为杂质)
加入的除杂试剂及方法
A
H2(CO)
通过约热的氧化铜
B
CaO(CaCO3)
高温灼烧
C
Cu(CuO)
加适量稀盐酸、蒸发
D
NaCl(MgCl2)
加适量氧氧化钾溶液、过滤、蒸发
12.下列除杂方法正确的是
13.合理的饮食是健康身体的重要保障,下列说法错误的是[
A.我国是通过在食盐中加入碘的化合物来补碘
B.儿童缺锌会导致生长迟缓、发育不良
C.人体缺少维生素A易患夜盲症
D.绿色食品是指颜色为绿色的水果、蔬菜等
14.分别将一小烧杯浓盐酸、浓硫酸落置在空气中段时间后,发生的共同变化是
A.溶液的质量减小 B.溶液的浓度减小 C.溶质的质量减小D.溶剂的质量增大
15.下列关于氢氧化钠的描述中错误的是
A.俗名苛性钠、火破或烧碱 B.易溶于水,溶于水时吸收大量的热
C.氢氧化钠固体露置在空气中易变质
D.是重要的化工原料,广泛应用于肥皂、纺织、印染等工业
16.化学就在我们身边,人类的衣、食、住、行都离不开化学。下列说法正确的是
A.煤炉上放壶水能防止CO中毒 B.铝制品耐腐蚀是因为铝的化学性质不活泼
C.“火力发电”是利用了化学反应产生的能量 D.油锅着火,可用水灭火
17.下列离子组能大量共存的是
A.Cu2+、Na+、OH—、SO42— B. Ba2+、H+、Cl—、SO42—
C.K+ 、Ag+、 NO3—、C l— D. H+、Na+、SO42—、NO3—
18.下列关于溶液的说法正确的是
A.水是最常用的溶剂 B.饱和溶液定比不饱和溶液浓度大
C.澄清、透明的液体一定是溶液 D.饱和溶液定不能再继续溶解溶质
19.25℃时,下列过程的pH变化符合右图所示的是
A. NaOH溶液中滴加稀盐酸
B.稀盐酸中滴加NaOH溶液
C.一定浓度的NaOH溶液加水稀释
D.一定浓度的盐酸加水稀释
20. 9g碳与16g氧气在密闭容器中点燃,充分反应,生成CO2的质量是
A. 11g B. 22g C.25g D.33g
第一周期
1H
2He
第二周期
3Li
4Be
5B
6C
①
②
9F
10Ne
第三周期
11Na
12Mg
③
14Si
15P
16S
17Cl
18Ar
二、填空题(共4小题,共20分)
21. (5分)请用下列物质的序号填空:①天然气②小苏打③不锈钢④尿素⑤锦纶
(1)可作糕点发酵粉的是 (2)可作化学肥料的是
(3)属于合金的是 (4)属于合成纤维的是
(5)属于化石燃料的是
22.(4分)下图是
元素周期表的
一部分,试回
答下列问题:
(1)①所示元素是 (填“金属元素“或“非金属元素”);
(2)②所示元素与③所示元索形成的化合物的化学式是
(3)用化学符号表示: 2个镁离子 ,正四价的硅
23.(5分)甲、乙、丙三种物质在水中形成的饱和溶液溶质的质量分数随温度变化如下
图所示,请回答下列问题:
(1)25C时,甲物质的溶解度为 (答案保留一位小数);
(2)从乙溶液中获得乙晶体的方法是 (填“蒸发
结晶“或“降温结晶”);
(3)将50℃甲的饱和溶液降温至25℃,溶液为
(填“饱和溶液”或“不饱和溶液”);
(4)气体的溶解度随温度的变化规律与 (填甲”、
“乙”或“丙”)相似。
B
A
D
C
24.(6分)如右图所示:A、B、C、D分别为铁、稀盐酸、AgNO3
溶液和氧气中的一种,短线相连的两物质间均能发生反应,
且A与C反应后溶液的质量增加。请回答:
(1) C是
(2)A与D反应的化学方程式为
反应类型为
(3) Ag2O与 CuCl之间能发生类似于C与D反应类型的
反应,则Ag2O CuCl反应的化学方程式为
三、简箸题(共2小题,共15分)
25.(7分)(1)"84消毒液"是现在家庭中常用的消毒剂和漂白剂(能使酸碱指示剂等有机
色素褪色的物质),它的有效成分是NaClO。 84消毒液”属于 (填“纯
净物”或“混合物”).,该消毒液呈碱性,我们 (填“能”或“不能”)用pH
试纸来测此溶液的pH,原因是 (若
“能”则此空可不填)
(2)“84消毒液”制取原理为: Cl+2NaOH=NaClO+ X +H2O, 则X 的化学式
观察上述反应中物质及化合价变化的特点,硫与氢氧化纳溶液在加热条件下的反应
与此类似,请填出空白处物质的化学式: S+NaOH Na2SO3+ +H2O(未配平)
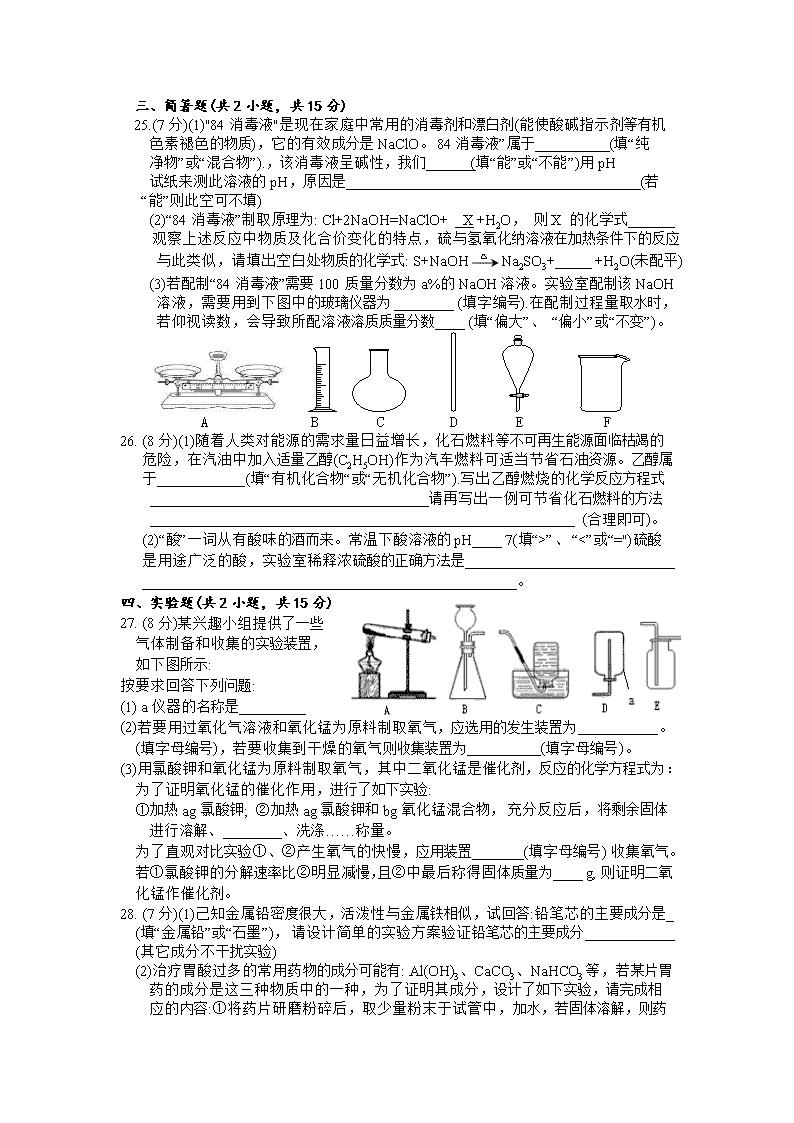
(3)若配制“84消毒液”需要100质量分数为a%的NaOH溶液。实验室配制该NaOH
溶液,需要用到下图中的玻璃仪器为 (填字编号).在配制过程量取水时,
若仰视读数,会导致所配溶液溶质质量分数____ (填“偏大”、 “偏小”或“不变”)。
A B C D E F
26. (8分)(1)随着人类对能源的需求量日益增长,化石燃料等不可再生能源面临枯竭的
危险,在汽油中加入适量乙醇(C2H5OH)作为汽车燃料可适当节省石油资源。乙醇属
于 (填“有机化合物“或“无机化合物”).写出乙醇燃烧的化学反应方程式
请再写出一例可节省化石燃料的方法
(合理即可)。
(2)“酸”一词从有酸味的酒而来。常温下酸溶液的pH____ 7(填“>”、 “<”或“=")硫酸
是用途广泛的酸,实验室稀释浓硫酸的正确方法是
。
四、实验题(共2小题,共15分)
27. (8分)某兴趣小组提供了一些
气体制备和收集的实验装置,
如下图所示:
按要求回答下列问题:
(1) a仪器的名称是
(2)若要用过氧化气溶液和氧化锰为原料制取氧气,应选用的发生装置为 。
(填字母编号),若要收集到干燥的氧气则收集装置为 (填字母编号)。
(3)用氯酸钾和氧化锰为原料制取氧气,其中二氧化锰是催化剂,反应的化学方程式为: 为了证明氧化锰的催化作用,进行了如下实验:
①加热ag氯酸钾; ②加热ag氯酸钾和bg氧化锰混合物, 充分反应后,将剩余固体
进行溶解、 、洗涤……称量。
为了直观对比实验①、②产生氧气的快慢,应用装置 (填字母编号) 收集氧气。若①氯酸钾的分解速率比②明显减慢,且②中最后称得固体质量为____ g, 则证明二氧化锰作催化剂。
28. (7分)(1)己知金属铅密度很大,活泼性与金属铁相似,试回答:铅笔芯的主要成分是_ (填“金属铅”或“石墨”), 请设计简单的实验方案验证铅笔芯的主要成分_ (其它成分不干扰实验)
(2)治疗胃酸过多的常用药物的成分可能有: Al(OH)3、CaCO3、NaHCO3等,若某片胃
药的成分是这三种物质中的一种,为了证明其成分,设计了如下实验,请完成相
应的内容:①将药片研磨粉碎后,取少量粉末于试管中,加水,若固体溶解,则药
品成分为_ (填化学式);
②若①中固体不溶解,再向试管中滴加稀盐酸,固体溶解,且有气泡产生,则药
品成分为 (填化学式),此过程反应的化学方程式为
五、计算题(共2小题,共10分)
29. (5分)维生素C (C6H8Ox) 主要存在于蔬菜、水果中,它能促进人体生长发育,增
强人体对疾病的抵抗力,其相对分子质量为176。试计算:
(1)维生素C中氢元素的质量分数为 (结果精确到0.1%); (2) x=
加入锌粉的质量/g
7.0
14.0
21.0
28.0
35.0
42.0
溶液的质量/g
188.8
195.1
a
207.7
214.0
214.0
(3)维生素C中C、H、O三种元素的质量比为
30.(5分)向182.5g
定浓度的盐酸中
加入一 定量的锌粉
(杂质不溶于水也不与盐酸反应)加入锌粉的质量与溶液质量变化如上表所示:
分析数据:试计算【第2问需写出计算过程】
(1)a= (2)盐酸中溶质的质量分数?
六、综合题(共1小题,共10分)
31. 用某含有CO2、水蒸气的还原性气体(可能含有CO、H2中的一种或两种)经过如下
图的装置来确定其成分及C装置中FexOy的化学式。
(1) B装置的作用是 D装置的作用是 _
(2)实验过程中观察到D中无明显变化,E中澄清石灰水变浑浊,则还原性气体是
当C中的FexOy完全反应后,测得E和F的总质量增加3.52g, C中剩余
固体质量为3.36g.则FexOy的化学式为 . 若没有A装置,则测得的x和
y的比值将 (填“偏大”、“偏小”或“不变”)。
上述实验中生成的二氧化碳用氢氧化钠溶液吸收,某工厂也利用此原理吸收生
产中排放的二氧化碳,再通过一定的方法将二氧化碳释放、储存达到回收再利用
吸收池
CO2含量低的气体
CO2含量高的气体
分离池
煅烧窑
CO2储存再利用
B溶液
产物CaO
的目的,具体流程如下(部分反应条件和试剂未标出):
根据上图回答下列问题:
(3)分离池中发生的化学反应方程式为 、
(4) B为 (填化学式);
(5)“人类只有一个地球!”防止温室效应的根本对策是全球参与控制 氧化碳的排放量,
“低碳生活从我做起”。请举出一例“低碳”生活的例子 (合理即可)。