- 576.50 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
中考工业流程题练习
一、海水资源的多重利用
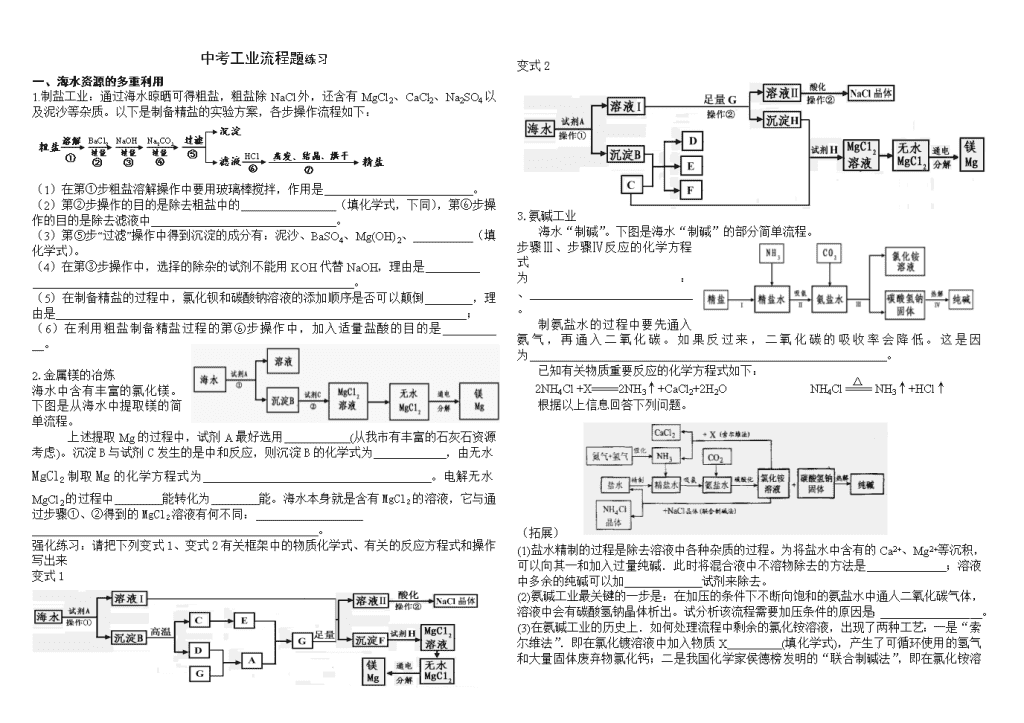
1.制盐工业:通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、 (填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
。
(5)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒________,理由是_____________________________________________________________________;
(6)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_________ __。
2.金属镁的冶炼
海水中含有丰富的氯化镁。下图是从海水中提取镁的简单流程。
上述提取Mg的过程中,试剂A最好选用 (从我市有丰富的石灰石资源考虑)。沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为 ,由无水MgCl2制取Mg的化学方程式为 。电解无水MgCl2的过程中 能转化为 能。海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:
。
强化练习:请把下列变式1、变式2有关框架中的物质化学式、有关的反应方程式和操作写出来
变式1
变式2
3.氨碱工业
海水“制碱”。下图是海水“制碱”的部分简单流程。
步骤Ⅲ、步骤Ⅳ反应的化学方程式为: 、 。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为 。
△
已知有关物质重要反应的化学方程式如下:
2NH4Cl +X====2NH3↑+CaCl2+2H2O NH4Cl ==== NH3↑+HCl↑
根据以上信息回答下列问题。
(拓展)
(1)盐水精制的过程是除去溶液中各种杂质的过程。为将盐水中含有的Ca2+、Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合液中不溶物除去的方法是 ;溶液中多余的纯碱可以加 试剂来除去。
(2)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通人二氧化碳气体,溶液中会有碳酸氢钠晶体析出。试分析该流程需要加压条件的原因是:_______________ 。
(3)在氨碱工业的历史上.如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”.即在氯化镀溶液中加入物质X (填化学式),产生了可循环使用的氢气和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”
,即在氯化铵溶液中加入适量氯化钠晶体.降低了氯化氨的 ,使氯化铵晶体单独析出得到另一种产品——氮肥.氯化钠溶液则可以循环利用。
(4)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体?
答: 。
二、传统能源工业(化石燃料的利用、及合成氨工业等)
1、煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。请回答下列问题:(1)下列说法正确的是 。
A.煤是复杂的混合物,主要含碳元素
B.由煤加工成焦炭发生的是物理变化
C.家用“液化石油气”就是煤隔绝空气加热得到的产品
D.煤燃烧排放的二氧化硫、二氧化氮是形成酸雨的主要物质
(2)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。
右图是高炉炼铁的示意图。请根据图例回答:
①焦炭在炼铁过程中的主要作用是 ;
②请用化学方程式表示炼铁的原理 ;
③高炉炼铁会产生大量的高炉气体,其主要成分是高浓度的CO和氧化铁尘粒。请你对高炉气体的处理提出合理化的建议 。
煤气发生炉
碳化塔
合成塔
液氨储槽
煤、空气、水
CO2、H2、N 2
H2、N 2
水
煤气发生炉
碳化塔
合成塔
液氨储槽
煤、空气、水
CO2、H2、N 2
H2、N 2
水
(3)化肥厂生产合成氨的原料是煤、空气、水。生产简要流程如下:
煤气发生炉中主要反应:① C + O2 = CO2;② C + H2O = CO + H2。两个反应必须进行调控才能保持一定的炉温。判断:反应② (填“放出”或“吸收”)热量。
将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH4HCO3,试写出该反应的化学方程式 。
三、石灰石工业
1、用作牙膏摩擦剂的轻质碳酸钙可以用矿石A来制备,某化学兴趣小组设计了2种转化流程,如下图所示。
已知:a.二氧化碳持续通入氢氧化钙溶液发生如下反应:
CO2+Ca(OH)2===CaCO3↓+H2O, CaCO3+ H2O + CO2===Ca(HCO3)2;
微热
b.碳酸氢钙微溶于水,微热易分解:
Ca(HCO3)2===== CaCO3↓+H2O+ CO2↑;
c.生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
(1)小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单。
请写出反应①和④的化学方程式:
① ;④ ;
操作Ⅱ包括 等工序。
(2)制轻质碳酸钙时,D为 (选填“悬浊液”或“溶液”或“乳浊液”),
理由是: .
(3)小李认为流程①、②、③和操作I比小王的主张更好,其理由是:_______________
;操作I包括搅拌和微热等工序。
四、污水处理工业
1、有一种工业废水,其中含有大量的硫酸亚铁,少量的银离子以及污泥。某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体。方案流程如下:
④
③
①
②
工业
废水
污泥
溶液1
固体
溶液2
Ag
溶液3
硫酸亚铁晶体
回答下列问题:
(1)步骤②中:需加入的物质是 ,分离所得混合物的方法是
。
(2)步骤③中:需加入的物质是 ,发生反应的化学方程式是
。
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理? ,理由是 .
(4)步骤④的操作是 ,溶液2和溶液3为什么要混合? .
五、金属回收工业
1、坐落于常熟的江苏常福电缆厂是一家以生产电缆类产品为主的企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
甲同学根据已学知识,提出了一套回收方案:
乙同学在查阅资料后得知:在通入空气并加热的务件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O22CuSO4+2H2O),于是他提出了另一套方案:
(1)甲方案的②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
② ;③ .
(2)从环保角度对两套方案的不同部分进行比较,你认为 (选填“甲”或“乙”)的方案更合理.理由是: .
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是: .
丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该用什么化学方法
处理?”请提出你的想法: .
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶的两种可能方法: 、 (“绿矾”溶解度随温度升高而增大).
同步练习
1、由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。下图是粗盐精制的流程:
回答下列问题:
(1) 操作的名称是 。
(2) 在悬浊液中加NaOH溶液、Na2CO3溶液、BaCl2溶液三种试剂的顺序合理的为 。
A、先加入NaOH,后加入Na2CO3,再加入BaCl2溶液
B、先加入NaOH,后加入BaCl2溶液,再加入Na2CO3
C、先加入BaCl2溶液,后加入NaOH,再加入Na2CO3
D、先加入BaCl2溶液,后加入Na2CO3,再加入NaOH
有同学提出用 溶液代替BaCl2溶液可达到同样的目的。
2、久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分。 溶液C
固体B
溶液变红
操作①
样品
浊液
(烧杯壁发热)
溶液A
固体B
浊液
加入
足量水
操作①
加入过量
CaCl2溶液
加入
酚酞
取样品进行以下探究:
试回答下列问题:
(1)操作①的名称是_________,溶液C中一定含_________离子。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有_________,反应的方程式_____________
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是_________ 。
3、医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~103.0%)的主要流程如下:
(1)写出①处化学反应方程式 。
(2)酸化操作加入盐酸的作用是 (写一点)。
(3)②处的操作名称是 。
(4)滤渣③成分的化学式 。
(5)若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 (写一点).
答案
1.制盐工业答案:(1)加快粗盐溶解 (2)Na2SO4 NaOH、Na2CO3 (3)CaCO3、BaCO3
(4)会引进新的杂质KCl (5)不可以。碳酸钠作用是既除去Ca2+,又除去多余的氯化钡
(6)除去多余的氢氧化钠和碳酸钠
2、 Mg(OH)2 MgCl2 通电 Mg+Cl2↑ 后者是经过富集和分离后的溶液(或海水中含有氯化钠等多种溶质,氯化镁的浓度很低)
3、 NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl 2NaHCO3△ Na2CO3+ H2O+CO2↑ 氨气溶于水形成碱性溶液,更易于吸收二氧化碳
(拓展)(1)过滤 盐酸 (2)促进更多CO2溶解反应充分 (3)Ca(OH)2 溶解度(4)氯化铵受热易分解
高温
二、传统能源工业
(1)AD(2)①制取CO、提供热量②Fe2O3 + 3CO 2Fe + 3CO2③回收利用
(3)吸收 CO2 + NH3 + H2O = NH4HCO3
三、石灰石工业
四、污水处理工业(1).Fe 过滤
(2).稀硫酸 Fe+H2SO4=FeSO4+H2 ↑
(3).不合理 因为要使Ag+ 完全置换出来,必须加入过量的铁
(4).两种滤液中都含有硫酸亚铁,可得到更多的硫酸亚铁,综合利用
(其他合理答案也可)
五、金属回收工业
NaCl晶体③C D E F G H I J