- 463.50 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2018河南中考化学模拟试卷二
(限时:50分钟 总分:50分)
相对原子质量 H:1 C:12 O:16 Na:23 Mg:24 Si:28 S:32 Cl:35.5 Ca:40 Ag:108
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
1.下列日常生活中的变化,属于物理变化的是( )
A.火药爆炸 B.面包发霉
C.葡萄酿酒 D.酒精挥发
2.鲁山揽锅菜营养美味,它用到的下列食材中富含维生素的是( )
A.猪肉 B.粉条
C.青菜 D.花生油
3.以下不属于空气污染物的是( )
A.CO2 B.可吸入颗粒物
C.SO2 D.氮氧化合物
4.下列各组物质,按化合物、混合物顺序排列的是( )
A.豆浆、冰水共存物 B.铝箔、石油
C.一氧化氮、牛奶 D.二氧化硫、氢氧化铝
5.下列实验现象描述不正确的是( )
A.磷在空气中燃烧,产生大量白烟
B.打开浓盐酸的试剂瓶盖,瓶口会出现白雾
C.硫在氧气中燃烧时,发出蓝紫色的火焰,生成了一种无色无味的气体
D.氢气燃烧时,罩在火焰上方的冷而干燥的烧杯内壁出现无色液滴
6.化学与生活息息相关,下列做法不合理的是( )
A.氧气用于医疗急救
B.用白醋除去热水瓶中的水垢
C.可用肥皂水鉴别硬水和软水
D.用甲醛的水溶液浸泡海产品,防腐保鲜
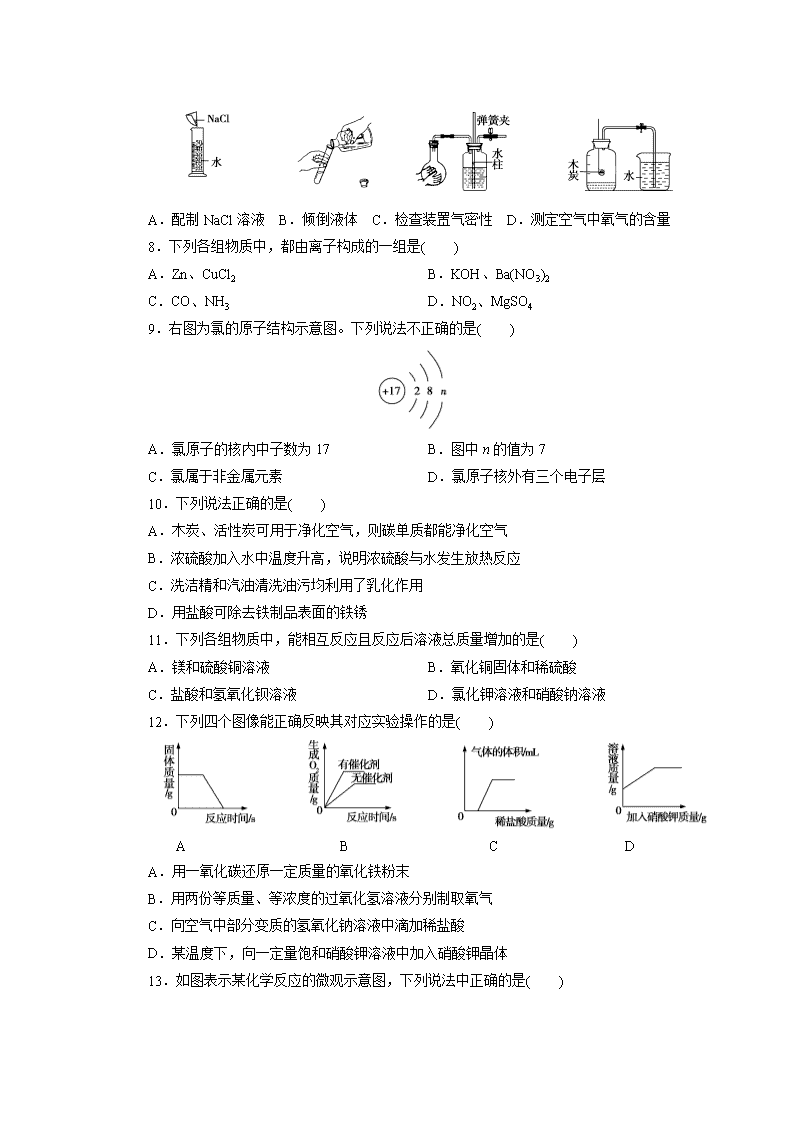
7.下列图示的实验操作中正确的是( )
A.配制NaCl溶液 B.倾倒液体 C.检查装置气密性 D.测定空气中氧气的含量
8.下列各组物质中,都由离子构成的一组是( )
A.Zn、CuCl2 B.KOH、Ba(NO3)2
C.CO、NH3 D.NO2、MgSO4
9.右图为氯的原子结构示意图。下列说法不正确的是( )
A.氯原子的核内中子数为17 B.图中n的值为7
C.氯属于非金属元素 D.氯原子核外有三个电子层
10.下列说法正确的是( )
A.木炭、活性炭可用于净化空气,则碳单质都能净化空气
B.浓硫酸加入水中温度升高,说明浓硫酸与水发生放热反应
C.洗洁精和汽油清洗油污均利用了乳化作用
D.用盐酸可除去铁制品表面的铁锈
11.下列各组物质中,能相互反应且反应后溶液总质量增加的是( )
A.镁和硫酸铜溶液 B.氧化铜固体和稀硫酸
C.盐酸和氢氧化钡溶液 D.氯化钾溶液和硝酸钠溶液
12.下列四个图像能正确反映其对应实验操作的是( )
A B C D
A.用一氧化碳还原一定质量的氧化铁粉末
B.用两份等质量、等浓度的过氧化氢溶液分别制取氧气
C.向空气中部分变质的氢氧化钠溶液中滴加稀盐酸
D.某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
13.如图表示某化学反应的微观示意图,下列说法中正确的是( )
A.该反应属于复分解反应
B.该反应中只有一种单质
C.图示物质中相对分子质量最小的是H2
D.生成丙和丁的质量比为1∶4
14.取Mg和MgO的混合物6.4 g,与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24 g。则原混合物中氧元素的质量为( )
A.1.6 g B.2.56 g
C.3.2 g D.4.8 g
二、填空题(本题包括6个小题,每空1分,共16分)
15.“烧烤”是一种街头美食。烧烤时远远就能闻到诱人的香味,从微观角度解释其原因是____________________________________________;烧烤的过程中,食物焦化易产生致癌苯并芘(化学式为C20H12),苯并芘中碳元素与氢元素的质量比为__________。
16.近年来,国家加大了对醉酒驾驶的处罚力度。交警通常用一种“酒精检测仪”检查司机呼出气体中酒精的含量,其反应原理为:C2H5OH+4CrO3+6H2SO4=== 2Cr2(SO4)3+2X↑+9H2O,反应中红色的CrO3转变为绿色的Cr2(SO4)3,则X的化学式为__________,CrO3中Cr元素的化合价为__________。
17.“美丽乡村”建设是精准扶贫的民心工程,在农村推广家用沼气池建设是改善农村能源结构和环境卫生的重要举措。沼气的主要成分是甲烷,其完全燃烧的化学方程式为____________________________。在炒菜时,不小心油锅着火了,迅速向锅内加入大量青菜灭火,其灭火原理是________________________________________________;在菜快熟的时候加入了铁强化酱油,这种酱油中的铁元素可以预防的疾病是__________________。
18.下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃
0
20
40
60
80
100
溶解度/g
Ca(OH)2
0.19
0.17
0.14
0.12
0.09
0.08
NaOH
31
91
111
129
313
336
20 ℃时,将191 g NaOH的饱和溶液稀释为质量分数为20%的溶液,需加水__________g;现有60 ℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是__________________________。现有20 ℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20 ℃,得到乙溶液,溶液中溶质质量的关系为甲__________(填“>”“<”或“=”)乙。
19.我国自行研发的大型客机C919于2017年5月成功试飞,
飞机所用的材料包括塑料扶手、 纯羊毛毯、真皮座套和铜制扣件等。其材料中由有机合成材料制成的是__________;选用铝合金做飞机机身而不选用纯铝,主要原因是__________________________________;飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与____________________接触。
20.A、B、C、D是初中化学中常见的物质,其中A是胃酸的主要成分,B在农业上常用于改良酸性土壤,D常温下为液体。A、B、C、D的物质类别不相同,它们相互反应及转化关系如图所示(“→”表示由一种物质可以转化为另一种物质,“-”表示相邻的物质间可以相互反应,其中部分反应物和生成物及反应条件已略去)。请回答:
(1)D物质是__________。
(2)写出B→C反应的化学方程式________________________________________。
(3)写出A与B反应的化学方程式________________________________________。
三、简答题(本题包括4个小题,共10分)
21.(2分)用化学方程式表示下列反应原理。
(1)在 440 ℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠。
(2)将氧化铜粉末置于试管中加热、通入氨气,生成铜、水和一种气体单质。
22.(2分)“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请回答下列问题:
(1)实验1中,观察到铜片上的白磷燃烧而水中的白磷不燃烧,可得出可燃物燃烧的一个条件是什么?
(2)实验2中,对比两支试管内液面高低的不同,可说明氢氧化钠能与二氧化碳发生反应,写出反应的化学方程式。
23.(3分)如图所示为实验室中常见的气体制备和收集装置。
(1)实验室制取CO2应选用的一套装置为__________(填字母代号);写出该反应的化学方程式________________________________。
(2)D装置有多种用途,可以作为集气瓶收集氧气,请写出用D装置收集氧气的验满方法。
24.(3分)在Cu(NO3)2、Zn(NO3)2和AgNO3的混合液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液。
(1)滤液中一定含有的溶质有________________(写化学式)。
(2)若向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质有________________(写化学式)。
(3)写出一个上述可能发生反应的化学方程式。
三、综合应用题(共10分)
25.酸、碱、盐是中学化学学习和研究的重要内容。
(1)某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,烧杯中溶液pH的变化图像如图所示。图中a点溶液中含有的溶质是____________________。
(2)采用氨碱法生产纯碱,主要流程如图:
①写出步骤Ⅲ中发生反应的化学方程式__________________________________。
②对步骤Ⅱ过滤后的滤液处理后可获得铵态氮肥NH4Cl。检验铵态氮肥的方法是
________________________________________________________________________
________________________________________________________________________。
(3)蒸发海水得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
①步骤②玻璃棒的作用是______________________________。
②写出加入NaOH发生反应的化学方程式______________________________。
③加入过量Na2CO3溶液的目的是__________________________________________,溶液B中含有的溶质有______________________。
(4)小明取上述制得的精盐5 g配制成溶液,向其中加硝酸银溶液100 g,恰好完全反应,过滤得到沉淀11.48 g。试计算精盐中氯化钠的质量分数。
参考答案:
一、选择题(每小题1分,共14分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
D
C
A
C
C
D
C
B
A
D
B
C
C
A
二、填空题(每空1分,共16分)
15.分子在不断地运动,使香味扩散 20∶1
16.CO2 +6
17.CH4+2O2 CO2+2H2O 降低温度至着火点以下 缺铁性贫血
18.264 冷却热饱和溶液 >
19.塑料扶手 铝合金的硬度和强度大于纯铝 氧气和水
20.(1)水(或H2O)
(2)Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH(合理即可)
(3)2HCl+Ca(OH)2=== CaCl2+2H2O
三、简答题(共10分)
21.(1)4Na+3CO2 2Na2CO3+C (1分)
(2)3CuO+2NH3 3Cu+3H2O+N2 (1分)
22.(1)需要与空气接触。 (1分)
(2)2NaOH+CO2=== Na2CO3+H2O (1分)
23.(1)BC或BD (1分) CaCO3+2HCl=== CaCl2+H2O+CO2↑ (1分)
(2)将带火星的木条放在b处,若木条复燃,则证明收集满了 (1分)
24.(1)Mg(NO3)2 (1分) (2)Cu、Zn、Ag (1分)
(3)Mg+Cu(NO3)2=== Mg(NO3)2+Cu
或Mg+Zn(NO3)2=== Mg(NO3)2+Zn (1分)
四、综合应用题(共10分)
25.(1)氢氧化钠和硫酸钠(或NaOH、Na2SO4) (1分)
(2)①2NaHCO3 Na2CO3+H2O+CO2↑ (1分)
②取少量样品于试管中,加氢氧化钠溶液混合加热能放出有刺激性气味气体,在试管口放一湿润的红色石蕊试纸,如果试纸变蓝,说明是铵态氮肥 (1分)
(3)①引流 (1分)
②MgCl2+2NaOH=== Mg(OH)2↓+2NaCl (1分)
③除去氯化钙和过量的氯化钡 (1分) 氯化钠、氢氧化钠、碳酸钠 (1分)
(4)解:设精盐中NaCl的质量为x。
NaCl+AgNO3=== AgCl↓+NaNO3 (1分)
58.5 143.5
x 11.48 g
=,x=4.68 g (1分)
精盐中NaCl的质量分数=×100%=93.6% (1分)
答:精盐中氯化钠的质量分数为93.6%。