- 656.50 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
姓名
班级
考点 必考8个小实验
【考 纲 解 读】
考点概况
1.粗盐中难溶性杂质的去除。 2.氧气的实验室制取与性质。
3.二氧化碳的实验室制取与性质。 4.金属的物理性质和某些化学性质。
5.燃烧的条件。 6.一定溶质质量分数的氯化钠溶液的配制。
7.溶液酸碱性的检验。 8.酸碱的化学性质。
命题把握
能力要求:
1.初步学习使用过滤、蒸发的方法对混合物进行分离。通过粗盐提纯实验,进一步掌握溶解、过滤、蒸发等基本操作。能独立完成粗盐中难溶性杂质去除的实验。
2.学习组装不同的制取氧气的实验装置,并能制取和收集氧气。通过木炭、硫、铁丝、蜡烛分别在氧气中燃烧的实验,认识氧气的性质。
3.学习组装石灰石(或大理石)与盐酸反应制取二氧化碳的装置,并能制取和收集二氧化碳。通过实验探究二氧化碳的性质。
4.通过验证金属活动性顺序的探究,学会设计验证实验的一般思路与方法,能对比较金属活动性强弱的实验方案做出分析与评价。
5.通过实验加深对物质燃烧条件的认识,进一步了解灭火的原理。能通过相关实验条件的对比得出物质燃烧的条件。熟练应用对比实验法和控制变量法设计物质燃烧条件的测定实验,并通过实验探究得出物质燃烧条件的结论。
6.明确配制一定溶质质量分数的溶液的一般步骤。学会配制一定溶质质量分数的溶液。进一步熟悉天平、量筒的使用,熟悉溶解的操作。
7.初步学会用酸碱指示剂、pH试纸检验溶液的酸碱性。通过对酸、碱化学性质实验的操作,加深对酸、碱化学性质的认识。
命题角度:
1.实验过程中的仪器、操作步骤及注意事项。
2.实验过程中导致误差原因。
3.实验原理、操作步骤、现象及注意事项。
4.考查粗盐中难溶性杂质的去除。
5.食盐中可溶性杂质的去除。
指点迷津
1.把握目的要求。2.确定原理方法。3.选择器材4.设计实验步骤
【核 心 题 组 训 练】
【一、粗盐中难溶性杂质的去除】
1.(2019·淄博)海水“晒盐”得到的是粗盐,粗盐提纯的步骤可简单的概括为:溶解—过滤—蒸发,下列说法错误的是( )
A.实验前需要查阅资料,了解食盐在室温时的溶解度
B.粗盐若未能充分溶解,则实验结果中食盐的含量将偏低
C.过滤后得到的滤渣是粗盐中的难溶性杂质
D.蒸发时需将滤液全部蒸干再停止加热
2.(2019·黑龙江)在粗盐提纯的实验操作中,下列说法正确的是( )
A.过滤时用到的仪器有烧杯、玻璃棒、铁架台、滤纸
B.蒸发操作结束后,将蒸发皿放在石棉网上
C.用药匙将蒸发皿中的白色固体直接转移到纸上
D.实验结束后所得到的白色固体为氯化钠
3.(2019·邵阳)在“粗盐中难溶性杂质的去除”实验中,操作步骤为溶解、过滤、蒸发、计算产率。这四步操作中均要用到的一种仪器是( )
A.烧杯 B.漏斗 C.玻璃棒 D.酒精灯
4.(2019·河南)除去食盐水中的CaCl2和Na2SO4杂质的操作有:①加过量的BaCl2溶液;②过滤;③加过量的Na2CO3溶液;④蒸发结晶;⑤加适量盐酸。下列操作顺序正确的是(提示BaSO4、BaCO3难溶于水)( )
A.③①②⑤④ B.①⑤③②④ C.①③⑤④② D.①③②⑤④
5.(2019·宁波)在粗盐提纯的实验中,下列操作正确的是( )
A.粗盐称量 B.粗盐溶解 C.浊液过滤 D.蒸发结晶.
6.(2019·南昌)下列是“粗盐中难溶性物质去除”的实验操作示意图:
A.称取5.0g粗盐 B.量取10 mL水 C.过滤 D.蒸发
a
粗盐
5 g
(1)仪器a的名称______________;
(2)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是____________________;
(3)操作B中还需用到的仪器是__________;
(4)操作C中,倒入液体时液面要低于滤纸边缘主要是为了防止_______(填序号)。
A.过滤速度慢 B.滤纸破损 C.杂质未经过滤就进入滤液
(5)操作C完成后滤液中还含有少量的氯化钙,写出除去氯化钙的化学方程式
________________________________________________________________;
(6)图中部分操作有错误,其中会导致精盐产率明显偏低的操作编号是___________,说明引起偏低的理由
________________________________________________________________。
【二、氧气的实验室制取与性质】
1.在进行“氧气的实验室制取与性质”实验时,某同学制得的氧气不纯。你认为可能的原因是( )
A.用排水法收集时O2,集气瓶装满水
B.用向上排空气法收集O2时,导管伸入到集气瓶的底部
C.用排水法收集O2时,导管口冒出气泡,立即收集
D.用排水法收集O2,收集满后,在水下盖上玻璃片
2.(2019·南通)用KMnO4制取O2并回收MnO2,下列操作或装置不正确的是( )
A.制取O2 B.收集O2 C.产物加水搅拌 D.过滤得MnO2
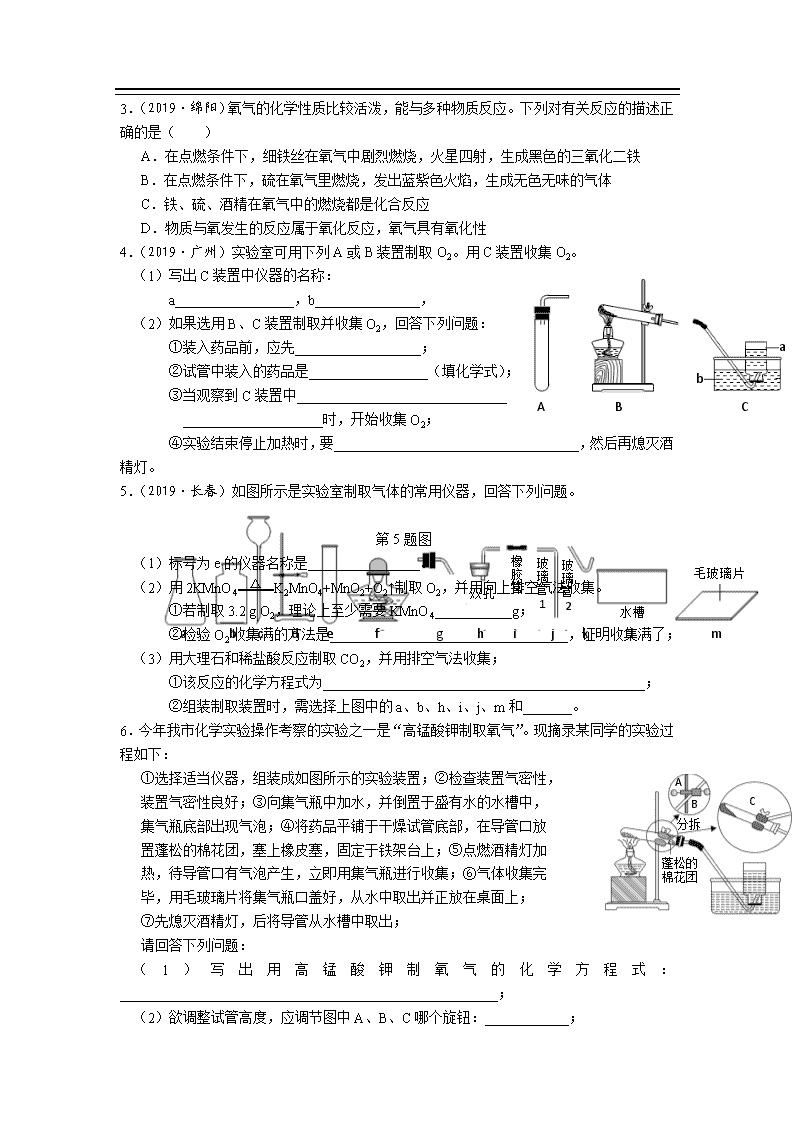
3.(2019·绵阳)氧气的化学性质比较活泼,能与多种物质反应。下列对有关反应的描述正确的是( )
A.在点燃条件下,细铁丝在氧气中剧烈燃烧,火星四射,生成黑色的三氧化二铁
B.在点燃条件下,硫在氧气里燃烧,发出蓝紫色火焰,生成无色无味的气体
C.铁、硫、酒精在氧气中的燃烧都是化合反应
D.物质与氧发生的反应属于氧化反应,氧气具有氧化性
4.(2019·广州)实验室可用下列A或B装置制取O2。用C装置收集O2。
a
b
A B C
(1)写出C装置中仪器的名称:
a_________________,b_______________,
(2)如果选用B、C装置制取并收集O2,回答下列问题:
①装入药品前,应先__________________;
②试管中装入的药品是_________________(填化学式);
③当观察到C装置中______________________________
____________________时,开始收集O2;
④实验结束停止加热时,要___________________________________,然后再熄灭酒精灯。
5.(2019·长春)如图所示是实验室制取气体的常用仪器,回答下列问题。
a b c d e f g h i j k l m
双孔
毛玻璃片
水槽
玻璃管1
2
玻璃管2
橡胶管
第5题图
(1)标号为e的仪器名称是________________。
(2)用2KMnO4 △ K2MnO4+MnO2+O2↑制取O2,并用向上排空气法收集。
①若制取3.2 g O2,理论上至少需要KMnO4___________g;
②检验O2收集满的方法是__________________________________,证明收集满了;
(3)用大理石和稀盐酸反应制取CO2,并用排空气法收集;
①该反应的化学方程式为______________________________________________;
②组装制取装置时,需选择上图中的a、b、h、i、j、m和_______。
6.今年我市化学实验操作考察的实验之一是“高锰酸钾制取氧气”。现摘录某同学的实验过程如下:
蓬松的
棉花团
分拆
A
B
C
①选择适当仪器,组装成如图所示的实验装置;②检查装置气密性,
装置气密性良好;③向集气瓶中加水,并倒置于盛有水的水槽中,
集气瓶底部出现气泡;④将药品平铺于干燥试管底部,在导管口放
置蓬松的棉花团,塞上橡皮塞,固定于铁架台上;⑤点燃酒精灯加
热,待导管口有气泡产生,立即用集气瓶进行收集;⑥气体收集完
毕,用毛玻璃片将集气瓶口盖好,从水中取出并正放在桌面上;
⑦先熄灭酒精灯,后将导管从水槽中取出;
请回答下列问题:
(1)写出用高锰酸钾制氧气的化学方程式:______________________________________________________;
(2)欲调整试管高度,应调节图中A、B、C哪个旋钮:____________;
(3)步骤②的操作与观察到的现象是:__________________________________________________________;
若装置无破损,加热一段时间后,观察到高锰酸钾已大量分解,但导管口仍未产生明显气泡,可能的原
因是_________________________________________________________;
(4)上述实验步骤中,可能导致集气瓶中收集的氧气不纯净(水蒸气不计)的是____________;(填序号)
(5)步骤⑦中的操作,可能引起_____________________________。
【三、二氧化碳的实验室制取与性质】
1.(2019·重庆)甲、乙两同学在实验室制取CO2和O2时,无论选择什么药品,他们都能选用的装置是( )
A B C D
① ② ③ ④
第2题图
a
b
浓硫酸
燃着的
木条
2.(2019·泰安)下列有关实验室制取气体的说法错误的是( )
A.装置①可作为CO2的发生装置
B.装置②干燥O2时,气体由a管进b管出
C.装置③可用作O2的收集装置
D.装置④是收集CO2气体的验满方法
3.(2019·南宁)下列有关二氧化碳的说法正确的是( )
A.实验室常用块状石灰石和稀硫酸反应制取二氧化碳气体
B.二氧化碳用于人工灭火,既利用了它的物理性质也利用了它的化学性质
C.将二氧化碳气体通入紫色石蕊试液中,溶液呈红色,说明二氧化碳显酸性
D.将燃着的木条伸入一瓶气体中,木条立即熄灭,证明瓶内原有气体就是二氧化碳
A B C D E F G
第4题图
a
4.(2019·梅州)某学习小组利用如图仪器或装置进行气体制备,回答有关问题:
(1)写出仪器a的名称___________,用A装置制取氧气的化学反应方程式为:_______________________。
(2)若要在实验室制取二氧化碳气体,其发生装置可选用图中的______(填序号)进行组装,连接玻璃管和胶皮管的操作:先把玻璃管口__________,然后稍稍用力即可把玻璃管插入胶皮管内。
(3)要制的干燥的二氧化碳,可在收集装置前增加盛有_______的洗气瓶。
(4)实验室收集氧气和二氧化碳都可用到的装置是______(填序号)。
(5)用澄清石灰水检验二氧化碳,其反应的化学方程式为:_______________________________________。
5.(2019·宜宾)化学是一门以实验为基础的科学。请根据下列仪器和实验装置回答有关问题:
① ② ③ ④ ⑤ ⑥
第5题图
双孔
盐酸
CO2
氢氧化
钠溶液
气球
玻
璃
管
(1)仪器②的名称是_______________。
(2)用①②③组合可制备CO2,写出实验室用此装置制备CO2的化学方程式:________________________。
(3)收集CO2应选用装置__________(填“④”或“⑤”)。
⑥ ⑦ ⑧ ⑨ ⑩ ⑾
① ② ③ ④ ⑤
火柴
第6题图
(4)利用如图⑥所示装置(集气瓶中预先装满CO2气体)来验证CO2的性质,先加入足量氢氧化钠溶液,观察到的现象是气球____________(填“变大”、“变小”或“不变”)。反应方程式为_______________________________;再加入足量盐酸,观察到的现象是气球__________(填“变大”、“变小”或“不变”)。
6.(2019·钦州)在化学实验操作技能考查中有三道考题:
a.氧气的实验室制取与性质;
b.二氧化碳的制取、收集和验满;
c.粗盐中难溶性杂质的去除。
小宇抽签后由监考老师引领至实验桌前,该实验桌上
摆放了如下药品和仪器。回答下列问题:
(1)图中所示仪器③和⑤的名称是:
③________________________________,
⑤________________________________。
(2)小宇进行的考题是_______(填序号),其主要操作如图所示:
火柴熄灭
A.加入药品 B.检查装置气密性 C.气体验满 D.收集气体 E.洗涤仪器,整理桌面
其中操作错误的是_______(填序号);改正该错误操作后,小宇完成实验的正确操作顺序应为_____________________(填序号)。
(3)C操作利用了该气体____________________________的化学性质。
(4)实验桌上的两种药品所发生反应的化学方程式为:_____________________________________________。
【四、金属的物理性质和某些化学性质】
1.(2019·揭阳)金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是( )
A.硬度很大、熔点很高 B.是银白色的固体
C.易与酸反应产生氢气 D.能够导电、能够导热
2.(2019·广州)下列有关金属的说法正确的是( )
A.铝元素在地壳中含量最多,使用也最早 B.不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C.灯泡里的灯丝常用钨制成 D.地球上金属矿物资源储量有限,可再生
3.(2019·株洲)下列有关金属及合金的说法中正确的是( )
A.合金是由两种或两种以上金属熔合而成的具有金属特性的物质
B.在日常生活中,大量使用的常常不是纯金属,而是它们的合金
C.“真金不怕火炼”说明黄金的硬度非常大
D.铜的化学性质不活泼,所以铜制品不会生锈
4.(2019·菏泽)某化学小组向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn
粉,充分反应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是( )
A.Zn(NO3)2、AgNO3 B.Zn(NO3)2、Cu(NO3)2、AgNO3
金属与盐酸反应
盐酸
Mg
Zn
Fe
Cu
第5题图
C.Zn(NO3)2、Cu(NO3)2 D.Zn(NO3)2
5.(2019·成都)金属与盐酸的反应的示意图如图所示,下列说法正确的是( )
A.实验室可用铜和稀盐酸制氢气
B.四种金属中活动性最强的是镁
C.铁可以把锌从硫酸锌溶液中置换出来
D.铁与稀盐酸反应的化学方程式为:2Fe+6HCl 2FeCl3+3H2↑
6.(2016·贺州)金属在日常生活中有着广泛的用途,常见金属的活动性顺序如图:
K Ca Na Mg Al Zn Fe Se Pb (H) Cu (X) Ag Pt Au
金属活动性由强逐渐减弱
.
第6题图
A
B
C
时间/s
溶
液
质
量
/g
请回答下面问题:
(1)金属活动性顺序表中的X是_______元素。
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过了一会儿,观察到
的现象有_______________________________,该反应的化学方程式
为:______________________________________________________。
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图所示,图中B点溶液中含有的溶质有_____________________。
【五、燃烧的条件】
80℃
热水
②红磷
①白磷
铜片
③白磷
1.(2019·漳州)运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
A.①②现象对比,说明温度达到可燃物的着火点是燃烧条件之一
B.①③现象对比,说明有氧气参与是燃烧条件之一
C.白磷的着火点低于80 ℃
D.热水只起到加热作用
80℃
热水
红磷
白磷
铜片
白磷
2.(2019·云南)为探究燃烧的条件。某同学进行了如图所示的实验,下列说法错误的是( )
A.白磷是可燃物,红磷不是可燃物
B.热水中的白磷不燃烧是因为没有与氧气接触
C.铜片上的红磷不燃烧是因为温度未达到它的着火点
D.实验中水的作用是提供热量及隔绝氧气
3.(2019·海南)据报道,长征七号运载火箭将于2019年6月下旬在海南文昌发射,火箭采用了液氧煤油发动机等新技术,下列说法不正确的是( )
A.液氧是助燃剂 B.煤油是燃料 C.液氧是混合物 D.煤油是有机物
4.(2019·郴州)下列有关燃烧、灭火的分析正确的是( )
A.火上浇油:增大可燃物与氧气的接触面
B.钻木取火:提高可燃物的温度达到着火点
C.吹灭烛火:降低着火点
D.电器着火:用水浇灭
5.(2019·滨州)化学课上我们曾经观察过如图所示的实验。
(1)实验中,铜片上的白磷很快燃烧,其反应的化学方程式为:_________________________________;
80℃
热水
红磷
白磷
铜片
白磷
(2)该实验主要利用了铜片良好的__________性,燃着的白磷
熄灭后,去掉铜片上的白色固体,可看到铜片表面变黑,
该黑色物质是________(填化学式);
(3)烧杯中的水在实验中没有起到的作用是_____(填序号)。
A、作反应物 B、隔绝空气 C、升高温度
【六、一定溶质质量分数的氯化钠溶液的配制】
1.(2019·扬州)在“配制一定溶质质量分数的氯化钠溶液”实验中,下列操作正确的是( )
甲 乙 丙 丁
第1题图
A.甲图表示称取7.5 g氯化钠 B.乙图表示量取42.5 mL水
C.丙图表示溶解氯化钠 D.丁图表示向试剂瓶中转移溶液
2.(2019·贺州)在《一定质量分数的氯化钠溶液的配制»和«粗盐中难溶性杂质的去除》两个实验中都能使用到的( )
A.烧杯、玻璃棒、托盘天平、量筒 B.烧杯、玻璃棒、托盘天平、试管
C.托盘天平、量筒、烧杯、漏斗 D.蒸发皿、酒精灯、烧杯、铁架台
3.(2016·常州)配制生理盐水时,导致其溶质质量分数偏小的原因可能是( )
①将称好的氯化钠固体转移到烧杯中时,有少量溢出 ②用量筒量取水时,将量筒举过头顶读数
③溶解过程中未用玻璃棒搅拌 ④盛装生理盐水的试管刷洗后未干燥
A.仅①④ B.仅②③
C.①②④ D.①③④
4.(2019·呼和浩特)小明要配制50 g质量分数为14%的氢氧化钠溶液制作“叶脉书签”,下列关于配制该溶液的说法不正确的是( )
①若用氢氧化钠固体配制,需称取氢氧化钠固体7.0 g
②用托盘天平称氢氧化钠固体时,在两盘各放一张质量相等的纸
③选用200 mL量筒量取所需水的体积
④实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
⑤用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小
A.①③ B.②③⑤ C.③⑤ D.②④⑤
5.(2019·丹东)小莉、小晶两位同学用如下两种不同的方法,配制100 g溶质质量分数为5%的氯化钠溶液.
【小莉用固体氯化钠和水配制溶液】
(1)小莉用到的玻璃仪器有量筒、胶头滴管、烧杯、_________和试剂瓶。
(2)小莉实验时应进行的步骤是计算、称量、量取、_________、装瓶并贴标签。
【小晶用溶质质量分数为20%的氯化钠溶液加水稀释】
(3)小晶实验时应量取水的体积是__________mL(水的密度可近似看做l g/cm3)。
(4)若小晶量取水时俯视读数,则所配溶液的溶质质量分数_________5%。(选填“>”“<”或“=”)
6.(2015·滨州)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
10 g
两盘均有小纸片
NaCl
5 g
① ② ③ ④ ⑤ ⑥
第6题图
(1)用图中序号表示配制溶液的正确操作顺序_______________________;
(2)图②中用来取用NaCl的仪器是____________;
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为_________g;
(4)NaCl称量完毕放回砝码时,发现10 g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数___________(填“大于”、“小于”或“等于”)10%。
【七、溶液酸碱性的检验】
1.(2019·舟山)以下是某些同学在“测定土壤酸碱性”实验中的操作,其中错误的是( )
A.加土壤颗粒 B.加水溶解 C.振荡试管 D.用玻璃棒蘸取清液
2.(2019·株洲)头发的主要成分是蛋白质,容易受碱性溶液的侵蚀。所以我们洗发时,在用过洗发剂后再使用护发剂,这样对头发有保护作用.由此可知,护发剂的pH( )
A.<7 B.>7
C.=7 D.比洗发剂的pH大
3.(2019·广州)常温下,下列说法错误的是( )
A.pH=2的溶液显酸性
B.pH=7的溶液显中性
C.溶液的pH由5变成2,其酸性减弱
D.pH>10的土壤不适于种植农作物,因为碱性太强
4.(2019·江西)某校同学开展了如图所示“溶液酸碱性的检验”的实验活动:
pH试纸
镊子
玻璃棒
玻璃棒
pH试纸
pH试纸
A B C
潮湿的
点滴板
干燥的
点滴板
白
醋
紫薯汁
盐酸
蔗糖水
草木灰水
石灰水
图1 图2
第4题图
(1)把自制的紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液
白醋
盐酸
蔗糖水
草木灰水
石灰水
加入紫薯汁之后的颜色
红色
红色
紫色
绿色
绿色
①图1中存放紫薯汁的仪器名称是___________________。
②据上表推测,紫薯汁遇到稀硫酸溶液可能显示的颜色是_________,该汁液______(填“能”或“不能”)作酸碱指示剂。
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于__________(填“酸性”、“中性”或“碱性”)溶液,白醋pH________(填“>”、“<”或“=”)7。
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是________(填“A”、“B”或“C”,下同),可能导致被测溶液的pH数值发生改变的错误操作是_________。
【八、酸碱的化学性质】
1.(2019·遵义)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
2.(2019·佛山)柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸性,主要用于香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )
A.Mg
B.Fe2O3
C.CO2
D.NaOH
3.(2019·金华)为区别稀盐酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂。其中能达到实验目的是( )
氢氧化钠溶液
碳酸钠溶液
石蕊试液
氯化钡溶液
A B C D
4.(2019·聊城)氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用 B.都能解离出氢氧根离子
C.都能解离出金属阳离子 D.都含有氢元素和氧元素
5.(2019·衢州)小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中滴加3滴溶液,除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%,下列叙述正确的是
甲 乙 丙 丁 戊
氢氧化钙
碳酸
钾
氯
化
铜
氯
化
铁
氢氧化钠
氢氧化钙
氢氧化钠
氢氧化钙
氯
化
铜
氯
化
铁
( )
第5题图
A.甲组和乙组实验能观察到相同的现象 B.乙组和丙组实验均能观察到蓝色沉淀
C.乙组实验产生的沉淀质量比丁组多 D.戊组实验产生的沉淀质量比丙组少
6.(2019·茂名)归纳总结是学习化学的一种方法。请结合小明同学对碱的四点化学性质的归纳图完成下列问题。
(箭头上方的物质是指与碱反应的物质)
碱
溶
液
某些非金
属氧化物
性质2
盐和水
指示剂
性质1
变色
某些盐
性质4
性质3
盐和水
新盐和新碱
第6题图
(1)碱溶液能使无色酚酞溶液变________。
(2)氢氧化钠暴露在空气中变质的化学方程式为__________________________________________,所以氢氧化钠必须_________________保存。
(3)请帮小明补充完整性质3箭头上方的反应物质是_________(填“酸”或“碱”或“盐”)。
(4)碱溶液有相似的化学性质,是因为碱溶液中都含有__________(填化学符号)。