- 167.83 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2018武汉市中考化学模拟卷
姓名: 分数:
说明:本试卷分第Ⅰ卷和第Ⅱ卷。第Ⅰ卷为选择题,第Ⅱ卷为非选择题。全卷满分50分,考试用时45分钟。
可能用到的相对原子质量:H-l C-12 O-16 Na-23 S-32 Cl-35.5
第Ⅰ卷(选择题 共24分)
一、选择题(本题包括8小题,每小题只有1个正确选项。每小题3分,共24分)
1.下列变化中,属于化学变化的是 ( )
A.瓷碗破碎
B.石蜡熔化
C.玉米酿酒
D.汽油挥发
2.下列说法错误的是 ( )
A.原子、分子总是在不断地运动
B.分子可以再分,原子不能再分
C.酒精、天然气、煤气都含有碳、氢元素,都可以作燃料
D.黄铜、硬铝、钢铁都是金属合金,与非金属无关
3.下列实验操作正确的是 ( )
A. 稀释浓硫酸
B.蒸发食盐水
C.倾倒液体
D.熄灭酒精灯
4.化学在生活中用途广泛,下列有关说法错误的是 ( )
A.运用活性炭净水能够降低水的硬度
B.适量补钙有利于青少年身体发育
C.滥用食品添加剂有害人体健康
D.回收塑料既节约资源又减少“白色污染”
5.一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2=2CuO+ O2↑+4X↑.下列有关说法错误的是 ( )
A.X属于氧化物
B.该反应的基本反应类型为分解反应
C.该反应前后元素的化合价没有发生改变
D.X中氮、氧元素的质量比为7:16
6.某化学小组利用如图所示实验装置测定空气中氧气的含量(部分固定装置已略去).关于该实验有下列说法:其中不正确正确的是 ( )
A.向烧杯中加水是为了提高烧杯内的温度;
B.白磷的量不足,会使测定的结果偏大;
C.实验中可观察到,注射器的活塞先向右移动,后向左移动;
D.若试管内净容积为50mL
,反应后冷却至室温,活塞停止在40mL附近.
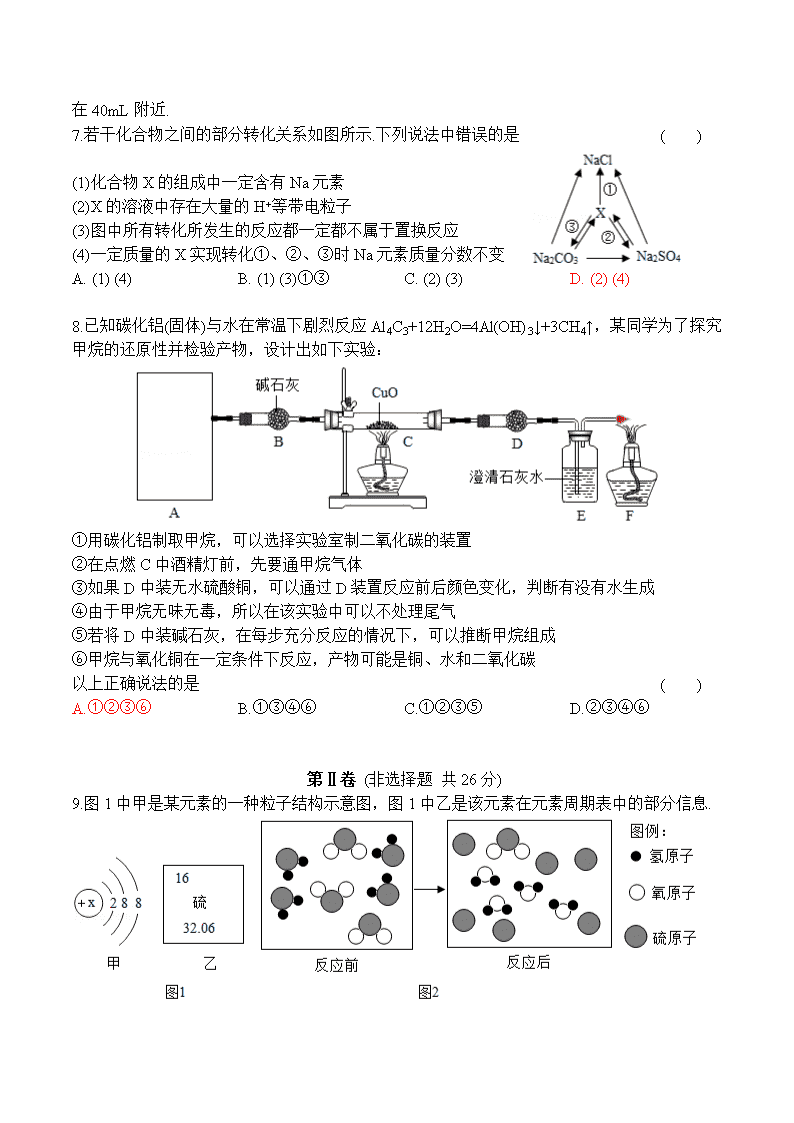
7.若干化合物之间的部分转化关系如图所示.下列说法中错误的是 ( )
(1)化合物X的组成中一定含有Na元素
(2)X的溶液中存在大量的H+等带电粒子
(3)图中所有转化所发生的反应都一定都不属于置换反应
(4)一定质量的X实现转化①、②、③时Na元素质量分数不变
A. (1) (4)
B. (1) (3)①③
C. (2) (3)
D. (2) (4)
8.已知碳化铝(固体)与水在常温下剧烈反应Al4C3+12H2O=4Al(OH)3↓+3CH4↑,某同学为了探究甲烷的还原性并检验产物,设计出如下实验:
①用碳化铝制取甲烷,可以选择实验室制二氧化碳的装置
②在点燃C中酒精灯前,先要通甲烷气体
③如果D中装无水硫酸铜,可以通过D装置反应前后颜色变化,判断有没有水生成
④由于甲烷无味无毒,所以在该实验中可以不处理尾气
⑤若将D中装碱石灰,在每步充分反应的情况下,可以推断甲烷组成
⑥甲烷与氧化铜在一定条件下反应,产物可能是铜、水和二氧化碳
以上正确说法的是 ( )
A.①②③⑥
B.①③④⑥
C.①②③⑤
D.②③④⑥
第Ⅱ卷 (非选择题 共26分)
9.图1中甲是某元素的一种粒子结构示意图,图1中乙是该元素在元素周期表中的部分信息.
(1)该元素原子的核外电子数为 16 ,图1甲所示粒子的符号为 S2﹣ .
(2)图2是该元素的化合物在常温下的有关化学反应的微观示意图.该反应的化学方程式为 SO2+2H2S=3S+2H2O .
10.根据如图A、B、C三种物质的溶解度曲线回答:
(1)A、B、C三种物质有可能为气体的是 C .
(2)t1℃时,将等质量的A和B分别加入盛有等质量水的烧杯中,充分搅拌后,其中一个烧杯中仍有少量固体未溶解,则未溶解的固体是 A .
(3)现要配制t3℃时,A物质的饱和溶液75g,需要A物质的质量为 25g .
(4)t3℃等质量的A、B、C的饱和溶液降温到t2℃,下列说法正确的是 B
A.析出晶体最多的是B
B.含溶剂量最多的是C
C.剩余溶液中,A与B的溶质的质量相等
D.t2℃时A、B、C都得到饱和溶液.
11.现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验。请根据实验现象判断:
(1)取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有 、 。
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡。则此固体粉末中一定有 、 。
(3)取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确 (填“是”或“否”)
(4)对于是否含有NaCl,你认为应对步骤(2)作如何改进
[若步骤(3)填“是”,此空不作答]。
答案:
(1)CaCO3、CuSO4
(2)Na2CO3、Na2SO4
(3)否
(4)将BaCl2溶液换成Ba(NO3)2溶液或Ba(OH)2溶液
12.某CuO粉末中混有少量Cu2O,现有一课外活动小组利用下图所示装置测定其中Cu2O的含量,请根据图示内容回答下列问题:
(1)X是常见还原性气体CO、H2中的一种,请根据组合装置判断X的化学式为 ,
A装置的作用是 .
(2)B装置的作用是 .若缺少它,将直接导致反应后
装置内的物质的质量有偏差.
(3)已知Cu2O在加热的条件下也能被X气体还原为Cu,写出该反应的化学方程式: .
(4)已知反应前CuO和Cu2O的总质量为m1g,完全反应后U型管内物质的质量增加了m2g(损失忽略不计),则原混合物中Cu2O的质量为 克.
(5)E装置的作用是 .
(6)若进入C中的气体换成两种气体中的另外一种,同样要求用该装置完成Cu2O含量的测定实验,则D中的药品应改换为 .
答案:(1)H2 除去X气体中可能混有的酸性气体;
(2)除去X气体中的水蒸气、D;
(3)H2+Cu2O2Cu+H2O;
(4)2.25m1-10m2;
(5)吸收空气中的水蒸气;
(6)碱石灰;
13.实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示.试回答:
(1)a点溶液中含有的溶质有 H2SO4、Na2SO4 .
(2)计算稀H2SO4的溶质质量分数.
(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以溶液中含有的溶质有:H2SO4、Na2SO4;故答案为:H2SO4、Na2SO4;
(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;
10g稀硫酸样品含有H2SO4的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
0.8g x
解得:x=0.98g
稀H2SO4的溶质质量分数为:×100%=9.8%
答:稀H2SO4的溶质质量分数是9.8%.