- 51.00 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
《金属和金属材料》考点例析
例1上海世博会部分场馆的图片如下。图片说明中出现了金属材料的是( )
解析 氟碳涂料也称氟碳漆,是一种化工原料;钢是铁的合金,属于金属材料;聚碳酸酯是一种塑料,常用于笔记本电脑的外壳;青花瓷属于陶瓷,是无机非金属材料。
答案 B
例2 菜刀用铁制而不用铅制的原因是( )
A.铁的硬度大,铅的硬度小 B.铁的熔点高,铅的熔点低
C.铁的密度大,铅的密度小 D.铁的导电性好,铅的导电性差
解析 菜刀用铁制主要利用了铁的硬度大的性质,与熔点、密度、导电性无关。
答案 A
例3 下列关于铁的叙述正确的是( )
A.切过泡菜的菜刀比置于潮湿空气中的菜刀更易生锈
B.铁与稀盐酸反应,生成FeCl3和H2
C.能用铁桶盛装农药波尔多液
D.用稀硫酸除铁锈,生成FeSO4和H2O
解析 泡菜呈酸性,切过泡菜的刀上残留酸性物质,更容易使菜刀生锈,A正确;Fe与稀盐酸反应生成FeCl2而不是FeCl3,B错误;波尔多液中含有CuSO4,若用铁桶盛装会发生反应,这样既会损失药效,又会腐蚀铁桶,C错误;铁锈的主要成分是Fe2O3,与稀硫酸反应生成Fe2(SO4)3而不是FeSO4,D错误。
答案 A
例4 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放人硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A.Z、Y、X B.X、Y、Z C.Y、X、Z D.X、Z、Y
解析 X能与稀硫酸反应产生氢气而Y不能,说明X排在金属活动顺序中氢的前面,而Y排在氢的后面;Y能置换出硝酸银中的银,而Z不能,说明Y的活动性比Z强,因此三种金属的活动性由强到弱的顺序为X、Y、Z。
答案 B
例5 物质的性质决定着物质在生产和生活中的的用途。木炭和一氧化碳都具有还原性,可用于冶炼金属。请根据下图回答:
(1)请写出下列反应的化学方程式:
①木炭还原氧化铜_________________________。
②一氧化碳还原氧化铁_________________________。
(2)A、B装置中澄清石灰水的作用是_________________________。
(3)B装置最右端酒精灯的作用是_________________________。
(4)在A装置中,当观察到______________现象时,证明木炭粉末和氧化铜粉末已经完全反应。
解析 木炭还原CuO生成Cu和CO2,CO还原Fe2O3生成Fe和CO2;装置中澄清石灰水的作用是检验反应是否生成CO2;因为CO有毒,会污染空气,因此需要将B装置尾气中末反应的CO燃烧掉;当A装置中竖直试管内的导管口没有气泡产生,说明不再有生成,证明反应已结束。
答案 (1)①C+2CuO2Cu+CO2↑ ②3CO+Fe2O32Fe+3CO2 (2)检验是否有二氧化碳生成 (3)除去未反应完的一氧化碳气体,防止污染空气
(4)A装置竖直放置的试管内导管口不再有气泡冒出
例6 右图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断错误的是( )
A.b管中铁钉不会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与空气、水有关
D.若将a管中的水改为食盐水能加快铁的锈蚀
解析 铁在潮湿的空气中易生锈,a试管中的铁钉会生锈,且试管内的压强减小,而b试管中的铁钉不会生锈,试管内的压强不变,因此L端与R端液面高度不会保持一致;铁生锈的条件是氧气和水,与氯化钠无关,但在氯化钠存在的环境中,铁生锈的速率会加快。
答案 B
例7 人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产的需要。
(1)钢铁是我们日常生活中使用最多的金属材料。高炉炼铁常以焦炭、铁矿石、石灰石、空气等为原料。炼铁过程中,一氧化碳和赤铁矿(主要成分为Fe2O3)反应的化学方程式为__________________________。
(2)我国钢铁年产量很高,但因锈蚀造成的损失也很惊人。人们常采取在铁制品表面涂刷油漆或镀上其他金属等方法,以防止其锈蚀。上述方法所依据的原理是___________。
(3)我国矿物储量很丰富,但人均占有量并不多,请保护金属资源!下面几种做法中,可有效保护金属资源的是__________(填字母)。
a.回收利用废旧金属制品 b.任意开采铁矿石
c.铁制品不加处理,存放在潮湿的环境中 d.寻找、开发金属的代用品
解析 CO具有还原性,能夺取Fe2O3中的氧生成Fe和CO2;在钢铁上涂上保护层以隔绝空气和水,防止钢铁生锈;保护金属资源的措施主要有:防止金属锈蚀、合理开采金属资源、回收利用废旧金属、寻找和开发金属的代用品等。
答案 (1)3CO+Fe2O32Fe+3CO2 (2)将铁制品与空气和水隔绝(或将铁制品与潮湿的空气隔绝) (3)ad
变式训练:
1.有关铝、铁、铜的说法中不正确的是( )
A.铝是地壳中含量最多的金属元素 B.三种金属中最活泼的是铁
C.铝可以与硫酸铜溶液反应 D.铜可以用来做电线
2.根据金属活动性顺序分析,下列描述或判断错误的是( )
A.常温下,在空气中金属镁比铁容易氧化
B.在氧气中灼烧时,铁丝比铜丝反应剧烈
C.与同种盐酸反应时,锌片比铁片反应剧烈
D.铜活动性不强,故铜不能与硝酸银溶液反应得到金属银
3.把金属X放人CuCl2溶液中有红色物质析出,放人MgCl2溶液中无现象。则X、Cu、Mg三种金属活动性由强到弱的顺序正确的是( )
A.Mg、X、Cu B.Cu、X、Mg C.Mg、Cu、X D.X、Mg、Cu
4.金属活动性顺序在运用中给我们三条判断依据,即在金属活动性顺序里:
⑴金属的位置越靠前它的活动性就越强;
⑵位于氢前面的金属能置换出盐酸、稀硫酸中的氢;
⑶位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
通过查阅资料我发现金属铝与氧化铜在高温条件下能发生置换反应,其化学方程式为_________,由此我发现了一条新的判断依据_____________。
5.
钢铁在生产、生活中有广泛的用途。建造上海世博会的中国馆——“东方之冠”的核心筒就是用四根巨型钢筋混凝土制成的,其中用了大量的钢铁。
(1)钢铁属于___________(填“纯净物”或“混合物”);
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:____________________;
(3)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的__________和___________共同作用的结果;
(4)为了防止钢铁锈蚀,人们常采用_______________的方法(任写一种)来达到目的。
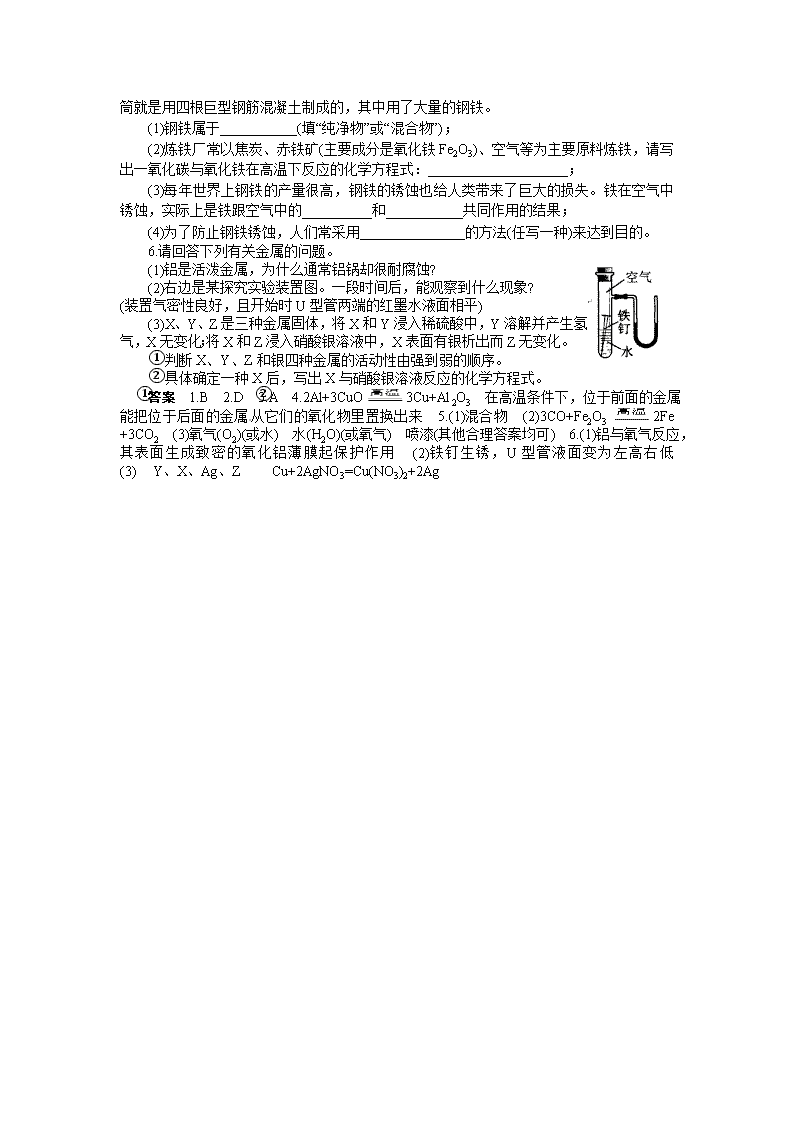
6.请回答下列有关金属的问题。
(1)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
(2)右边是某探究实验装置图。一段时间后,能观察到什么现象?
(装置气密性良好,且开始时U型管两端的红墨水液面相平)
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序。
②具体确定一种X后,写出X与硝酸银溶液反应的化学方程式。
答案 1.B 2.D 3.A 4.2Al+3CuO3Cu+Al2O3 在高温条件下,位于前面的金属能把位于后面的金属从它们的氧化物里置换出来 5.(1)混合物 (2)3CO+Fe2O3 2Fe +3CO2 (3)氧气(O2)(或水) 水(H2O)(或氧气) 喷漆(其他合理答案均可) 6.(1)铝与氧气反应,其表面生成致密的氧化铝薄膜起保护作用 (2)铁钉生锈,U型管液面变为左高右低 (3)①Y、X、Ag、Z ②Cu+2AgNO3=Cu(NO3)2+2Ag