- 553.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
注意事项:
1.本试卷1至15题为选择题,共30分。16至21题为非选择题,共50分。全卷满分80分.考试时间为60分钟。考生答题全部答在答题卡上,答在本试卷上无效。
2.请认真核对监考教师在答题卡上所粘贴条形码的姓名、考试证号是否与本人的相符合,再将自己的姓名、考试证号用0.5毫米黑色墨水签字笔填写在答题卡及本试卷上。
3.答选择题必须用2B铅笔将答题卡上对应的答案标号涂黑。如需改动,请用橡皮擦干净后.再选涂其他答案。答非选择题必须用0.5毫米黑色墨水签字笔写在答题卡的指定位置。在其他位置答题一律无效。
可能用到的相对原子质量:H-I C- 12 O-16 Na-23 S-32 Cl-35.5 K-39 Fe-56 Cu-64
一、选择题(本题共15小题,每小题只有一个选项符合题意。每小题2分,共30分)
1.在人体所含的元素中,质量分数最高的是
A.氢 B.氧 C.钙 D.铁
2.今年5月31日是第31个世界无烟日,下列图标中表示禁止吸烟的是
3.下列属于天然有机高分子材料的是
A.塑料 B.棉花 C.涤纶 D.不锈钢
4.通常状况下,颜色呈紫红色的金属是
A.铁 B.银 C.铜 D.铝
5.下列做法有利于保护水资源的是
A.生活污水直接排放 B.生活中节约用水
C.大量开采使用地下水 D.大量使用化肥和农药
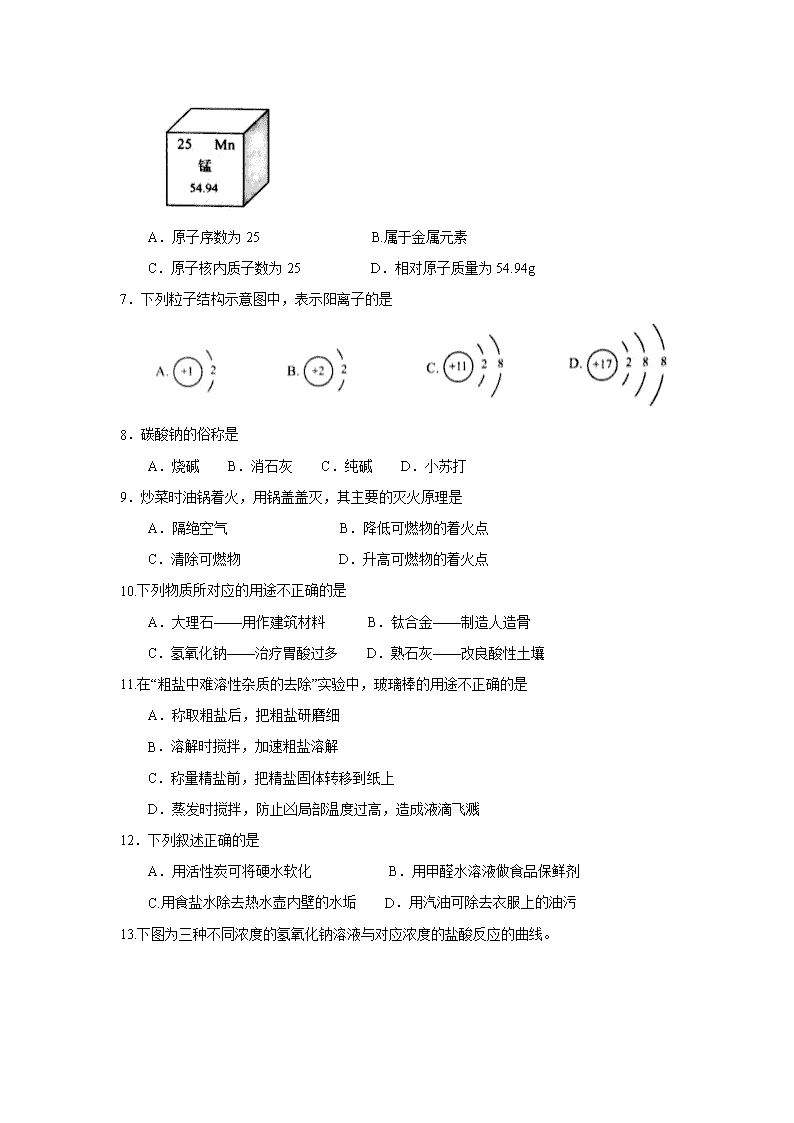
6.北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。在元素周期表中锰元素的某些信息如图所示,下列有关锰的说法不正确的是
A.原子序数为25 B.属于金属元素
C.原子核内质子数为25 D.相对原子质量为54.94g
7.下列粒子结构示意图中,表示阳离子的是
8.碳酸钠的俗称是
A.烧碱 B.消石灰 C.纯碱 D.小苏打
9.炒菜时油锅着火,用锅盖盖灭,其主要的灭火原理是
A.隔绝空气 B.降低可燃物的着火点
C.清除可燃物 D.升高可燃物的着火点
10.下列物质所对应的用途不正确的是
A.大理石——用作建筑材料 B.钛合金——制造人造骨
C.氢氧化钠——治疗胃酸过多 D.熟石灰——改良酸性土壤
11.在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是
A.称取粗盐后,把粗盐研磨细
B.溶解时搅拌,加速粗盐溶解
C.称量精盐前,把精盐固体转移到纸上
D.蒸发时搅拌,防止凶局部温度过高,造成液滴飞溅
12.下列叙述正确的是
A.用活性炭可将硬水软化 B.用甲醛水溶液做食品保鲜剂
C.用食盐水除去热水壶内壁的水垢 D.用汽油可除去衣服上的油污
13.下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。
下列说法正确的是
A.在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B.在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C.在a、b、c三种曲线所示的实验中,反应速率相同
D.在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
14.下列各组离子在水中一定能大量共存,并形成无色溶液的是
A. Cu2+、H+、SO42-、CI- B. Ba2+、Na+、CI-、NO3-
C. K+、Ca2+、OH-、CO32- D. Na+、H+、HCO3-、NO3-
15.在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示。图中a、b、c、d分别表示相应物质的质量分数。下列数据正确的是
A. a=56% B. b=6% C. c=17% D. d=8%
二、(本题包括2小题,共13分)
16.(9分)某同学在学习中构建了“氮及其化合物的价、类关系图”。
(1)写出图中A、B、C点对应物质的化学式各—个:________ 、________ 、________。
(2)与图中的点对应物质不相符合的化学式是________。
(3)在纯净物中,根据________ ,可以把它们分成单质和化合物。
(4)氮气是由________(填“分子”、“原子”或“离子”)构成的。
(5)完成鉴别硫酸钾和硫酸铵两种固体化肥的实验报告。
实验步骤
实验现象
实验结论
________
________
________
17.(4分)201 8年5月9日我国成功发射高分五号卫星,它是世界首颗实现对大气和陆地综合观测的全谱段高光谱卫星,可通过对大气污染气体、温室气体等物理要素的监测,动态反映我国空气质量状况。
(1)下列属于空气污染物的是________。
A.臭氧 B.一氧化碳 C.PM2.5 D.PM10
(2)化石燃料是________(填“可再生能源”或“不可再生能源”),它们燃烧会造成空气污染,应合理利用与开发。
(3)下列气体排放到空气中会形成酸雨的是________。
A.二氧化硫 B.氮气 C.二氧化氮 D.一氧化碳
(4)小明同学收集刚降到地面的雨水水样,用pH计每隔几分钟测一次pH,其数据如下图所示,则所降雨水________(填“是”或“不是”)酸雨。
18.(5分)下表是NaCl、KNO3在不同温度时的溶解度:
(1)根据表中的数据,在坐标纸上绘制出氯化钠和硝酸钾两种物质的溶解度曲线。(在答题卡的坐标纸上绘图)
(2)根据绘制的氯化钠和硝酸钾的溶解度曲线判断,温度大约在______℃时,两种物质的溶解度大小相等。
(3)20℃时,在50 g水中加入12.5 g硝酸钾固体,允分搅拌后得到______(填“饱和”或“不饱和”)溶液,此时该溶液中溶质的质量分数为______。
(4)在60℃时,硝酸钾的溶解度是110g。这句话的含义是______。
四、(本题包括2小题,共l 8分)
19.(12分)碳及其氧化物性质的应用。
(1)如右图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色消失,说明木炭具有______能力,其原因是木炭具有______的结构。
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,原因是______。
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出反应的化学方程式 ____________;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于______时,则可证明金刚石是由碳元素组成的单质。
(4)
在实验室里,检验二氧化碳一般用澄清石灰水,而吸收二氧化碳常用氢氧化钠溶液,理由是____________。
(5)写出碳在高温时还原氧化铜的化学方程式,并计算要使80 g氧化铜完全还原,需要碳的质量至少是多少?(在答题卡上写出计算过程)
20.(6分)图中A~M是初中化学常见的物质,且分别由H、C、O、Na、S、Cl、K、Fe中一种或几种元素组成。B、C、E、F、M均由两种元素组成,B中两种元素质量之化为7:3.固态E叫做“干冰”;A、D、H均由三种元素组成,H在实验室可用于制取氧气;G是焙制糕点所用的发酵粉的主要成分之一。图中“—”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(l)写出化学式:G________,B________。
(2)写小H→I反应的化学方程式___________。
(3)写出A与D反应的化学方程式__________。
五、(本题包括l小题,共14分)
21.(14分)兴趣小组的同学对铝的某些性质进行相关探究。
【实验回顾】
(l)铝与稀盐酸反应。
①用图1所示装置制取氢气。
铝与稀盐酸反应的化学方程式为__________。
②用B装置收集氢气的原因是____________。
(2)在金属活动性顺序里,金属能否置换出盐酸和稀硫酸中的氢,判断的依据是__________。
【提出问题】
铝能否与水反应生成氢气?
【查阅资料】
物质
钠与水
铝与水
汞与水
能否发生反应
能反应
能反应
不反应
【交流与讨论】
(I)铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,起到保护膜的作用。如生活中可用铝壶烧水。铝与氧气反应的化学方程式为_____________。
(2)除去铝表面氧化铝薄膜的方法(举一例)_________。除上述方法外,还可以将铝片浸入氯化汞( HgCI2)溶液中,形成铝汞齐(铝汞合金)破坏铝表面致密的氧化膜且防止其重新生成。
【实验探究】
(1)将铝片完全浸入氯化汞(HgCl2)溶液中1分钟左右,取出,立即用流水冲洗干净后加入到蒸馏水中(如图2),其表面生成大量气泡、周围出现白色沉淀。铝与氯化汞溶液发生置换反应的化学方程式为__________。
(2)在导管口a处涂肥皂水,发现导管口有气泡形成,当气泡离开导管后,气泡______(填“下沉”或“上升”),用燃着的木条点燃气泡,发出爆鸣声。
【实验结论】
铝能与水反应生成氢气。
写出铝与水反应生成氢氧化铝和氢气的化学方程式____________。
【实验反思】
(1)图2装置内,在铝与水反应的过程中,若关闭导管上的活塞K,反应停止,其原理是_______。当再次打开活塞K,反应继续,产生气泡。铝未能生成氧化铝,其原因是________。
(2)汞有毒,会污染环境,兴趣小组的同学用硫粉处理单质汞,用饱和硫化钠溶液处理使用过的氯化汞废液。
一、选择题(本题共15小题,每小题只有一个选项符合题意。每小题2分,共30分)
1.B 2.D 3.B 4.C 5.B 6.D 7.C 8.C 9.A 10.C 11.A 12.D 13.A 14.B 15.A
说明:主观性试题,答案合理均给分。
二、(本题包括2小题,共13分)
16.(本题共9分)
(1)N2O HNO3 NH3·H2O;(2) NaNO3 ;(3)组成元素的异同;(4)分子;
(5)
实验步骤
实验现象
实验结论
取样,分别放入研钵内,各加入少量熟石灰粉末,混合、研磨。
一只研钵中有刺激性气味气体放出;
另一只研钵中无刺激性气味气体放出。
有刺激性气味气体放出的原样品是硫酸铵;
无刺激性气味气体放出的原样品是硫酸钾。
17.(本题共4分)
(1)ABCD;(2)不可再生能源;(3)AC;(4)是
三、(本题包括1小题,共5分)
18.(本题共5分)
(1)
(2)24;(3)不饱和;20%
(4)在60℃时,100 g水里最多能溶解110 g硝酸钾。
四、(本题包括2小题,共18分)
19.(本题共I 2分)
(1)吸附; 疏松多孔
(2)碳素墨水中含有碳,在常温下,碳的化学性质不活泼。
(3)C+O2CO2,生成的二氧化碳中碳元素的质量
(4)答题要点:澄清石灰水、氢氧化钠溶液分别与二氧化碳反应的现象不同;氢氧化钠、氢氧化钙溶解性的大小,氢氧化钠溶液和氢氧化钙溶液分别吸收二氧化碳的能力不同。
(5) 6g。
20.(本题共6分)
(1) NaHCO3;Fe2O3
(2)2KClO32KCl+3O2↑
(3)K2CO3+H2SO4==K2SO4+H2O+CO2↑
五、(本题包括1小题,共14分)
21.(本题共14分)
【实验回顾】(1)①2Al+6HCl==2AlCl3+3H2↑
②氢气难溶于水,不与水反应。
(2)答题要点:金属是否位于氢前面。
【交流与讨论】(1)4Al+3O2==2A12O3
(2)用砂纸打磨
【实验探究】(1)2Al+3HgCl2==2AlCl3+3Hg
(2)上升
【实验结论】2Al+6H2O=2Al(OH)3+3H2 ↑
【实验反思】(1)关闭活塞K,容器内压强增大,把液体压回烧杯,固体与液体分离,反应停止。容器内充满氢气,铝无法与氧气接触。