- 632.00 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
中考化学教师辅导讲义
授课主题
图像专题
教学目的
掌握图像信息题解题技能,掌握常考内容。
教学重难点
溶质质量分数 反应先后顺序
授课日期及时段
教学内容
一、 知识点讲解
类型一 pH变化曲线
1. 酸碱中和反应中的pH曲线图像:
图①,碱入酸,在0点时,溶液的pH<7,此时溶液呈酸性;当酸碱恰好完全反应时,溶液的pH=7;随着碱的继续加入,溶液的pH>7,溶液呈碱性。
图②,酸入碱,在0点时,溶液的pH>7,此时溶液呈碱性;当酸碱恰好完全反应时,溶液的pH=7;随着酸的继续加入,溶液的pH<7,溶液呈酸性。
2.溶液稀释的pH曲线图像:
图①,碱性溶液稀释时,由于碱性溶液的pH>7,而水的pH=7,随着水的质量的增加,pH不断减小,但不会小于等于7。
图②,酸性溶液稀释时,由于酸性溶液的pH<7,而水的pH=7,随着水的质量的增加,pH不断增大,但不会大于等于7。
类型二 溶质质量分数的变化曲线
1、物质溶解时,溶质质量分数的变化图像:
图①,在一定温度下,向某溶液的不饱和溶液中继续加入某溶质,该溶质的质量分数随着溶质的增加而增大,当溶液达到饱和时,溶质质量分数不变。
图②,溶液稀释时,溶质的质量不变,而溶液的总质量不断增加,所以溶质质量分数不断减小。
2、关于曲线类试题,全国中考中,还会涉及到发生化学反应的溶质质量分数的曲线图。
图像:
图①,随着反应的进行,反应物的溶质质量分数不断减小,直到反应物恰好完全反应后溶质质量分数为零。
图②,随着反应的进行,生成物溶质质量不断增加,溶质质量分数不断增大,直至反应结束溶质质量分数达到最大值。
类型三 化学反应中物质质量的变化曲线
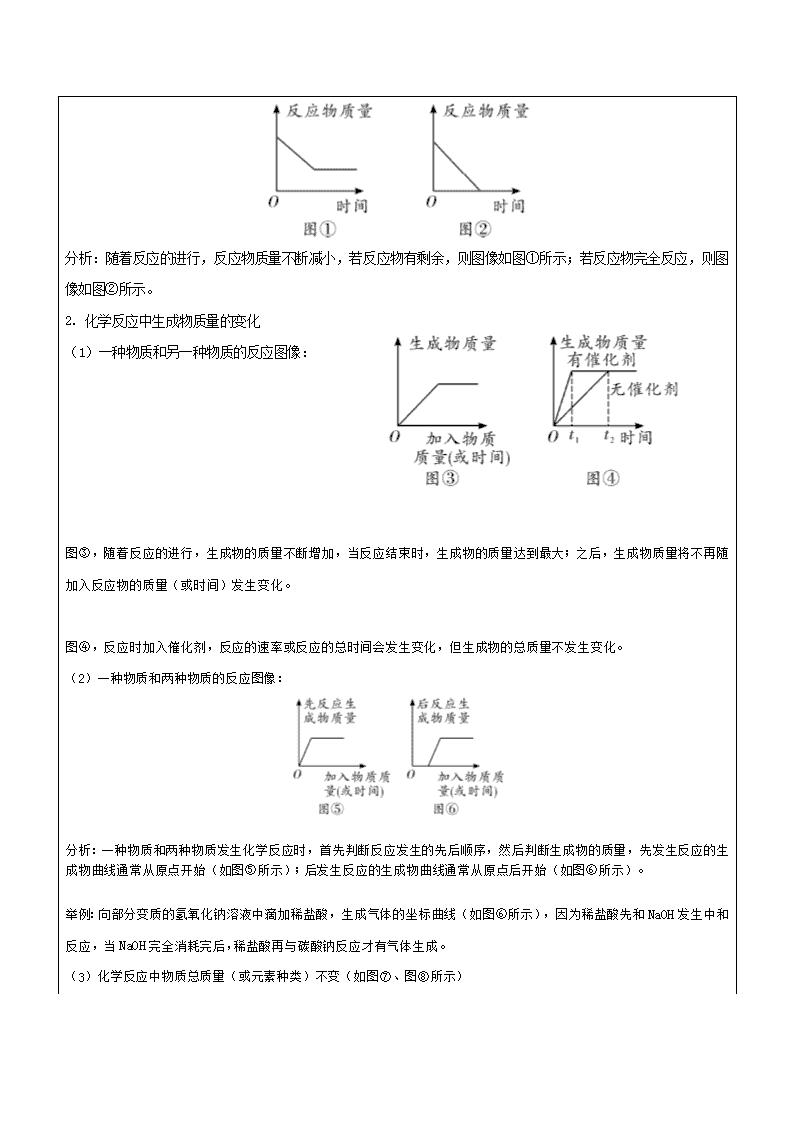
1. 化学反应中反应物质量的变化图像:
分析:随着反应的进行,反应物质量不断减小,若反应物有剩余,则图像如图①所示;若反应物完全反应,则图像如图②所示。
2. 化学反应中生成物质量的变化
(1)一种物质和另一种物质的反应图像:
图③,随着反应的进行,生成物的质量不断增加,当反应结束时,生成物的质量达到最大;之后,生成物质量将不再随加入反应物的质量(或时间)发生变化。
图④,反应时加入催化剂,反应的速率或反应的总时间会发生变化,但生成物的总质量不发生变化。
(2)一种物质和两种物质的反应图像:
分析:一种物质和两种物质发生化学反应时,首先判断反应发生的先后顺序,然后判断生成物的质量,先发生反应的生成物曲线通常从原点开始(如图⑤所示);后发生反应的生成物曲线通常从原点后开始(如图⑥所示)。
举例:向部分变质的氢氧化钠溶液中滴加稀盐酸,生成气体的坐标曲线(如图⑥所示),因为稀盐酸先和NaOH发生中和反应,当NaOH完全消耗完后,稀盐酸再与碳酸钠反应才有气体生成。
(3)化学反应中物质总质量(或元素种类)不变(如图⑦、图⑧所示)
类型四 放出气体或生成沉淀时的反应先后
1.向Na2CO3和NaOH的混合溶液中滴入稀HCl。
2. 向CuSO4和H2SO4的混合溶液中滴入NaOH溶液。(向FeCl3和HCl的混合溶液中滴入NaOH溶液)
3. 向CaCl2和HCl的混合溶液中滴入Na2CO3溶液。
4.向BaCl2和NaOH的混合溶液中滴入H2SO4。
(H2SO4会先和BaCl2发生反应,因此从开始就会有沉淀产生。)
类型五 吸收气体时的反应先后
1、下列四个图像,分别对应四种操作过程,其中正确的是
A. 向盐酸中不断加水
B. 一定质量的镁在密闭的容器内燃烧
C. 等质量的铁和镁分别放入两份溶质质量分数相同的足量稀盐酸中
D. 某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体
一、 当堂检测
4、下列图像分别与选项中的操作相对应,其中合理的是( )
A. 向一定量稀氢氧化钠溶液中滴入水
B. 向一定量氯化铜溶液中加入一定量铝
C. 向一定量二氧化锰固体中加入一定过氧化氢溶液
D. 向一定量硫酸和硫酸铜混合溶液中滴氢氧化钠溶液
5、已知:2KClO3 2KCl + 3O2↑,如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量 y随时间的变化趋势。纵坐标表示的是( )
A.固体中氧元素的质量
B.生成O2的质量
C.固体中MnO2的质量
D. 固体中钾元素的质量分数
6、下列四个图像中有关量的变化趋势与对应叙述关系正确的是( )
A. 向一定量的氢氧化钠溶液中加入水
B. 加热一定质量的高锰酸钾固体
C. 分别向等质量等溶质质量分数的稀硫酸中加入足量的铁和锌
D. 向一定量的稀盐酸中加入大理石
7、在盛有一定质量硫酸铜溶液的小烧杯中,逐渐加入铁粉,直至过量。如图横坐标表示加入铁粉的质量,根据图像判断纵坐标可能表示( )
A. 小烧杯中所有物质的总质量
B. 小烧杯中溶液的总质量
C. 小烧杯中离子的总数目
D. 小烧杯中固体的总质量
8、下列所示图像能正确反映对应的实验或事实的是( )
A. 向氯化铁和稀盐酸的混合溶液中不断加氢氧化钠溶液
B. 等质量的碳酸钠粉末和块状碳酸钙分别与足量的等体积、等浓度盐酸反应
C. 向一定量的碳酸钠溶液中逐渐加水稀释
D. 向一定量的实验室废液(实验室制取二氧化碳后产生的)中逐滴滴加碳酸钠溶液
9、向装有50 g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量。有关量的变化情况见下图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中肯定不正确的是( )
10、向一定质量AgNO3和Cu(NO3)2
的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )
A. 取a点溶液,滴加稀盐酸,无白色沉淀
B.图标上b~c段质量增加的原因是Zn与Cu(NO3)2溶液反应
C. b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag
D. c点和d点溶质种类不同,金属单质种类也不同
11、下列曲线能正确表达对应的反应或过程的是( )。
A.向一定量的水中加入生石灰 B.红磷在装有空气的密闭容器中燃烧
C.向一定质量的烧碱溶液中滴入盐酸 D.向饱和KNO3溶液中加入KMnO4固体
12、在一定质量表面被氧化的镁条中,慢慢加入一定浓度的盐酸,反应中有关量的变化情况描述正确的是( )。
A B C D
13、下列4个图形能正确反映对应变化关系的是( )。
A B C D
A.向一定量稀硫酸中加入NaOH溶液
B.向一定量CuSO4溶液中加入Zn粉
C.加热KClO3与MnO2固体混合物
D.向一定量NaOH和Ca(OH)2的混合溶液中加入Na2CO3溶液
14、列图象中有关量的变化趋势与对应叙述关系正确的是( )。
A B C D
A.分别向质量相等的铁片和锌片中滴加稀硫酸
B.加热一定质量的高锰酸钾
C.某温度下,向一定质量的饱和硝酸钾溶液中不断加入硝酸钾晶体
D.向一定质量的NaOH溶液中滴加水
15、“铁、锌、铜、镁、铝”是生活中常见的金属。请根据所学知识回答下列问题:
(1)铝块能制成铝箔是利用了铝的______性。
(2)黄铜是铜锌合金,其硬度比纯铜_____(选填“大”或“小”)。
(3)将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有__________。
(4)将等质量的镁、铁、锌三种金属分别放入三份溶质质量分数相等的稀盐酸中。生成H2的质量与反应时间的关系如图所示。金属X是__________(填化学式,下同),反应后可能已经反应完的金属是________,一定有剩余的金属是_________。
16、NaOH是化学实验中常用的试剂。
(1)将某NaOH溶液逐滴滴入一定量的某盐酸中,上边图像合理的是______(选填“甲”或“乙”)。
(2)向长期敞口放置的NaOH溶液中滴加盐酸时,意外发现有气泡产生,请解释其原因。
(3)向足量某NaOH溶液中通入CO2,反应后溶液中的溶质可能只有Na2CO3,也可能还有NaOH,请设计实验检验溶质的成分,简要写出实验步骤、现象和结论。(提示:Na2CO3溶液呈碱性)
四、课堂总结
五、家庭作业
1.请用所学知识回答下列问题:
(1)不能服用NaOH治疗胃酸过多,因为NaOH具有 性.
(2)如图装置不能用来验证质量守恒定律,请解释原因.
2.分析下列现象回答下列问题:
(1)二氧化碳和水反应生成碳酸,光合作用将二氧化碳和水转化为有机物和氧气.反应物相同,产物不同,说明化学反应的产物受什么因素的影响?
(2)过氧化氢溶液在常温下分解缓慢,加入少量硫酸铜溶液后反应速率加快,说明化学反应速率受什么因素影响?
(3) 氧气能供给呼吸,而二氧化碳不能供给呼吸,请从分子的角度加以解释.
3.某化学兴趣小组的同学在做完硫酸铜溶液和氢氧化钠溶液反应实验后,对浑浊液过滤,得到无色澄清的滤液.
(1)对滤液中溶质的成分,同学们进行了如下猜想:
猜想一:硫酸钠
猜想二:硫酸钠与氢氧化钠
猜想三:硫酸钠与硫酸铜
经过讨论,同学们一致认为猜想 不成立,理由是 .
(2) 请你选择一种可能的猜想,进行验证,简要写出实验步骤和现象.
4.如图所示,向一定量AgNO3溶液中加入铜和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙.
(1)若乙中含有锌、铜、银三种固体,则溶液甲中所含的金属离子符号为 ,此时向固体乙中加入稀盐酸,写出反应的化学方程式为 .
(2)若溶液甲显蓝色,原因是什么?(用化学反应方程式表示).
5.看图回答下列问题.
(1)请写出用A装置制取氧气的化学方程式及选择依据.
(2) 实验室可用B装置制取CO2,其优点是什么?
(3) 为了得到纯净、干燥的CO2,除杂装置导管的正确连接顺序是 (填数字序号),请写出该过程中发生的化学反应的化学方程式 .
(4)CO2在生产生活中应用广泛,常用做灭火剂,其灭火的原理是 .金属钠失火时不能用二氧 化碳灭火,钠能和二氧化碳反应生成一种单质和一种盐,请写出反应的化学方程式.