- 154.50 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
初三化学中考模拟试题及答案
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24 S—32
Cl—35.5 K—39 Ca—40 Fe—56 Zn—65 I—127
注意:请将选择题答案填入第8页表格内
一、下列各题均有4个选项,其中只有1个是符合题意的。(共35分,每小题1分)
1. 空气是我们人类赖以生存的物质。在空气的组成中,体积约占1/5的气体是
(A)氧气 (B)水蒸气 (C)氮气 (D)二氧化碳
2. 亲爱的同学们,你是否注意过,我们身边有很多公共标志,下面与消防安全无关的公共标志是
(A) (B) (C) (D)
3. 下列变化中,属于化学变化的是
(A)轮胎爆炸 (B)玻璃破碎 (C)冰棒融化 (D)菜刀生锈
4. 地壳中含量最多的金属元素是
(A)氧 (B)硅 (C)铝 (D)铁
5. 下列各组物质中,属于单质的是
(A)水 (B)干冰 (C)红磷 (D)石灰水
6.人类生活需要能量。下列能量由化学变化产生的是
(A)电灯通电发出的光 (B)液化石油气燃烧放出的热量
(C)水力发电产生的电能 (D)电熨斗通电发出的热
7. 能决定元素种类的微粒数是
(A)质子数 (B)中子数 (C)最外层电子数 (D)电子数
8. 下列属于氧化物的是
(A)H2O (B)O2 (C)NaOH (D)KNO3
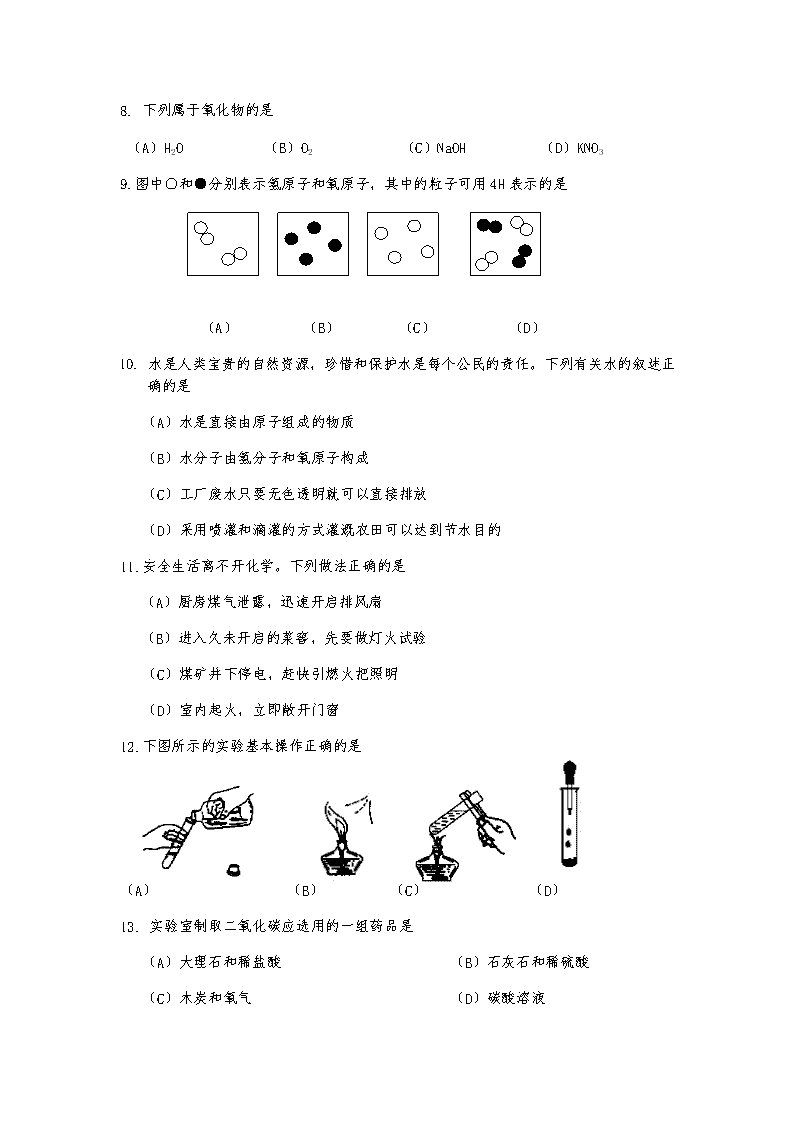
9.图中○和●分别表示氢原子和氧原子,其中的粒子可用4H表示的是
(A) (B) (C) (D)
10. 水是人类宝贵的自然资源,珍惜和保护水是每个公民的责任。下列有关水的叙述正确的是
(A)水是直接由原子组成的物质
(B)水分子由氢分子和氧原子构成
(C)工厂废水只要无色透明就可以直接排放
(D)采用喷灌和滴灌的方式灌溉农田可以达到节水目的
11.安全生活离不开化学。下列做法正确的是
(A)厨房煤气泄露,迅速开启排风扇
(B)进入久未开启的菜窖,先要做灯火试验
(C)煤矿井下停电,赶快引燃火把照明
(D)室内起火,立即敞开门窗
12.下图所示的实验基本操作正确的是
(A) (B) (C) (D)
13. 实验室制取二氧化碳应选用的一组药品是
(A)大理石和稀盐酸 (B)石灰石和稀硫酸
(C)木炭和氧气 (D)碳酸溶液
14.近几年我国一些地区时有火灾发生。如果室内遭遇火灾时,下列自救措施不正确的是
(A)尽快到达最近的可用出口的楼梯
(B)可将毛巾用水浸湿,捂在口鼻上作防毒面具
(C)遇房内浓烟弥漫时,可匍匐爬行逃生
(D)躲在衣柜内等待救援
15. 生活中下列常见的物质与水混合后,不能形成溶液的是
(A)蔗糖 (B)花生油 (C)食盐 (D)白醋
16. 下列仪器中,量取一定体积的液体时必须用到的是
(A) (B) (C) (D)
17.生活中的下列现象,可用分子的知识加以解释,其中正确的是
(A)热胀冷缩是因为分子大小随温度而变化
(B)蔗糖溶解是因为分子很小
(C)气体易被压缩是因为气体分子间隔很小
(D)墙内开花墙外香是因为分子在不断运动
18.下列关于分子和原子的说法中,错误的是
(A)原子是由原子核和核外电子构成的 (B)保持水的化学性质的粒子是水分子
(C)分子的质量总比原子的质量大 (D)在化学反应中分子可分而原子不可分
19.已知物质X符合下列转化关系:HCl + X MgCl2 + H2↑,则X可能是
(A)镁 (B)氧化镁 (C)锌 (D)氢气
20.下列气体与空气混合后点燃,有可能发生爆炸的是
(A)二氧化碳 (B)氢气 (C)氮气 (D)氧气
21.下列各混合物能用过滤法分离的是
(A)氯化钠和硝酸钾 (B)碘和酒精 (C)牛奶和水 (D)食盐水中的泥沙
22.现有20%的氯化钠溶液,根据“20%”这一数值,你可以知道该溶液
(A)溶质质量为20g (B)溶液质量为100g
(C)水的质量为80g (D)溶质∶溶剂∶溶液 (质量比)= 1∶4∶5
23.氯化钠在20℃时的溶解度为36克。则20℃时,氯化钠饱和溶液中溶质、溶剂、溶液之间的质量比正确的是
(A)溶质∶溶剂 = 36∶100 (B)溶质∶溶剂 = 36∶136
(C)溶剂∶溶液 = 136∶100 (D)溶质∶溶液 = 36∶100
24. 碳在氧气中充分燃烧的现象是
(A)生成CO2 (B)产生大量烟 (C)发白光 (D)产生蓝紫色火焰
25. 2.4g镁在氧气中充分反应后,固体质量增加了1.6g,则参加反应的氧气的质量为
(A)16g (B)4g (C)2.4g (D)1.6g
26. 1个CO2分子和1个SO2分子中,一样多的是
(A)氧分子数 (B)氧原子数 (C)电子数 (D)氧元素的质量分数
27.北京地区空气质量日报公布的污染物中不包括
(A)二氧化硫 (B)二氧化碳 (C)一氧化碳 (D)可吸入颗粒物
28. 根据下列原子结构示意图判断,属于金属元素的是
1
2
+11
8
6
2
+8
7
2
+17
8
6
2
+16
8
(A) (B) (C) (D)
29. 1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量的新值。铟元素的核电荷数为49,相对原子质量为115,铟原子的质子数为
(A)115 (B)49 (C)66 (D)164
30. 下列化学方程式书写错误的是
点燃
(A)加热高锰酸钾: KMnO4 → KMnO2 + O2↑
通电
(B)镁在氧气中燃烧:2Mg + O2 → 2MgO
点燃
(C)电解水: 2H2O → 2H2↑ + O2↑
(D)木炭在氧气中充分燃烧: C + O2 → CO2
31. 硝酸的化学式为HNO3,其中氮元素的化合价为
(A)-3 (B)+2 (C)+3 (D)+5
32. 山梨酸(C6H8O2)是一种安全的食品防腐剂。下列说法正确的是
(A)山梨酸的相对分子质量为29
(B)山梨酸中碳、氢、氧的质量比为3:4:1
(C)每个山梨酸分子中含有16个原子
(D)山梨酸中碳元素的质量分数为10.7%
33. 化学知识中有很多的“相等”。请你判断下列说法中不正确的是
(A)溶液稀释前后,溶质的质量相等
(B)化合物中,元素正化合价数值等于负化和价数值
(C)50mL的水和50mL的酒精混合,所得溶液的体积等于100mL
(D)50g水和50g酒精混合,所得溶液的质量等于100g
34. 蜡烛在空气中燃烧,蜡烛质量逐渐变小。这说明
(A)物质可以自生自灭 (B)发生的不是化学变化
(C)不遵守质量守恒定律 (D)生成物为气体,散发到空气中了
35. 下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是
(A)NaCl (B)Fe (C)O2 (D) H
第Ⅱ卷(非选择题 45分)
二、填空题(共22分,每空1分)
36.(2分)请分别写出你所学过的氧气和二氧化碳的一种用途:
(1)氧气可用于_____________________;(2)二氧化碳可用于__________________。
37.(6分)按要求写出下列反应的化学方程式并在括号内注明反应的基本类型:
(1)铁在充足的氧气中燃烧
______________________________________ ( )
(2)实验室加热高锰酸钾制氧气
__________________________________________________( )
(3)实验室用双氧水制氧气(二氧化锰为催化剂)
_________________________________________________ ( )
38.(4分)用化学符号填空:
2个氮原子______________;2个氧分子______________;2个镁离子____________
+2价的钙元素________________。
39.(7分)化学学科的任务之一是研究物质组成,那么从宏观上来说,物质都是由________组成的;从微观上来说,物质是由_________、或__________、或________构成的。请以二氧化碳为例,说一说“CO2”这一化学式的含义(只答物质组成的含义):
(1) __________________________________
(2) __________________________________
(3) __________________________________________
40. (1分)下图为某物质的溶解度曲线图。对于该物质下列说法错误的是_____(填序号)
(A)A点的溶液是不饱和溶液
(B)50℃时的溶解度大于20℃时的溶解度
(C)将A点溶液降温至20℃时,将有晶体析出
(D)A、B点比较,B点溶液的溶质质量分数较大
41.(2分)在A + 2B → 2C的反应中,若32g物质A和足量物质B恰好完全反应,生成56g物质C,则参加反应的物质B的质量为________________。若 A的相对分子质量为32,则B的相对分子质量为_____________________。
三、实验题(共15分,每空1分)
42. (9分)下列是实验室常用的仪器:
⑧
单孔
请回答下列问题
(1) 图中仪器①的名称_______________,仪器④的名称_____________________。
(2) 实验室用石灰石和盐酸制取二氧化碳的化学方程式为:
______________________________________________________
(3) 选用上图所示的仪器组装一套制取二氧化碳的发生装置:
_____________________________(填编号)。
(4) 收集二氧化碳的方法是____________________,不选装置⑧收集二氧化碳的原因是_____________________________。
(5) 检验产生的气体是否是二氧化碳的方法是_______________________________。
(6) 下图为某同学设计并进行有关CO2性质的探究实验过程,请回答:
① 该实验的实验目的是_______________________________________________;
② 该实验得到的结论是_______________________________________________。
43.(6分)用固体氯化钠和水配制100g溶质质量分数为5%的氯化钠溶液,除用托盘天平、 药匙外,还需要的玻璃仪器有__________________、_________________、_______________________、_______________________;配制溶液的实验步骤包括①称量、②_________________、③__________________、④溶液倒入试剂瓶。
四、计算题(共8分)(最后结果保留在小数点后一位)
44. (2分)在农业科研上,有时用10%~20%的氯化钠溶液来选种。现需用30Kg 16%的氯化钠溶液,可用下述两种方法配制。
(1) 若用氯化钠固体和水配制上述溶液,需用氯化钠的质量____________Kg;
(2) 若用25%的氯化钠溶液和水配制上述溶液,需用25%氯化钠溶液的质量是 ____________________Kg。
45.(6分)下图是“×××钙片商品标签图”
×××儿童咀嚼片
(60片装)
[主要成分]碳酸钙,维生素D
[规格]2.5g/片,每片中含碳酸钙≥1.24g,维生素D 100l.U.
[食用方法]嚼食,每天一片
[功效]补钙
根据标签内容信息,计算回答下列问题:
(1) 主要成分碳酸钙中钙元素的质量分数为______________,每片中至少含钙元素的质量为______________________g。
(2) 小红同学为测定其碳酸钙的含量标注是否属实,她取出4片钙片,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g。称量烧杯中剩余物为47.8g(不含烧杯质量,假定钙片其他成分不与稀盐酸反应)。
试计算:①生成二氧化碳的质量;
②稀盐酸中溶质的质量分数;
③通过计算判断钙片中碳酸钙的含量标注是否属实。
初 三 化 学 参 考 答 案
一、选择题(共35分,每小题1分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
C
D
C
C
B
A
A
C
D
题号
11
12
13
14
15
16
17
18
19
20
答案
B
A
A
D
B
C
D
C
A
B
题号
21
22
23
24
25
26
27
28
29
30
答案
D
D
A
C
D
B
B
A
B
A
题号
31
32
33
34
35
答案
D
C
C
D
B
二、填空题(共22分,每空1分)
36. (2分)略。答案正确合理即给分。
+2
Ca
37.(6分)略。
38.(4分)2N 2O2 2Mg2+
39.(7分)元素 原子 分子 离子
(1) 二氧化碳由碳、氧两种元素组成
(2) 二氧化碳由二氧化碳分子构成
(3) 二氧化碳分子是由1个碳原子和2个氧原子构成
40.(1分)D
41.(2分)24g 12
三、实验题(共15分,每空1分)
42. (9分,每空1分)
(1)锥形瓶 长颈漏斗
(2)CaCO3 + 2HCl → CaCl2 + H2O + CO2 ↑
(3)①⑥ (或③⑥、 或①④⑤、 或③④⑤)
(4)向上排空气法 CO2能溶于水
(5)将气体通入澄清的石灰水
(6)①比较二氧化碳和空气的密度大小; ②二氧化碳密度比空气密度大
43.(6分) 量筒、胶头滴管、烧杯、玻璃棒 量取 溶解
四、计算题(共10分)(最后结果保留在小数点后一位)
44. (2分)(1)4.8 (2)19.2
45.(6分)(1)40% ……(1分) 0.496(或0.5) …………(1分)
(2)解:①根据质量守恒定律可知。生成二氧化碳的质量为:
40g + 4×2.5g - 47.8g = 2.2g …………………(1分)
② 设参加反应的CaCO3和HCl的质量分别为x和y
CaCO3 + 2HCl → CaCl2 + H2O + CO2 ↑
100 73 44
x y 2.2g
= x = 5g
= y = 3.65g ……(1分)
则稀盐酸中溶质的质量分数为:
×100% = 9.13% (或9.1%) ……(1分)
③每片中含CaCO3的质量为: =1.25g>1.24g,故钙片中碳酸钙的含量标注属实。 ……………………(1分)
答:①生成二氧化碳的质量为2.2g;②稀盐酸中溶质的质量分数为9.13%; ③通过计算判断钙片中碳酸钙的含量标注属实。您好,欢迎您阅读我的文章,本WORD文档可编辑修改,也可以直接打印。阅读过后,希望您提出保贵的意见或建议。阅读和学习是一种非常好的习惯,坚持下去,让我们共同进步。