- 1.30 MB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
东城区2018-2019学年度第二学期高三综合练习(一)
理科综合 2019.4
第一部分(选择题 共120分)
可能用到的相对原子质量:H 1 C 12 O 16
本部分共20小题,每小题6分,共120分。在每小题列出的四个选项中,选出最符合题目要求的一项。
1.感冒患者在发热门诊治疗时,医生会根据主要病原体是病毒还是细菌采取不同的治疗措施。引起感冒的病毒和细菌都可以
A. 利用自身核糖体合成蛋白质 B. 将有机物分解为CO2和H2O
C. 通过细胞分裂进行增殖 D. 诱导机体免疫反应产生抗体
2.以下有关叶绿体中类囊体的叙述不正确的是
A.类囊体膜的基本支架是磷脂双分子层 B.类囊体可增大叶绿体的受光面积
C.类囊体上有可以催化形成ATP的酶 D.类囊体上可发生C3的还原过程
3.大鼠神经元单独培养时,其轴突侧支返回细胞体,形成自突触(图1)。电极刺激这些形成了自突触的神经元细胞体引起兴奋,电位变化结果如图2。部分神经元电位变化为曲线①,其余神经元为曲线②。用谷氨酸受体抑制剂处理上述所有神经元后,再进行相同刺激,测定结果为曲线③。以下叙述不正确的是
A.静息时自突触神经元细胞膜内外存在电位差
B.曲线①的a峰表明这些神经元再次产生神经冲动
C.发生曲线②变化的神经细胞膜上无谷氨酸受体
D.谷氨酸可以使突触后膜发生阳离子内流
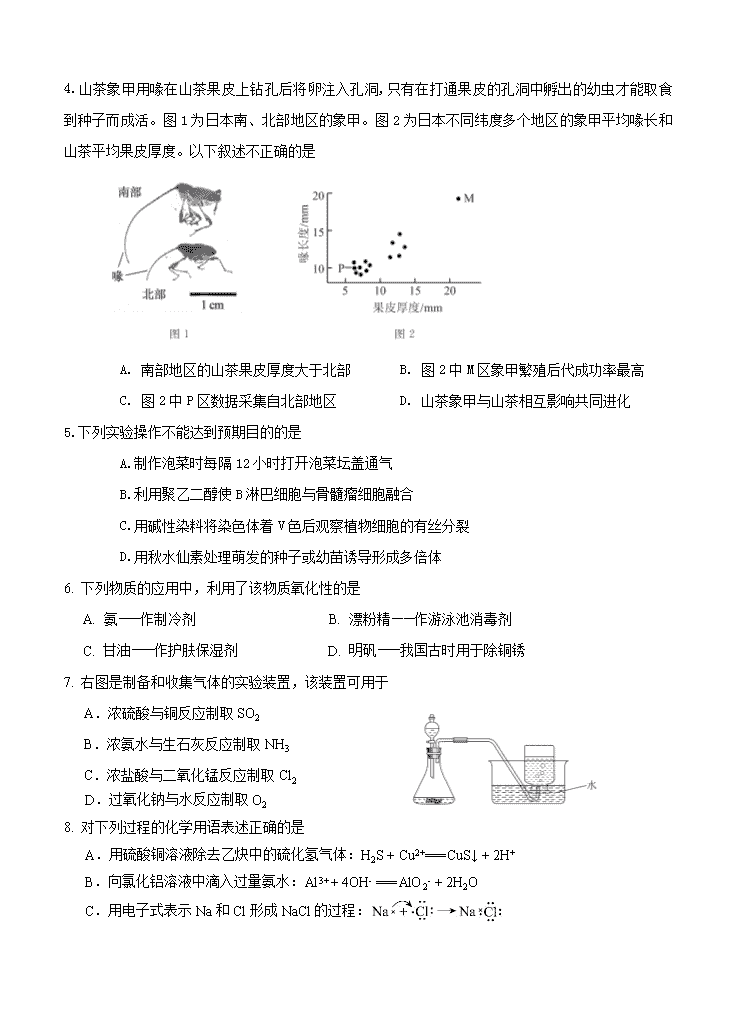
4.山茶象甲用喙在山茶果皮上钻孔后将卵注入孔洞,只有在打通果皮的孔洞中孵出的幼虫才能取食到种子而成活。图1为日本南、北部地区的象甲。图2为日本不同纬度多个地区的象甲平均喙长和山茶平均果皮厚度。以下叙述不正确的是
A. 南部地区的山茶果皮厚度大于北部 B. 图2中M区象甲繁殖后代成功率最高
C. 图2中P区数据采集自北部地区 D. 山茶象甲与山茶相互影响共同进化
5.下列实验操作不能达到预期目的的是
A.制作泡菜时每隔12小时打开泡菜坛盖通气
B.利用聚乙二醇使B淋巴细胞与骨髓瘤细胞融合
C.用碱性染料将染色体着V色后观察植物细胞的有丝分裂
D.用秋水仙素处理萌发的种子或幼苗诱导形成多倍体
6. 下列物质的应用中,利用了该物质氧化性的是
A. 氨——作制冷剂 B. 漂粉精——作游泳池消毒剂
C. 甘油——作护肤保湿剂 D. 明矾——我国古时用于除铜锈
7. 右图是制备和收集气体的实验装置,该装置可用于
A.浓硫酸与铜反应制取SO2
B.浓氨水与生石灰反应制取NH3
C.浓盐酸与二氧化锰反应制取Cl2
D.过氧化钠与水反应制取O2
8. 对下列过程的化学用语表述正确的是
A.用硫酸铜溶液除去乙炔中的硫化氢气体:H2S + Cu2+=== CuS↓ + 2H+
B.向氯化铝溶液中滴入过量氨水:Al3+ + 4OH- === AlO2- + 2H2O
C.用电子式表示Na和Cl形成NaCl的过程:
D.钢铁发生电化学腐蚀的正极反应:Fe-3e- === Fe3+
9. 为纪念门捷列夫发表第一张元素周期表(部分如下)150周年,联合国宣布2019年为“国际化学元素周期表年”。关于下表的说法正确的是
A. 表中数字代表元素的原子序数
B. 表中元素的排列依据是元素的原子结构
C. 推测表中“?=70”指代的元素的最高化合价为+4
D. 每一纵行(列)都对应现在常用的元素周期表中的一族
10.凯夫拉是一种高强度、耐腐蚀的芳纶纤维,军事上称为“装甲卫士”,但长期浸渍在强酸或强碱中强度有所下降。下表中是凯夫拉的两种结构:
名称
芳纶1313(PMTA)
芳纶1414(PPTA)
结构
简式
以下说法不正确的是
A.PMTA和PPTA互为同分异构体
B.“芳纶1313”、“芳纶1414”中的数字表示苯环上取代基的位置
C.凯夫拉在强酸或强碱中强度下降,可能与“”的水解有关
D.以和为原料制备PPTA的反应为缩聚反应
温度T/℃
1000
1150
1300
平衡常数K
4.0
3.7
3.5
11. 高炉炼铁过程中发生反应:
Fe2O3(s)+CO(g) Fe(s)+CO2(g),
该反应在不同温度下的平衡常数见右表。
下列说法正确的是
A.增加高炉的高度可以有效降低炼铁尾气中CO的含量
B.由表中数据可判断该反应:反应物的总能量>生成物的总能量
C.为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D.1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO表示该反应的平均速率为 mol/(L·min)
12. 空气中的硫酸盐会加剧雾霾的形成,我国科学家用下列实验研究其成因:反应室底部盛有不同吸收液,将SO2和NO2按一定比例混合,以N2或空气为载气通入反应室,相同时间后,检测吸收液中的含量,数据如下:
反应室
载气
吸收液
SO42-含量
数据分析
①
N2
蒸馏水
a
ⅰ. b≈d>a≈c
ⅱ.若起始不通入NO2,则最终检测不到SO42-
②
3%氨水
b
③
空气
蒸馏水
c
④
3%氨水
d
下列说法不正确的是
A. 控制SO2和氮氧化物的排放是治理雾霾的有效措施
B. 反应室①中可能发生反应:SO2 + 2NO2 + 2H2O === H2SO4 + 2HNO2
C. 本研究表明:硫酸盐的形成主要与空气中O2有关
D. 农业生产中大量使用铵态氮肥可能会加重雾霾的形成
13.下列核反应方程中,属于α衰变的是
A. B.
C. D.
14.下列说法正确的是
A.同一个物体,运动时的内能一定比静止时的内能大
B.物体温度升高,组成物体的分子平均动能一定增加
C.一定质量的物体,内能增加,温度一定升高
D.温度升高时物体的每个分子的动能都将增大
15.如图,两束单色光A、B分别沿半径方向由空气射入半圆形玻璃砖,出射时合成一束复色光P,下列说法正确的是
A. A光的频率小于B光的频率
B.在玻璃砖中A光的传播速度小于B光的传播速度
C.玻璃砖对A光的折射率大于对B光的折射率
D.两种单色光由玻璃射向空气时,A光的临界角较小
16.一列横波沿x轴正方向传播,若t=0时刻的波形图如图甲所示,则图乙描述的可能是哪个质点的振动图像
A.x=0处的质点 B.x=0.5 m处的质点
C.x=1.5 m处的质点 D.x=2.5 m处的质点
17.2018年12月我国成功发射嫦娥四号探测器.2019年1月嫦娥四号成功落月,我国探月工程四期和深空探测工程全面拉开序幕。假设探测器仅在月球引力作用下,在月球表面附近做匀速圆周运动.可以近似认为探测器的轨道半径等于月球半径。已知该探测器的周期为T.万有引力常量为G。根据这些信息可以计算出下面哪个物理量
A.月球的质量 B.月球的平均密度
C.该探测器的加速度 D.该探测器的运行速率
18.如图甲所示,直线AB是某电场中的一条电场线。一正电荷在该电场中运动,始终只受到电场力作用。已知该正电荷沿电场线从A点运动到B点的过程中,其速度平方与位移x的关系如图乙所示。、。表示A,B两点的电场强度,、表示A、B
两点的电势。以下判断正确的是
A. <
B. >
C. >
D. <
19.下面四幅图是用来“探究感应电流的方向遵循什么规律”的实验示意图。灵敏电流计和线圈组成闭合回路,通过“插入”“拔出”磁铁,使线圈中产生感应电流,记录实验过程中的相关信息,分析得出楞次定律。下列说法正确的是
A.该实验无需确认电流计指针偏转方向与通过电流计的电流方向的关系
B.该实验无需记录磁铁在线圈中的磁场方向
C.该实验必需保持磁铁运动的速率不变
D.该实验必需记录感应电流产生的磁场方向
20.将一质量为M的光滑斜劈固定在水平面上一质量为M的光滑滑块(滑块可以看成质点)从斜面顶端由静止自由滑下.在此过程中,斜劈对滑块的支持力记为,地面对斜劈的支持力记为,滑块到达斜面底端时,相对地面的速度大小记为v、竖直分速度的大小记为。若取消固定斜劈的装置.再让滑块从斜面顶端由静止下滑.在滑块的压力作用下斜劈会向左做匀加速运动.在此过程中.斜劈对滑块的支持力记为'、地面对斜劈的支持力记为',滑块到达斜面底端时,相对地面的速度大小记为v'、竖直分速度的大小记为’。下面大小关系正确的是
A.<'
B.<'
C. v< v'
D.<’
第二部分 非选择题
21.实验题(18分)
(1)(5分)某同学用图甲所示的装置来脸证动量守恒定律,A、B为半径相同的小球((mA>mB),图中PQ是斜槽,QR为水平槽。实验时先使A球从斜槽上某一位置G由静止释放,落到位于水平地面的记录纸上,留下痕迹。重复上述操作多次,得到多个落点痕迹。再把B球放在水平槽上靠近槽末端的地方,让A球仍从位置G由静止释放.两球碰撞后.A、B球分别在记录纸上留下各自的落点痕迹,重复这种操作多次。图甲中O点是水平槽末端R在记录纸上的竖直投影点。B球落点痕迹如图乙所示,图中米尺的零刻度线与O点对齐(未画出)。
①碰撞后B球的水平射程应为 cm;
②以下选项,哪些是本次实验必须进行的测量? (填选项前的字母)
A.测量A球未与B球相碰时的平均落点到O点的距离
B.测量A球与B球相碰后的平均落点到O点的距离
C.测量A球和B球的直径
D.测量A球和B球的质量
E.测量水平槽面相对于O点的高度
(2)(13分)如图所示的电路图是利用半偏法测量一块电流计G(量程300A,内阻100Ω到200Ω之间)的内阻。
现有器材如下:
A.直流电源(输出电压12 V)
B.电阻箱(999. 9Ω)
C.滑动变阻器(500Ω)
D.电位器(5kΩ)
E.电位器(50kΩ)
①电阻器选用 ,电阻器选用 。(填器材前的字母)
②为了测定电流计G的内阻,在接通电路前,先把电阻器R1、的阻值调到最大。然后操作
步骤依次是 (填选项前的字母),最后记录R2的阻值.
A.闭合
B.闭合
C.调节的阻值,使电流计指针偏转到满刻度
D.调节的阻值.使电流计指针偏转到满刻度的一半
E.调节的阻值.使电流计指针偏转到满刻度的一半
F.调节的阻值.使电流计指针偏转到满刻度
③若电流计半偏时,R2的阻值为120.0Ω,则电流计内阻Rg的测量值为_ Ω,由于存在系统误差,该测量值 电流计内阻的真实值(填“大于”或“小于”)。造成这种误差的原因是 。
22.(16分)
为了迎接2022年冬季奥运会,让更多的人感受运动的快乐,北京在许多游乐场增设了坡面场地.坡而场地可以看作由一个斜坡平面和一个水平面衔接而成。如图所示.已知某坡面场地的斜面高为h.斜面倾角为θ。某同学坐在保护垫上,从斜面顶端A由静止开始沿着斜而AC下滑.最终停在水平面上的D点.该同学与保护垫的总质量为m,保护垫与斜面、水平面间的滑动摩擦因数均为声。(人与垫可看作质点处理,忽略衔接处的速率变化及空气阻力)。求:
(1)保护垫与斜面间的滑动摩擦力大小?
(2)该同学滑到斜面底端时的速度大小?
(3)该同学从A到D运动过程中,摩擦产生的总热量为多少?
23.(18分)
能量守恒是自然界基本规律,能量转化通过做功实现。
(1)如图甲所示,质量为m的小球在自由下落过程中只受到重力作用,小球经过A点的速率为,经过B点的速率为。以地面为重力势能的零势能面,小球在A点的重力势能为=,在B点的重力势能为=。请根据动能定理证明:小球在A、B两点的机械能相等。
(2)如图乙所示,平行板电容器水平放置,上板正中央有一小孔,两极板间的距离为d,电势差为U。一质量为)m、带电量为+q的小球从小孔正上方某处由静止开始下落,穿过小孔到达下极板处速度恰为零。重力加速度为g(空气阻力忽略不计)。求:小球释放位置距离上极板的高度h。
(3〕研究发现,电容器存储的能最表达式为=,其中U为电容器两极板间的电势差.C为电容器的电容。现将一电容器、电源和某定值电阻按照如图丙所示电路进行连接。已知电源电动势为,电容器电容为,定值电阻阻值为R,其他电阻均不计,电容器原来不带电。现将开关S闭合,一段时间后,电路达到稳定状态。求:在闭合开关到电路稳定的过程中,该电路因电磁辐射、电流的热效应等原因而损失的能量。
24. (20分)
伽利略在研究自出落体运动时,猜想自由落体的速度是均匀变化的,他考虑了速度的两种变化:一种是速度随时间均匀变化,另一种是速度随位移均匀变化。
(1)现在我们已经知道.自由落体运动是速度随时间均匀变化的运动。有一种“傻瓜”照相机的曝光时间极短,且固定不变。为估测“傻瓜”照相机的曝光时间,实验者从某砖墙前的高处使一个石子自由落下,拍摄石子在空中的照片如图甲所示。由于石子的运动,它在照片上留下了一条模糊的径迹。已知石子在A点正上方1.8m的高度自由下落.每块砖的平均厚度为6.0cm.(不计空气阻力,g取10m/s2)
a.计算石子到达A点的速度大小;
b.估算这架照相机的曝光时间(结果保留一位有效数字〕。
(2)速度随位移均匀变化的运动也确实存在。已知一物体做速度随位移均匀变化的变速直
线运动.其速度与位移的关系式为v=+kx(为初速度,v为位移为x时的速度).
a.证明:此物体运动的加速度α和速度v成正比,且比例系数为k;
b.如图乙所示,两个光滑的水平金属导轨间距为L,左侧连接有阻值为R的电阻.磁感应强度为B的匀强磁场垂直穿过导轨平面。有一质量为m的导体棒以初速度向右运动,导体棒始终与导轨接触良好。除左边的电阻R外,其他电阻均不计。已知棒的运动是速度随位移均匀变化的运动,即满足关系式v=+kx。设棒向右移动最远的距离为s(s未知),求k值及当棒运动到s时((0<<1)电阻R上的热功率。
25.(15分)抗心律失常药物心律平的合成路线如下:
OH-
Cl2
ⅱ.酸化
I
C18H18O3
H2
Pd/C
F
G
C15H12O2
H
C15H14O2
E
C3H5OCl
J
C21H27NO3
CH3CH2CH2NH2
HCl
ⅰ.C7H6O/OH-、△
A
C3H6
B
C3H5Cl
Cl2
500℃
C
C3H6O
D
C3H6OCl2
OH-
(心律平)
已知:① R-OH + Cl-R´ OH-
R-O-R´ + HCl
OH-
△
② R-CHO + + H2O
请回答:
(1)A属于链烃,则A中所含的官能团是 。
(2)B中无甲基,A→B的反应类型是 反应。
(3)C的结构简式是 。
(4)E中含有三元环,且无羟基,则D→E的化学方程式是 。
(5)结合官能团的性质,解释F→G的转化中需酸化的原因: 。
(6)H的结构简式是 。
(7)I→J的化学方程式是 。
(8)在I→J的反应中,生成J的同时会有副产物K,K与J互为同分异构体,则K的结构简式是 。
26.(13分)软锰矿在生产中有广泛的应用。
IV
某软锰矿
(含MnO2、FeS2等)
MnSO4
溶液
锰钢原料:Mn单质
软磁原料:Mn3O4
锂电池电极原料:MnCO3
I
II
III
(1)过程I:软锰矿的酸浸处理
① 酸浸过程中的主要反应(将方程式补充完整):
2FeS2+□MnO2+□ === □Mn2++2Fe3++4S+□ 。
② 生成的硫附着在矿粉颗粒表面使上述反应受阻,此时加入H2O2,利用其迅速分解产生的大量气体破除附着的硫。导致H2O2迅速分解的因素是 。
③ 矿粉颗粒表面附着的硫被破除后,H2O2可以继续与MnO2反应,从而提高锰元素的浸出率,该反应的离子方程式是 。
(2)过程II:电解法制备金属锰
金属锰在 (填“阳”或“阴”)极析出。
氨水
过滤
(3)过程III:制备Mn3O4
加蒸馏水
洗涤后
MnSO4
溶液
O2
Mn3O4
固体
滤饼[含Mn(OH)2、
Mn2(OH)2SO4]
右图表示通入O2时pH随时间的变化。15~150分钟滤饼中一定参与反应的成分是 ,判断的理由是 。
(4)过程Ⅳ:制备MnCO3
MnCO3难溶于水、能溶于强酸,可用MnSO4溶液和NH4HCO3溶液混合制备。
每制得1 mol MnCO3,至少消耗a mol/L NH4HCO3溶液的体积为 L。
27.(15分)富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
Fe(OH)3
Al(OH)3
Fe(OH)2
Mg(OH)2
开始沉淀时
1.9
3.4
7.0
9.1
完全沉淀时
3.2
4.7
9.0
11.1
(1)上述流程中能加快反应速率的措施有 、 等。
(2)酸浸时发生反应:
2MgO·SiO2 + 2H2SO4 2MgSO4 + SiO2 + 2H2O
2MgO·B2O3+ 2H2SO4 + H2O 2H3BO3 + 2MgSO4
① 上述反应体现出酸性强弱:H2SO4 H3BO3(填“>”或“<”)。
② 酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式: 、 。
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH- B(OH)4-。
下列关于硼酸的说法正确的是 (填序号)。
a. 硼酸是一元酸
b. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
c. 硼酸的电离方程式可表示为:H3BO3 + H2OB(OH)4-+H+
(3)检验褐色浸出液中的杂质离子:取少量浸出液, (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子: 用MgO调节溶液的pH至 以上,使杂质离子转化为 (填化学式)沉淀,过滤。
注:温度较高时,硼酸会随水蒸气挥发
(5)获取晶体:
ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。
结合右图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中, (将方法补充完整)。
28.(15分)某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。
已知:
物质
BaSO4
BaCO3
AgI
AgCl
溶解度/g(20℃)
2.4×10-4
1.4×10-3
3.0×10-7
1.5×10-4
(1)探究BaCO3和BaSO4之间的转化
实验操作:充分振荡后
3滴0.1 mol/L A溶液
2 mL 0.1 mol/L B溶液
1 mol/L C溶液
充分振荡后,
过滤,取洗净后的沉淀
足量稀盐酸
试剂A
试剂B
试剂C
加入盐酸后的现象
实验Ⅰ
BaCl2
Na2CO3
Na2SO4
……
实验Ⅱ
Na2SO4
Na2CO3
有少量气泡产生,沉淀部分溶解
实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后, 。
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是 。
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因: 。
(2)探究AgCl和AgI之间的转化
实验Ⅲ:充分振荡后
3滴0.1 mol/L乙溶液
2 mL 0.1 mol/L甲溶液
0.1 mol/L KI(aq)
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置
步骤
电压表
读数
ⅰ.如图连接装置并加入试剂,闭合K
a
ⅱ.向B中滴入AgNO3(aq),至沉淀完全
b
ⅲ.再向B中投入一定量NaCl (s)
c
ⅳ.重复ⅰ,再向B中加入与ⅲ等量NaCl(s)
a
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是 (填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是 。
③ 结合信息,解释实验Ⅳ中b<a的原因: 。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是 。
(3)综合实验Ⅰ~Ⅳ,可得出结论: 。
29.(18分)植物对病原微生物的防御反应包含多种物质介导的多条途径,其中水杨酸(SA)和茉莉酸(JA)可以诱导植物合成防御素等物质,引发防御反应。
(1)科研人员选用野生型和E3基因功能缺失突变体拟南芥,分别用一定浓度的SA、JA溶液处理,然后从各组植株中提取_________,反转录形成cDNA,再运用______技术扩增,进而检测防御素合成关键基因PDF的转录水平,结果见图1。
野生型的实验结果可说明,SA和JA对PDF基因转录的作用存在______关系。比较两组实验结果可知SA和JA的作用与E3有关。
科研人员构建含有E3基因的Ti质粒,利用___________法将其导入E3功能缺失突变体拟南芥,重复上述处理后进行测定。若实验结果为__________________,则支持上述结论。
(2)PDF基因转录过程需要ORA蛋白激活。科研人员依据以下原理研究了E3蛋白与ORA蛋白之间的关系。原理如下:在酵母菌细胞中,可以利用基因工程表达出两种融合蛋白(BD—待测蛋白X、AD—待测蛋白Y)。如图2a,若两种待测蛋白可以相互作用,则AD蛋白和BD蛋白就能充分接近形成复合物,并启动组氨酸合成基因的转录;否则组氨酸合成基因不能转录(如图2b)。
由此,科研人员构建两种重组载体(见下表),将它们导入不能合成亮氨酸、色氨酸和组氨酸的缺陷型酵母菌中。
重组载体包含的部分基因
载体1
AD蛋白基因 E3蛋白基因 亮氨酸合成基因
载体2
① 基因 ② 基因 色氨酸合成基因
上表中的相应基因分别为①____________;②____________。
将转基因酵母菌接种到不含亮氨酸、色氨酸和___________的固体培养基上进行培养,观察到____________,说明E3蛋白可以与ORA蛋白相互作用。
(3)科研人员进一步研究SA在调控PDF基因转录过程中与E3和ORA的关系,结果如图3、图4所示。
分析图3可知, SA可以促进ORA基因转录,且该过程与E3无关。判断依据:与对照组相比,SA处理后的野生型和突变体中的ORA基因转录量______________。
研究还发现,SA可以使E3蛋白增多。结合(2)结论和图3、图4,推测SA调节ORA蛋白量的机制是_____________,进而调控PDF基因的转录过程。
30.(18分) 杂交水稻为解决我国粮食问题作出了巨大贡献。水稻籼、粳亚种间杂交稻可能比现有的杂交稻单产提高,但目前面临的问题是两者杂交子代会出现花粉不育的现象。
(1)科研人员研究上述现象的遗传机制时发现,水稻7号染色体上名为qH7的片段与此密切相关。他们用粳稻品种D(qH7片段的遗传组成为DD,花粉100%可育)与籼稻品种M(qH7片段的遗传组成为MM,花粉100%可育)进行杂交,得到水稻品系N(qH7片段的遗传组成为DM)。品系N的表现型为花粉50%可育。品系N自交,子代结果如下表所示:
自交子代遗传组成及数量
DM(236株)
DD(242株)
表现型(可育花粉占比)
50%
100%
实验结果说明品系N产生的含有__________的花粉是不育的。据此推测水稻品系N(♂)与水稻品种D(♀)杂交子代的遗传组成为_________,表现型为____________。
(2)为进一步研究上述花粉不育的机理,科研人员对水稻品系N(DM)的7号染色体qH7片段进行测序和分析,结果如图1所示。
图1
科研人员利用基因工程向水稻品系N(DM)的体细胞中导入基因F,获得转基因杂合植株A。植株A的遗传组成为DMF-(F-表示在qH7区域外含有一个基因工程导入的F基因)。植株A自交,子代结果如图2所示。
① 据图2分析,利用基因工程导入的基因F插入到了______染色体上。基因F的功能是__________。
②上述结果说明品系N 的花粉50%不育与基因ED有关,据图2简述理由______________。
③为确定②的结论是否正确,最佳方案是将ED基因导入________的愈伤组织中,培育转基因植株。
A. 品种D B.品种M C. 品系N D. 植株A
若转基因植株的表现型为________________,则支持该结论。
(3)物种之间存在__________
,从生物进化的角度分析,上述导致杂交水稻部分花粉不育的基因是新物种形成的分子基础。
31. (14分)
内质网是真核细胞中重要的细胞器。一些细胞内外的因素会使内质网功能紊乱,引起内质网应激(ERS),甚至启动细胞凋亡。
(1)在核糖体上氨基酸形成的肽链进入内质网进行________,形成具有一定___ 结构的蛋白质。
(2)正常情况下,内质网膜上的PERK与Bip结合后保持失活状态。但当细胞受到一定刺激后,内质网腔内积累大量错误折叠的蛋白质,扰乱细胞内环境,导致如图1所示内质网应激(ERS)的一系列反应。由于错误折叠蛋白质对Bip的亲和力_______PERK对Bip的亲和力,使PERK发生磷酸化被激活,p-PERK(磷酸化PERK)促进eIF2α的磷酸化,进而阻止新生蛋白质的合成,这是__________调节机制。在持续而严重的ERS条件下,p-eIF2α(磷酸化eIF2α)还促进有关转录因子的合成,通过调节相关基因的________,降低抗凋亡蛋白BCL-2的含量,提高促凋亡蛋白Bax的含量,诱导受损细胞凋亡。
(3)丹参是我国的一种传统中药,研究人员对其有效成分丹参二萜醌的抗肿瘤作用展开实验。用丹参二萜醌处理肺癌PC9细胞24小时后测定凋亡率(如图2)。实验结果表明_________________。为了验证丹参二萜醌对PC9细胞的上述作用是通过影响PERK并经图1所示途径完成,请提出研究思路并预测实验结果:___________。
生物试题答案
1.D 2.D 3.C 4.B 5.A
29.(18分)
(1)RNA PCR(1分) 拮抗 农杆菌转化
PDF基因转录量相对值与野生型组相似
(2)BD蛋白 ORA蛋白 (两空都写对得2分) 组氨酸(1分) 酵母菌菌落
(3)增加且增加的量没有显著差异
SA使E3蛋白增多,E3蛋白与ORA蛋白相互作用使其降解
30. (18分)
(1) M DD 花粉100%可育
(2)①非7号 恢复M型花粉的可育性
② MMF-的花粉100%可育,而DMF-的花粉只有75%可育,说明花粉不育与D中基因有关,而基因F可以恢复M型花粉育性,因此基因ED导致M型花粉不育(3分)
③B 花粉100%不育
(3)生殖隔离(1分)
31. (14分)
(1)加工 空间
(2)大于 反馈 表达
(3)丹参二萜醌促进肺癌PC9细胞凋亡;浓度越高促进凋亡效果越好
研究思路:用丹参二萜醌处理肺癌PC9细胞,检测处理后与未经处理的细胞中相关物质的含量
预测结果:与未处理细胞相比,处理后细胞内的p-PERK、p-eIF2α、有关转录因子、Bax含量增多,BCL-2含量减少
北京市东城区2018-2019学年度第二学期高三综合练习(一)2019.4
理科综合参考答案(化学部分)
6.B 7.D 8.A 9.C 10.A 11.B 12.C
25.(15分)
(1)碳碳双键(或C=C)
(2)取代
(3)CH2 == CHCH2OH
(4)
(5)F中的酚羟基具有弱酸性,在碱性条件下成盐,最终用酸将酚羟基复原
(6)
(7)
(8)
26.(13分)
(1)①
② Fe3+(或Mn2+或MnO2)等作催化剂
③ MnO2 + H2O2 + 2H+ === Mn2+ + O2↑ + 2H2O
(2)阴
(3)Mn2(OH)2SO4
Mn2(OH)2SO4被O2氧化产生H+,而Mn(OH)2被O2氧化不产生H+
(4)
27.(15分)
(1)研磨 加热
(2)①> ② Al2O3 + 6H+ === 2Al3+ + 3H2O FeO + 2H+ === Fe2+ + H2O
③ a c
(3)滴加K3[Fe(CN)6]溶液,产生蓝色沉淀(合理答案给分)
(4)4.7 Al(OH)3、Fe(OH)3
(5)升温结晶,得到硫酸镁晶体,分离后,再将母液降温结晶,分离得到硼酸晶体
28.(15分)
(1)① 沉淀不溶解或无明显现象
② BaCO3 + 2H+ === Ba2+ + CO2↑+ H2O
③ BaSO4在溶液中存在BaSO4(s) Ba2+(aq) + (aq),当加入浓度较高的Na2CO3溶液,与Ba2+结合生成BaCO3沉淀,使上述平衡向右移动
(2)① b
② 2I- - 2e- === I2
③ 由于生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱
④ 实验ⅳ表明Cl-本身对该原电池电压无影响,则c>b说明加入Cl-使c(I-)增大,证明发生了AgI + Cl- AgCl + I-
(3)溶解度小的沉淀容易转化成溶解度更小的沉淀,反之则不易;溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现
物理答案
13、A 14、B 15、A
16、C 17、B 18、C 19、D 20、D
21、
22、
23、
24、
欢迎访问“高中试卷网”——http://sj.fjjy.org