- 290.00 KB
- 2021-05-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
北京市西城区2010年抽样测试
高三理科综合能力测试(化学部分) 2010.5
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Si 28 S 32
6.下列说法不正确的是
A.可用中和法处理酸性或碱性工业废水
B.垃圾填埋正成为垃圾处理的发展方向
C.使用纤维素和淀粉为原料制成的微生物降解塑料,可治理“白色污染”
D.向煤中加入适量石灰石,可减少其燃烧产物中的SO2,降低对大气的污染
7.下列说法正确的是
A.用氨水洗涤附着银镜的试管
B.用CCl4作萃取剂直接从海带中提取I2
C.用向下排空气法收集NH3,并用湿润的蓝色石蕊试纸验满
D.制乙炔时滴加饱和食盐水是为了减缓电石与水的反应速率
8.下列离子方程式书写不正确的是
A.Cl2通入FeCl2溶液中:Cl2+Fe2+=Fe3++2Cl-
B.Na2CO3溶液显碱性:CO32-+ H2OHCO3-+ OH-
C.Al和NaOH溶液反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
D.少量SO2通入氨水中:SO2+2NH3••H2O=2NH4++SO32-+H2O
9.X和Y元素的原子在化学反应中都容易失去电子,形成与Ne原子具有相同电子层结构的离子,且X的原子序数大于Y的原子序数。下列说法正确的是
A.X的金属性比Y的强
B.X的最高正化合价比Y 的高
C.常温下,X和Y的单质一定不与水反应
D.Y的最高价氧化物对应水化物的碱性比X的弱
放电
充电
10.Li-SO2电池具有输出功率高和低温性能好等特点。其电解质是LiBr,溶剂是碳酸丙烯酯和乙腈,电池反应为2Li + 2SO2 Li2S2O4。下列说法正确的是
A.该电池反应为可逆反应
B.放电时,Li+向负极移动
C.充电时,阴极反应式为Li+ + e-=Li
D.该电池的电解质溶液可以换成LiBr的水溶液
11.25℃时,下列关于分别由等体积0.1 mol/L的2种溶液混合而成的溶液的说法中,不正确的是
A.Ba(OH)2溶液与 Na2SO4溶液:pH=13
B.醋酸与CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.Na2CO3溶液与 NaOH溶液:c(Na+)>c(CO32-)>c(OH-)>c(H+)
D.Na2CO3溶液与 NaHCO3溶液:2c(Na+)=3c(CO32-) + 3c(HCO3-) + 3c(H2CO3)
800℃
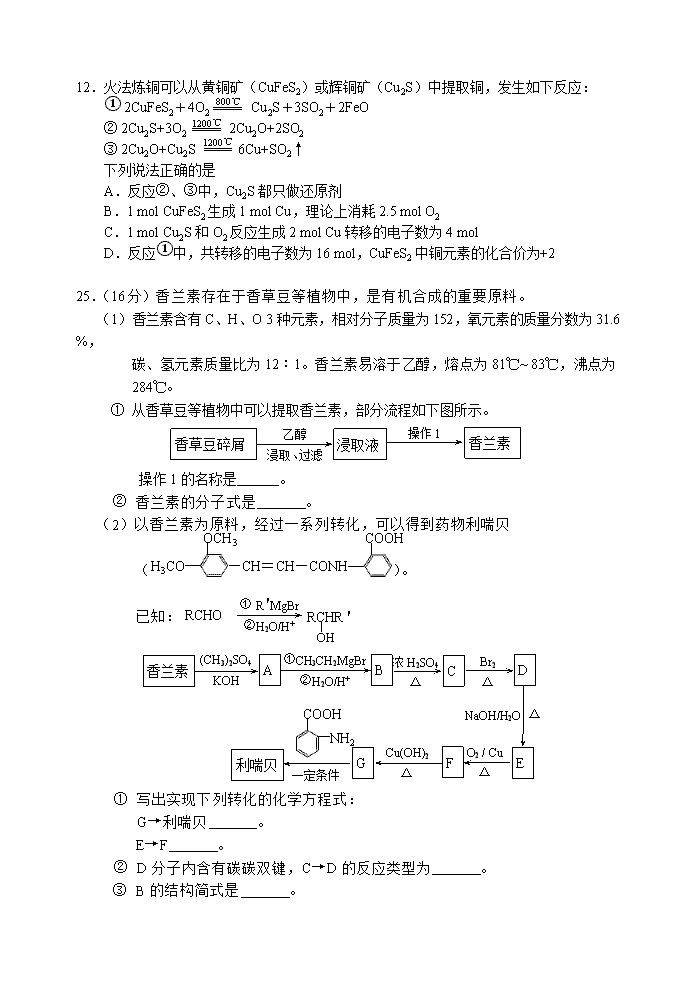
12.火法炼铜可以从黄铜矿(CuFeS2)或辉铜矿(Cu2S)中提取铜,发生如下反应:
1200℃
① 2CuFeS2+4O2 Cu2S+3SO2+2FeO
1200℃
② 2Cu2S+3O2 2Cu2O+2SO2
③ 2Cu2O+Cu2S 6Cu+SO2↑
下列说法正确的是
A.反应②、③中,Cu2S都只做还原剂
B.1 mol CuFeS2生成1 mol Cu,理论上消耗2.5 mol O2
C.1 mol Cu2S和O2反应生成2 mol Cu转移的电子数为4 mol
D.反应①中,共转移的电子数为16 mol,CuFeS2中铜元素的化合价为+2
25.(16分)香兰素存在于香草豆等植物中,是有机合成的重要原料。
(1)香兰素含有C、H、O 3种元素,相对分子质量为152,氧元素的质量分数为31.6 %,
碳、氢元素质量比为12︰1。香兰素易溶于乙醇,熔点为81℃~ 83℃,沸点为284℃。
乙醇
浸取、过滤
浸取液
香兰素
香草豆碎屑
操作1
① 从香草豆等植物中可以提取香兰素,部分流程如下图所示。
操作1的名称是 。
② 香兰素的分子式是 。
—CH=CH—CONH
OCH3
COOH
H3CO
(2)以香兰素为原料,经过一系列转化,可以得到药物利喘贝
( )。
RCHO
RCHR'
OH
① MgBr
②H2O/H+
R'
已知:
(CH3)2SO4
KOH
A
B
①CH3CH2MgBr
②H2O/H+
浓H2SO4
△
C
Br2
△
D
香兰素
E
NaOH/H2O
O2 / Cu
Cu(OH)2
△
F
G
一定条件
NH2
COOH
△
△
利喘贝
① 写出实现下列转化的化学方程式:
G→利喘贝 。
E→F 。
② D分子内含有碳碳双键,C→D的反应类型为 。
③ B的结构简式是 。
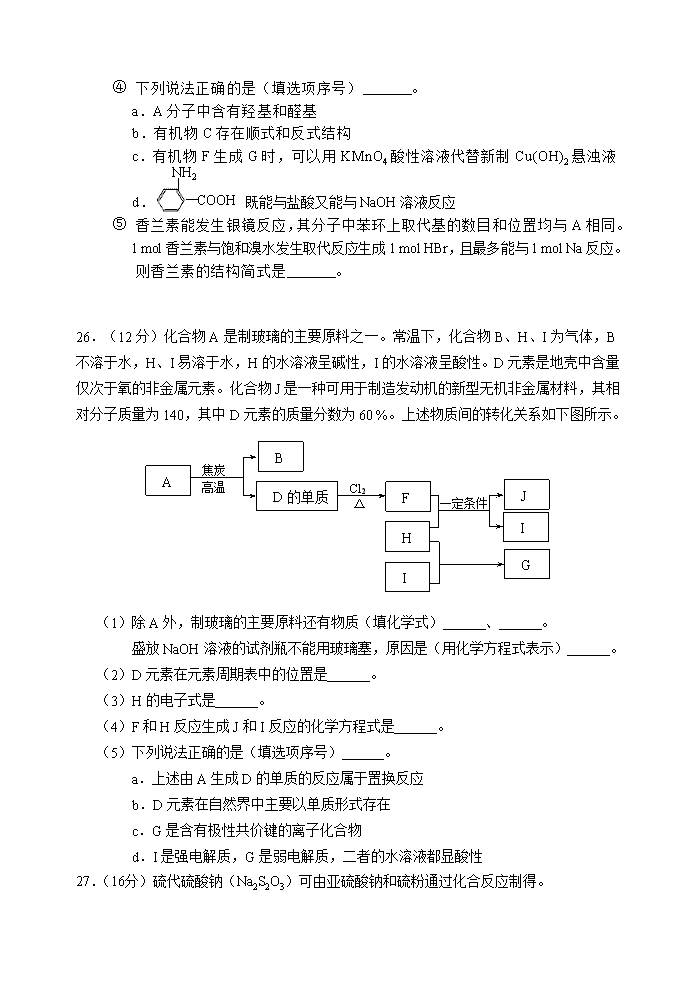
④ 下列说法正确的是(填选项序号) 。
a.A分子中含有羟基和醛基
b.有机物C存在顺式和反式结构
NH2
COOH
c.有机物F生成G时,可以用KMnO4酸性溶液代替新制Cu(OH)2悬浊液
d. 既能与盐酸又能与NaOH溶液反应
⑤ 香兰素能发生银镜反应,其分子中苯环上取代基的数目和位置均与A相同。
1 mol香兰素与饱和溴水发生取代反应生成1 mol HBr,且最多能与1 mol Na反应。
则香兰素的结构简式是 。
26.(12分)化合物A是制玻璃的主要原料之一。常温下,化合物B、H、I为气体,B不溶于水,H、I易溶于水,H的水溶液呈碱性,I的水溶液呈酸性。D元素是地壳中含量仅次于氧的非金属元素。化合物J是一种可用于制造发动机的新型无机非金属材料,其相对分子质量为140,其中D元素的质量分数为60 %。上述物质间的转化关系如下图所示。
A
焦炭
高温
B
D的单质
F
G
I
H
Cl2
△
J
I
一定条件
(1)除A外,制玻璃的主要原料还有物质(填化学式) 、 。
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示) 。
(2)D元素在元素周期表中的位置是 。
(3)H的电子式是 。
(4)F和H反应生成J和I反应的化学方程式是 。
(5)下列说法正确的是(填选项序号) 。
a.上述由A生成D的单质的反应属于置换反应
b.D元素在自然界中主要以单质形式存在
c.G是含有极性共价键的离子化合物
d.I是强电解质,G是弱电解质,二者的水溶液都显酸性
27.(16分)硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得。
已知:Na2S2O3在酸性溶液中不能稳定存在。
(1)某研究小组设计了制备Na2S2O3•5H2O的装置和部分操作步骤如下。
Cu片
A
B
C
D
浓硫酸
K1
K2
Na2CO3溶液
和硫粉
NaOH溶液
I.打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热。
II.C中的混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。
当C中溶液的pH接近7时即停止C中的反应,停止加热。
III.过滤C中的混合液。
IV.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品。
① I中,圆底烧瓶中发生反应的化学方程式是 。
② II中,“当C中溶液的pH接近7时即停止C中的反应”的原因是 。
“停止C中的反应”的操作是 。
③ III中,“过滤”用到的玻璃仪器是(填仪器名称) 。
④ 装置B中盛放的试剂是(填化学式) 溶液,其作用是 。
(2)依据反应2S2O32—+I2=S4O62—+2I—,可用I2的标准溶液测定产品的纯度。取5.5 g 产品,配制成100 mL溶液。取10 mL溶液,以淀粉溶液为指示剂,用浓度为0.050 mol/L I2的标准溶液进行滴定,相关数据记录如下表所示。
编 号
1
2
3
4
溶液的体积/mL
10.00
10.00
10.00
10.00
消耗I2标准溶液的体积/mL
19.99
19.98
17.13
20.03
① 判断达到滴定终点的现象是 。
② Na2S2O3•5H2O在产品中的质量分数是(计算结果保留1位小数) 。
(Na2S2O3•5H2O的式量为248)
28.(14分)硝酸是一种重要的化工原料,工业上生产硝酸的主要过程如下。
(1)以N2和H2为原料合成氨气。反应:N2(g)+3H2(g)2NH3(g) ΔH<0。
① 下列措施可以提高H2的转化率的是(填选项序号) 。
a.选择适当的催化剂 b.增大压强
c.及时分离生成的NH3 d.升高温度
② 一定温度下,在密闭容器中充入1 mol N2和3 mol H2发生反应。
若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的,则N2的转化率
α1= ;
若容器压强恒定,达到平衡状态时,N2的转化率为α2,则α2 α1(填“>”、“<”或“=”)。
(2)以氨气、空气为主要原料制硝酸。
① NH3被氧气催化氧化生成NO的反应的化学方程式是 。
② 在容积恒定的密闭容器中进行反应2NO(g)+O2(g)2NO2(g) ΔH>0。该反应的反应速率(υ)随时间(t)变化的关系如右图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) 。
a.在t1 ~ t2时,可依据容器内气体的压强保持
不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3 ~ t4时,可依据容器内气体的密度保持
不变判断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
(3)硝酸厂常用如下2种方法处理尾气。
① 催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g) + O2(g)=2H2O(g) ΔH=— 483.6 kJ/mol
N2(g) + 2O2(g)=2NO2(g) ΔH=+ 67.7 kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是 。
② 碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2 g NO2和Na2CO3溶液反应时转移电子数为0.1 mol,则反应的离子方程式
是 。
北京市西城区2010年抽样测试
高三理科综合能力测试(化学部分) 2010.5
参考答案及评分标准
6.B 7.D 8.A 9.B 10.C 11.C 12.B
25 ~ 28题其他合理答案可给分
25.(16分)
(1)①(2分)蒸馏 ②(2分)C8H8O3
H3CO
一定条件
H2N
COOH
+
H2O +
—CH=CH—CONH
OCH3
COOH
H3CO
OCH3
—CH=CHCOOH
(2)
①(2分)
O2
△
OCH3
H3CO
—CH=CHCH2OH
+
2
Cu
OCH3
H3CO
—CH=CHCHO
2
+2H2O
(2分)
②(2分)取代反应
H3CO
—CHCH2CH3
OCH3
OH
③(2分)
④(2分)bd
OH
CHO
OCH3
⑤(2分)
26.(12分)
(1)(1分)Na2CO3 (1分)CaCO3
(2分)SiO2+2NaOH=Na2SiO3+H2O
(2)(2分)第3周期IVA族
一定条件
(3)(2分)
(4)(2分)3SiCl4+4NH3 Si3N4+12HCl
(5)(2分)ac
27.(16分)
(1)①(2分)Cu+2H2SO4(浓) CuSO4 + SO2↑+2H2O
②(2分)Na2S2O3在酸性溶液中不能稳定存在
(2分)打开K2,关闭K1
③(2分)漏斗、玻璃棒、烧杯
④(2分)NaOH
(2分)在C中的反应停止后,吸收A中产生的多余SO2 ,防止空气污染
(2)①(2分)加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变
②(2分)90.2 %
28.(14分)
(1)①(2分)bc
②(2分)12.5 %
△
催化剂
(2分)>
(2)①(2分)4NH3 +5O2 4NO+6H2O
②(2分)ab
(3)①(2分)4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=— 1034.9 kJ/mol
②(2分)2NO2 +CO32-=NO3-+NO2-+CO2
相关文档
- 2014年版高考语文二轮精选基础试题2021-05-132页
- 2020版高考地理一轮复习第13章第292021-05-136页
- 高考英语六百高频词汇2021-05-1311页
- 高考经济生活主观题精选大全2021-05-138页
- 2020年高考物理备考冲刺之易错点点2021-05-1335页
- (浙江专版)备战2020高考地理一轮复习2021-05-1312页
- 2020版高考数学二轮复习 专题四 数2021-05-136页
- 高考一轮复习水体运动与地壳运动专2021-05-133页
- 2011山东高考英语一轮复习巩固提升2021-05-136页
- 2017高考新课标全国1卷文科综合试2021-05-1321页