- 537.48 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
考点清单
考点一 物质的组成、性质和分类
一、物质的组成
1.宏观上:物质由①
元素
组成,元素在自然界有两种存在形式,以
单质
形
式存在的称为元素的②
游离
态,以
化合物
形式存在的称为元素的
③
化合
态。
2.
微观上
:
质子、中子、④
电子
是构成原子的三种基本粒子
,
原子、分子、⑤
离子
是构成物质的三种基本微粒。
二、分类的方法
1.
单一分类法
单一分类法就是对被分类的对象只用一种标准进行分别归类的分类方法
,
如
:
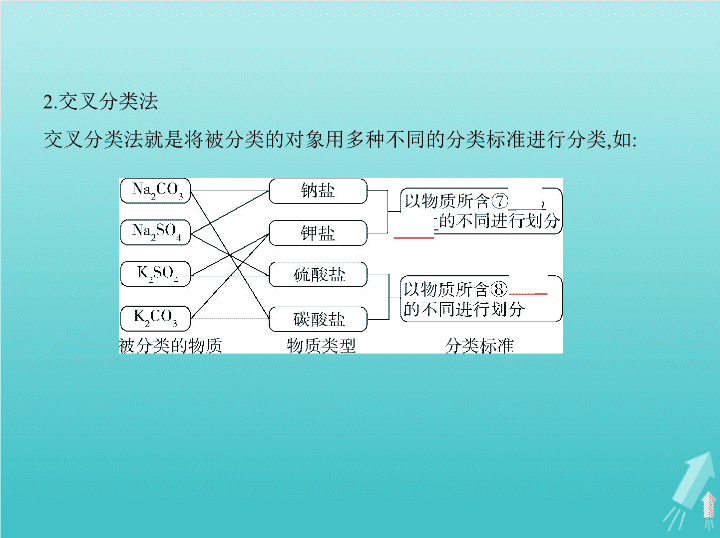
2.交叉分类法
交叉分类法就是将被分类的对象用多种不同的分类标准进行分类,如:
3.树状分类法
所谓树状分类法,简单地说,是根据被分类对象的整体与分出的类别间的关
系及其陈列式的形状(像树)来定义的,如下图:
考点二 分散系
一、分散系
二、溶液
1.饱和溶液
在一定温度下,向一定量的溶剂里加入某种溶质,当溶质不能继续溶解时,
所得到的溶液叫作这种溶质的饱和溶液。
2.溶解度
溶解度
:
在一定温度下
,
某物质在
100
g
溶剂里达到
饱和
状态
时所溶解的质量
,
单位是克
,
符号为
S
。计算公式
:
溶解度
=
×
100 g,
即
S
=
×
100 g
溶解度随温度升高而增大的物质
,
当把其饱和溶液的温度降低时
,
溶质将会
析出。
3.溶解度与溶质质量分数的区别
溶质质量分数与溶解度不同,它没有单位,既可以用百分数表示,又可以用
小数表示,且适用于任何溶液。而
溶解度仅适用于饱和溶液
。
4.溶解度的影响因素
(1)KNO
3
的溶解度随温度升高而显著
增大
;NaCl的溶解度也随温度
升高而
增大
,但变化趋势不如KNO
3
的大;Ca(OH)
2
的溶解度随温度的
升高而
减小
。
(2)气体的溶解度随温度升高而减小,随压强的增大而增大。
5.有关溶质质量分数的计算
(1)
ω
=
×
100%=
×
100%。
(2)
ω
=
×
100%(饱和溶液,溶解度为
S
)。
三、胶体
1.定义:分散质粒子直径介于1~100 nm之间的分散系。
2.特征
(1)外观特征:均一。
(2)
本质特征:胶体粒子直径介于1~100 nm之间
。
3.分类
按照存在状态的不同,将胶体分为三类:
(1)气溶胶,如烟、云、雾;
(2)液溶胶,如AgI水溶胶;
(3)固溶胶,如烟水晶、有色玻璃。
4.性质
(1)丁达尔效应
当光束通过胶体时,可以看到一条光亮的“通路”。这是胶体粒子对光线
散射
形成的,叫作丁达尔效应。
说明 a.
丁达尔效应是物理现象;
b.
利用丁达尔效应可区别溶液和胶体;
c.丁达尔效应能证明分散质粒子直径的大小范围;
d.当光束通过胶体时,看到的光亮的“通路”是光被胶体粒子散射的现象,
并不是胶体粒子本身发光。
(2)介稳性
胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳
体系。
写出制备Fe(OH)
3
胶体的离子方程式:
Fe
3+
+3H
2
O
Fe(OH)
3
(胶体)+3H
+
。
5.Fe(OH)
3
胶体的制备
知能拓展
一、物质分类中易混淆的概念关系
1.名称中有“酸”的物质不一定是酸,如石炭酸(C
6
H
5
OH)是酚,不是酸。
2.
酸的元数不一定等于酸分子中的
H
原子数。如亚磷酸
(H
3
PO
3
)
是二元酸
,
次磷酸
(H
3
PO
2
)
是一元酸
,
因为它们的结构分别是
、
3.无氧酸不一定是非金属元素的氢化物,如氢氰酸(HCN)等。
4.酸的氧化性与氧化性酸不同。酸的氧化性指H
+
的氧化性;氧化性酸指中
心原子具有氧化性的酸,如HClO、HNO
3
、浓H
2
SO
4
。
5.非金属氧化物不一定是酸性氧化物,如CO、NO等。酸性氧化物不一定
是非金属氧化物,如Mn
2
O
7
、CrO
3
。金属氧化物不一定是碱性氧化物,如
Al
2
O
3
、ZnO(两性氧化物),Mn
2
O
7
、CrO
3
(酸性氧化物)。碱性氧化物一定是金
属氧化物。
6.酸酐不一定是酸性氧化物,如乙酸酐[(CH
3
CO)
2
O]等。
7.酸性氧化物不一定能与水反应生成相应的酸,如SiO
2
。
8.Na
2
O
2
与酸反应不仅生成盐和水,还生成O
2
,因而不是碱性氧化物。
例1 (2018茂名高三五大联盟学校9月联考,4)下列有关物质的分类正确的
是
( )
A.H
2
SO
4
、HNO
3
、CH
3
COOH均属于酸
B.NO、CO、NO
2
均属于酸性氧化物
C.NaCl、CuSO
4
、NH
3
·H
2
O均属于盐
D.H
2
S、HCl、NH
3
均属于电解质
解题导引 要明确课本所给的定义,结合题目所给信息的细微之处进行分
析,如在判断电解质和非电解质时,要明确电解质与非电解质都属于化合
物,溶液导电的原因是不是化合物本身电离出了自由移动的离子。
解析 H
2
SO
4
、HNO
3
、CH
3
COOH电离出的阳离子均为氢离子,均属于酸,
A项正确;NO、CO与碱不发生反应,属于不成盐氧化物,B项错误;NH
3
·H
2
O
电离出的阴离子为氢氧根离子,属于碱,C项错误;NH
3
溶于水生成NH
3
·H
2
O,
NH
3
·H
2
O能够电离,溶液能够导电,NH
3
·H
2
O属于电解质,而NH
3
属于非电解
质,D项错误。
答案 A
二、分散系的比较
溶液
胶体
浊液
分散质粒子
直径的大小
<1 nm
1~100 nm
>100 nm
分散质粒子
单个小分
子或离子
许多分子的集
合体或高分子
巨大数目分
子的集合体
实例
乙醇溶液、
氯化钠溶液
Fe(OH)
3
胶体
石灰乳、油水
混合液
溶液
胶体
浊液
性
质
外观
均一、透明
均一
不均一、不透明
稳定性
稳定
较稳定
不稳定
能否透过滤纸
能
能
不能
能否透过半透膜
能
不能
不能
鉴别
无丁达尔效应
有丁达尔效应
静置分层
续表
例2 有关胶体与溶液的说法正确的是
( )
A.胶体粒子带电,溶液中的溶质粒子不带电
B.渗析实验可以鉴别胶体和溶液
C.胶体与溶液都可以通过滤纸、半透膜和分子筛
D.丁达尔效应可以区分胶体和溶液
解题导引 明确溶液、胶体及浊液本质上的区别在于粒子直径大小不同,
微观尺度影响了宏观表征,使胶体具有较为特殊的性质。
解析 溶液呈电中性,溶液中的溶质粒子可能带电,如Na
+
,A项错误;渗析可
以分离胶体粒子和溶液中的溶质粒子,不能鉴别胶体和溶液,B项错误;胶体
和溶液可以透过滤纸,但胶体不能透过半透膜和分子筛,C项错误;胶体具有
丁达尔效应,而溶液不具有,D项正确。
答案 D
实践探究
1.化学与社会是紧密联系的。应注意以周边环境为背景创设题目,考查学
生综合运用所学的化学知识和技能,分析和解决与化学有关的实际问题。
例1 (2019江苏南京师范大学附属中学模拟,1)2019年4月22日是第50个
“世界地球日”,我国确定的活动主题为“珍爱美丽地球,守护自然资
源”。下列行为不符合这一活动主题的是
( )
A.改进汽车尾气净化技术,减少大气污染物的排放
B.加快化石燃料的开采与使用,促进社会可持续发展
C.用CO
2
合成聚碳酸酯可降解塑料,实现碳的循环利用
D.对工业废水、生活污水进行净化处理,减少污染物的排放
解析 改进汽车尾气净化技术,减少大气污染物的排放,有利于保护环境,
符合题述主题;加快化石燃料的开采与使用会增加污染物的排放量,不符合
该主题;用CO
2
合成聚碳酸酯可降解塑料,实现碳的循环利用,减少二氧化碳
对环境的影响,符合该主题;对工业废水、生活污水进行净化处理,减少污
染物的排放,循环高效利用水资源,可以节约能源、减少污染物的排放,符
合该主题。
答案 B
题目价值 真实、具体的问题情境是学科核心素养形成和发展的重要平
台。因此
,
应重视构建真实且富有价值的问题情境
,
促进学科核心素养的形
成与发展。
2.物质分类方法多种多样,应注意从多角度对物质进行分类,提高学生迁移
应用的变通能力。
例2 (2018安徽淮南等五校联考,5)清华大学的科学家将古老的养蚕技术
与时兴的碳纳米管和石墨烯结合,发现通过给蚕宝宝喂食含有碳纳米管和
石墨烯的桑叶,可以获得更加牢固的蚕丝纤维。已知:当把石墨片剥成单层
之后,这种只有一个碳原子厚度的单层就是石墨烯。下列说法正确的是
( )
A.蚕丝纤维的主要成分是纤维素
B.石墨烯像烯烃一样,是一种有机物
C.碳纳米管和石墨烯互为同素异形体
D.碳纳米管具有丁达尔效应
解析 蚕丝的主要成分是蛋白质,A项错误;石墨烯是只有一个碳原子厚度
的石墨片,属于单质,B项错误;碳纳米管和石墨烯是由碳元素组成的不同单
质,互为同素异形体,C项正确;碳纳米管在合适的分散剂中形成胶体才能具
有丁达尔效应,D项错误。
答案 C
题目价值 能根据物质组成和性质对物质进行分类,形成物质由元素组成
和化学变化中元素不变的观点。了解生活中常用材料的组成与性能,认识
化学在日用材料的发展中的重要作用。
相关文档
- 重庆市2021高考化学一轮复习专题三2021-07-0273页
- 高考化学一轮复习专题11_3物质的分2021-07-0219页
- 2021高考化学一轮复习专题5第3讲化2021-07-0241页
- 北京版2021高考化学一轮复习专题六2021-07-0228页
- 2021高考化学一轮复习专题9第1讲重2021-07-0221页
- 浙江版2021高考化学一轮复习专题七2021-07-0221页
- 山东版2021高考化学一轮复习专题十2021-07-0217页
- 高考化学一轮复习专题7_1化学反应2021-07-0231页
- 2021高考化学一轮复习专题3第2讲镁2021-07-0294页
- 山东版2021高考化学一轮复习专题五2021-07-0221页