- 615.04 KB
- 2021-07-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课时作业19 化学电源
时间:45分钟 满分:100分
一、选择题(每小题4分,共48分)
1.银锌电池广泛用作各种电子仪器的电源,它的电池反应是:Zn+Ag2O+H2O===2Ag+Zn(OH)2,则负极上发生反应的物质是( D )
A.Ag B.Zn(OH)2
C.Ag2O D.Zn
解析:由题给总方程式得:Zn+2OH--2e-===Zn(OH)2,故Zn为负极。
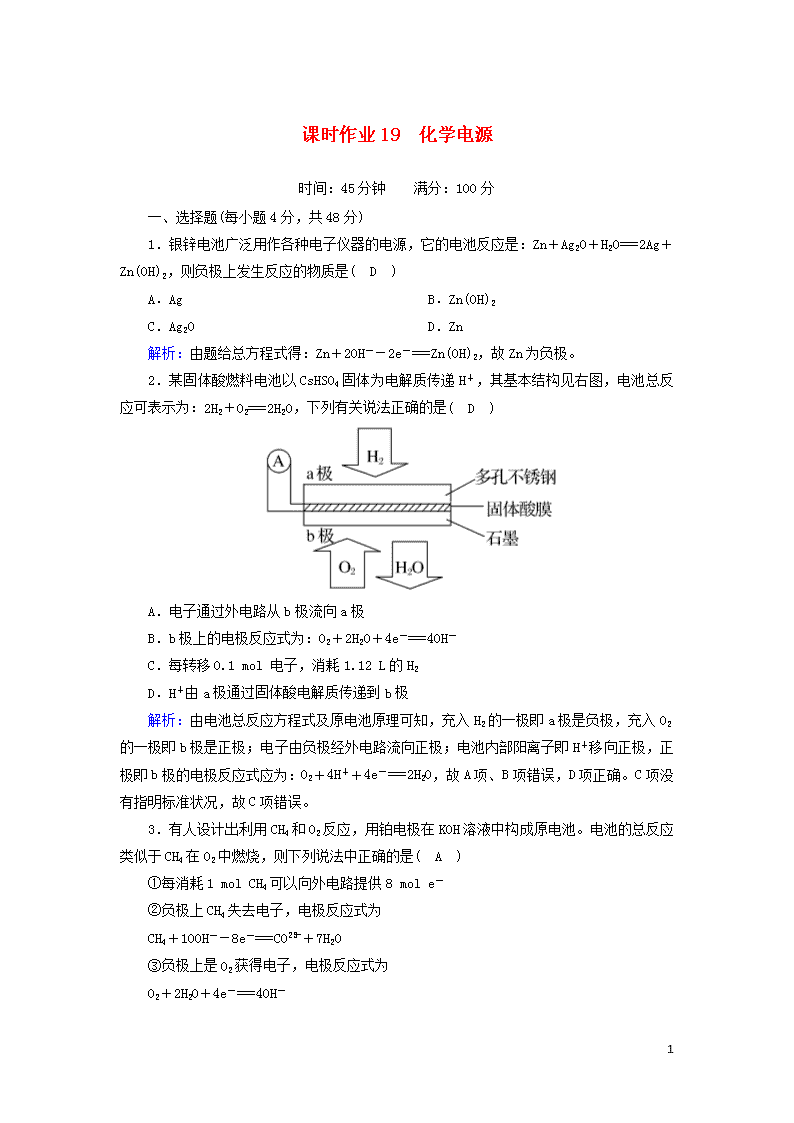
2.某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见右图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是( D )
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-===4OH-
C.每转移0.1 mol 电子,消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
解析:由电池总反应方程式及原电池原理可知,充入H2的一极即a极是负极,充入O2的一极即b极是正极;电子由负极经外电路流向正极;电池内部阳离子即H+移向正极,正极即b极的电极反应式应为:O2+4H++4e-===2H2O,故A项、B项错误,D项正确。C项没有指明标准状况,故C项错误。
3.有人设计出利用CH4和O2反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法中正确的是( A )
①每消耗1 mol CH4可以向外电路提供8 mol e-
②负极上CH4失去电子,电极反应式为
CH4+10OH--8e-===CO+7H2O
③负极上是O2获得电子,电极反应式为
O2+2H2O+4e-===4OH-
9
④电池放电时,溶液pH不断升高
A.①② B.①③ C.①④ D.③④
解析:CH4在铂电极上发生类似于CH4在O2中燃烧的反应,即CH4→CO2,严格地讲生成的CO2还与KOH反应生成K2CO3,化合价升高,失去电子,是电池的负极,电极反应式为CH4+10OH--8e-===CO+7H2O,1 mol CH4参加反应有8 mol e-发生转移,O2在正极上发生反应,获得电子,电极反应式为O2+2H2O+4e-===4OH-。虽然正极产生OH-,负极消耗OH-,但从总反应CH4+2O2+2KOH===K2CO3+3H2O可看出是消耗KOH,所以电池放电时溶液的pH不断下降,故①②正确,③④错误。故正确答案为A。
4.镍镉(NiCd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd+2NiO(OH)+2H2OCd(OH)2+2Ni(OH)2。下列叙述中正确的是( C )
A.该电池放电的时候,负极材料是Ni(OH)2
B.放电时每转移3 mol电子时,正极有3 mol NiO(OH)被氧化
C.充电时,阴极附近pH增大
D.充电时,阳极反应是Cd(OH)2+2e-===Cd+2OH-
解析:放电时为原电池原理,电池总反应为Cd+2NiO(OH)+2H2O===Cd(OH)2+2Ni(OH)2,负极材料为Cd,负极电极反应式为Cd-2e-+2OH-===Cd(OH)2,正极电极反应式为2NiO(OH)+2e-+2H2O===2Ni(OH)2+2OH-,A错误;根据电极反应式知,放电时每转移3 mol电子,正极有3 mol NiO(OH)被还原,B错误;充电时为电解原理,电解反应为Cd(OH)2+2Ni(OH)2===Cd+2NiO(OH)+2H2O,阴极电极反应式为Cd(OH)2+2e-===Cd+2OH-,阴极附近碱性增强,pH增大,C正确;充电时的阳极电极反应式为2Ni(OH)2+2OH--2e-===2NiO(OH)+2H2O,D错误。
5.科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料。电池中的一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-。下列对该燃料电池的说法不正确的是( A )
A.在熔融电解质中,O2-由负极移向正极
B.该电池的总反应是:C3H8+5O2===3CO2+4H2O
C.电路中每通过5 mol电子,约有5.6 L标准状况下的丙烷被完全氧化
D.通入丙烷的电极为电池负极,发生的电极反应为:
C3H8-20e-+10O2-===3CO2+4H2O
解析:该燃料电池的化学反应原理是:C3H8+5O2===3CO2+4H2O,B正确;放电过程中通入丙烷的电极为负极:C3H8-20e-+10O2-===3CO2+4H2O,C、D正确;通入O2的电极为正极:O2+4e-===2O2-,产生的O2-将向负极移动,A项错。
9
6.美国海军海底战事中心与麻省理工学院共同研制成功的用于潜航器的镁-过氧化氢燃料电池系统。其工作原理如图所示。以下说法中错误的是( B )
A.电池的负极反应为:Mg-2e-===Mg2+
B.电池工作时,H+向负极移动
C.电池工作一段时间后,溶液的pH增大
D.电池总反应式是:Mg+H2O2+2H+===Mg2++2H2O
解析:Mg-H2O2燃料电池中Mg作负极:Mg-2e-===Mg2+,Pt作正极:H2O2+2H++2e-===2H2O,总式为:Mg+H2O2+2H+===Mg2++2H2O,消耗H+,使c(H+)减小,pH增大,且H+移向正极。
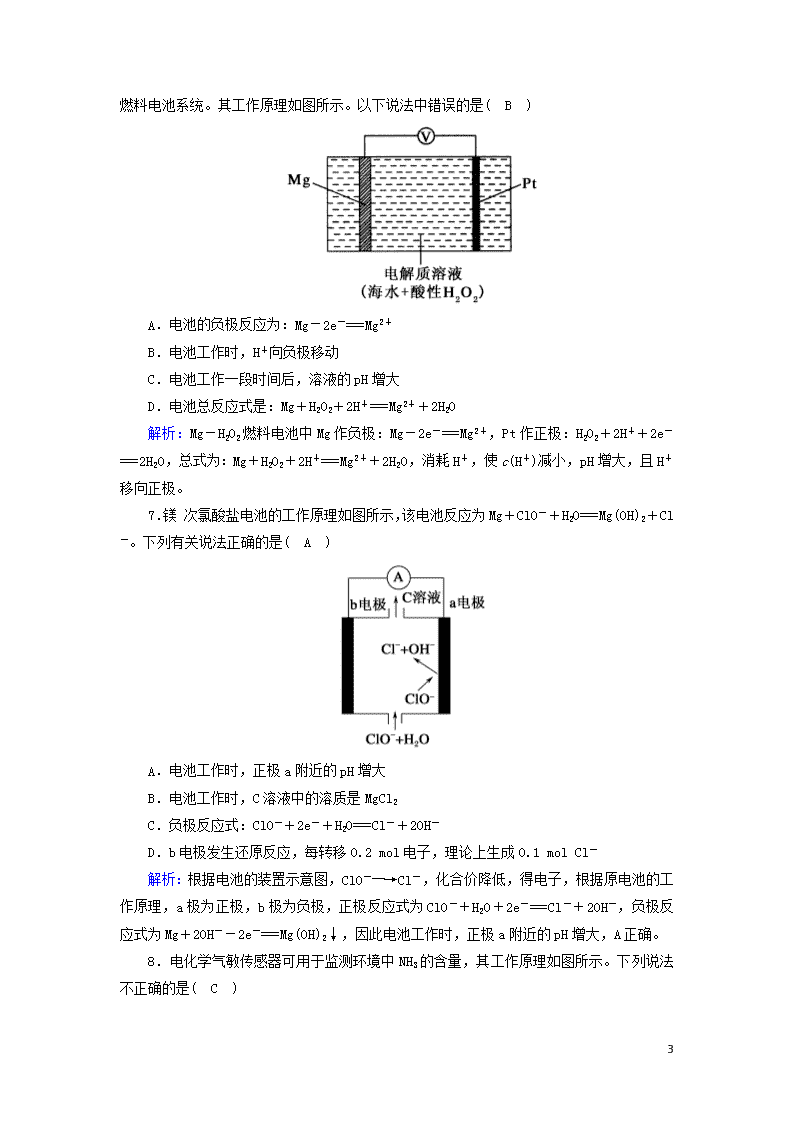
7.镁次氯酸盐电池的工作原理如图所示,该电池反应为Mg+ClO-+H2O===Mg(OH)2+Cl-。下列有关说法正确的是( A )
A.电池工作时,正极a附近的pH增大
B.电池工作时,C溶液中的溶质是MgCl2
C.负极反应式:ClO-+2e-+H2O===Cl-+2OH-
D.b电极发生还原反应,每转移0.2 mol电子,理论上生成0.1 mol Cl-
解析:根据电池的装置示意图,ClO-―→Cl-,化合价降低,得电子,根据原电池的工作原理,a极为正极,b极为负极,正极反应式为ClO-+H2O+2e-===Cl-+2OH-,负极反应式为Mg+2OH--2e-===Mg(OH)2↓,因此电池工作时,正极a附近的pH增大,A正确。
8.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示。下列说法不正确的是( C )
9
A.O2在电极b上发生还原反应
B.溶液中OH-向电极a移动
C.反应消耗的NH3与O2的物质的量之比为45
D.负极的电极反应式为2NH3-6e-+6OH-===N2+6H2O
解析:构成的原电池中,通入氧气的电极是正极,发生还原反应,A项正确;电池放电过程中,溶液中的阴离子移向负极(a极),B项正确;1 mol NH3反应生成N2转移3 mol电子,1 mol O2反应转移4 mol电子,根据电子守恒可知,消耗的NH3与O2的物质的量之比为43,C项错误;负极的电极反应式为2NH3-6e-+6OH-===N2+6H2O,D项正确。
9.乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应式为C2H5OH+3O2===2CO2+3H2O,电池示意图如右,下列说法中正确的是( B )
A.电池工作时,质子向电池的负极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是C2H5OH+3H2O+12e-===2CO2+12H+
D.b极上发生的电极反应是2H2O+O2+4e-===4OH-
解析:通入乙醇的一极(a极)为负极,发生氧化反应;通入氧气的一极(b极)为正极,发生还原反应。电池工作时,阳离子(质子)向电池的正极迁移,选项A不正确;电流方向与电子流向相反,电流由b极沿导线流向a极,选项B正确;a极上乙醇应该失电子被氧化,所以选项C不正确;因为电池中使用的是磺酸类质子溶剂,所以电极反应式中不能出现OH-,选项D不正确。
10.据报道,美国一个海军航空站安装了一台250 kW的MCFC型燃料电池。该电池可同时供应电和水蒸气,其燃料为H2,电解质为熔融的K2CO3,工作温度为600~700
9
℃。已知该电池的总反应为2H2+O2===2H2O,负极反应为H2+CO-2e-===H2O+CO2。下列推断正确的是( B )
A.正极反应为4OH--4e-===O2+2H2O
B.放电时,CO向负极移动
C.电池供应1 mol水蒸气,转移电子的物质的量为4 mol
D.放电时,CO向正极移动
解析:该电池的正极反应为O2+4e-+2CO2===2CO,A项错误;原电池工作时,阴离子向负极移动,B项正确,D项错误;电池提供1 mol水蒸气时,转移的电子的物质的量为2 mol,C项错误。
11.某种新型超级电池采用高铁酸钾(K2FeO4)作正极材料,填充H2的金属作负极材料,KOH溶液为电解液,该电池具有电压高且稳定、绿色环保等特点。下列说法正确的是( C )
A.正极的电极反应式为2FeO+10OH-+6e-===Fe2O3+5H2O
B.负极的电极反应式为H2-2e-===2H+
C.电池工作过程中,溶液的pH增大
D.该电池中电子从负极经KOH溶液流向正极
解析:根据题意可知,正极的电极反应式为 2FeO+5H2O+6e-===Fe2O3+10OH-,负极的电极反应式为H2+2OH--2e-===2H2O,电池总反应为2K2FeO4+3H2===Fe2O3+H2O+4KOH,故A、B项错误,C项正确。该电池中电子从负极经外电路流向正极,D项错误。
12.硼化矾(VB2)空气电池是目前储电能力最高的电池,电池示意图如右,该电池工作时反应为4VB2+11O2===4B2O3+2V2O5。下列说法正确的是( D )
A.电极a为电池负极
B.图中选择性透过膜只能让阳离子选择性通过
C.电子由VB2极经KOH溶液流向电极a
D.VB2极发生的电极反应为2VB2+22OH--22e-===V2O5+2B2O3+11H2O
解析:
9
根据电池总反应和题图知电极a为正极,A项错误;题图中选择性透过膜只能让阴离子选择性通过,B项错误;电子由VB2极经负载流向电极a,C项错误;根据总反应和电子转移情况可知D项正确。
二、非选择题(52分)
13.(12分)SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
(1)利用电化学原理将CO、SO2转化为重要化工原料,装置如图所示。
①若A为CO,B为H2,C为CH3OH,则通入CO一极的电极反应式为CO+4e-+4H+===CH3OH。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为SO2+2H2O-2e-===SO+4H+。
③若A为NO2,B为O2,C为HNO3,则负极的电极反应式为NO2-e-+H2O===NO+2H+。
(2)碳酸盐燃料电池以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650 ℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为11)直接作燃料,其工作原理如图所示。
则电池负极反应式为CO+H2-4e-+2CO===3CO2+H2O。
解析:(1)①燃料电池中,通入氧化剂的电极是正极,通入还原剂的电极是负极,该反应中C化合价由+2价变为-2价,H化合价由0价变为+1价,所以CO是氧化剂,则通入CO的电极为正极,电极反应式为CO+4e-+4H+===CH3OH;
②若A为SO2,B为O2,C为H2SO4,负极上二氧化硫失电子,与水反应生成硫酸根离子和氢离子,电极反应式为SO2+2H2O-2e-===SO+4H+;
9
③若A为NO2,B为O2,C为HNO3,则正极发生还原反应,氧气得电子生成水,电极反应式为O2+4e-+4H+===2H2O,负极发生氧化反应,电极反应式为NO2-e-+H2O===NO+2H+。
(2)该燃料电池中,负极上一氧化碳、氢气失电子,与碳酸根离子反应生成二氧化碳和水,电极反应式为CO+H2-4e-+2CO===3CO2+H2O。
14.(14分)科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下图:
请回答下列问题:
(1)Pt(a)电极是电池的负极,电极反应式为2CH3OH+2H2O-12e-===2CO2↑+12H+;Pt(b)电极发生还原(填“氧化”或“还原”)反应,电极反应式为3O2+12H++12e-===6H2O。
(2)该电池的总反应方程式为2CH3OH+3O2===2CO2+4H2O。
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有 mol。
解析:Pt(a)端的原料为CH3OH和H2O,产物为CO2、H+,根据C化合价由-2价升到+4价,失去6个电子,Pt(a)为负极;Pt(b)端的原料为O2和H+,产物为H2O,O化合价由0价降为-2价,发生还原反应,为正极。
15.(14分)(1)根据氧化还原反应2H2+O2===2H2O,设计成燃料电池,负极通的气体应是H2,正极通的气体应是O2。
9
(2)上图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是B。
A.a电极是负极
B.b电极的电极反应为4OH--4e-===2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(3)根据选择电解质溶液的不同,填写下表:
(4)若把H2改为CH4,KOH溶液作电解质,则负极反应为CH4+10OH--8e-===CO+7H2O。
16.(12分)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-
9
根据上述反应式,完成下列填空。
(1)下列叙述正确的是C。
A.在使用过程中,电解质溶液中的KOH被不断消耗,pH减小
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:Zn+Ag2O===ZnO+2Ag。
(3)使用时,负极区的pH减小(填“增大”“减小”或“不变”,下同),正极区的pH增大,电解质溶液的pH不变。
解析:(1)在使用过程中,负极消耗OH-,pH减小,正极生成OH-,pH增大,电解质溶液中KOH的量不变,pH不变,A项错;电子流向是由Zn极经外电路流向Ag2O极,B项错;Zn为负极,发生氧化反应,Ag2O为正极,发生还原反应,C项对,D项错。
(2)将正负两极反应式相加可得总反应式。
9
相关文档
- 2020届一轮复习人教版金属的化学性2021-07-0625页
- 2018-2019学年安徽省滁州市定远县2021-07-066页
- 2020高考化学刷题冲刺(含最新模拟题2021-07-0612页
- 2018-2019学年重庆市铜梁一中高二2021-07-068页
- 2020届高考化学二轮复习铁、铜及其2021-07-0629页
- 2018-2019学年四川省阆中中学高一2021-07-065页
- 2019届一轮复习人教版有机化学基础2021-07-0610页
- 北京市海淀区2018-2019学年高一学2021-07-0623页
- 【化学】宁夏吴忠中学2019-2020学2021-07-0618页
- 人教版高二化学5-2关于硫酸工业综2021-07-065页