- 883.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
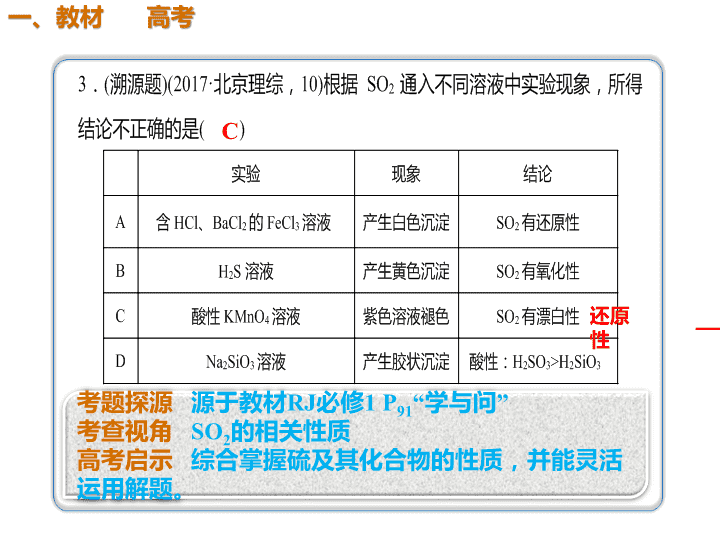
C
还原
性
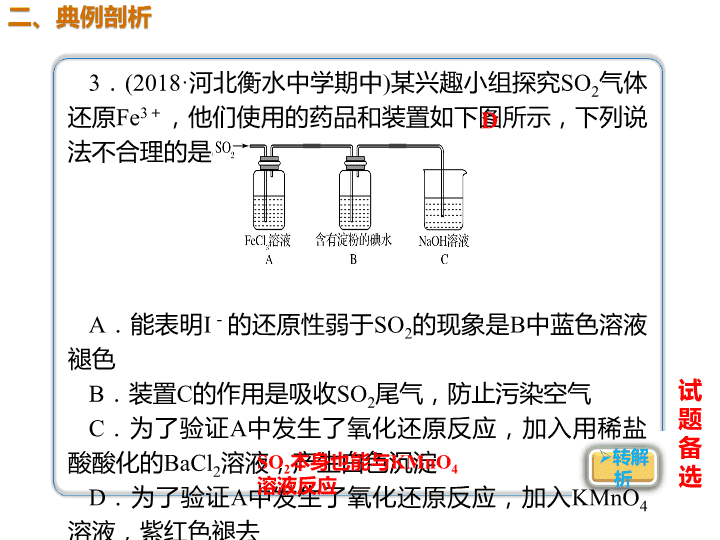
3.(2018·河北衡水中学期中)某兴趣小组探究SO2气体
还原Fe3+,他们使用的药品和装置如下图所示,下列说
法不合理的是( )
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液
褪色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐
酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4
溶液,紫红色褪去
D
试
题
备
选
SO2本身也能与KMnO4
溶液反应
解析 A项,向含有淀粉的碘水中通入SO2气体,会发生
反应:SO2+I2+2H2O===H2SO4+2HI,由于I2反应消耗,
因此B中蓝色溶液褪色,证明物质的还原性:SO2>I-,正
确。B项,SO2是大气污染物,由于SO2是酸性气体,可以
与NaOH发生反应:SO2+2NaOH===Na2SO3+H2O,因此
可以用NaOH溶液吸收尾气,防止污染空气,正确。C项,
若A中发生了氧化还原反应:SO2+2H2O+2FeCl3===H2SO4
+2HCl+2FeCl2,溶液中含有硫酸,当加入用稀盐酸酸化
的BaCl2溶液时,会产生白色沉淀;若没有发生氧化还原反
应,则由于酸性HCl>H2SO3,向溶液中加入用稀盐酸酸化
的BaCl2溶液,不会产生白色沉淀,正确。D项,若SO2与
FeCl3不发生反应,向A中加入KMnO4溶液,发生反应:
2KMnO4+5SO2+2H2O===K2SO4+2MnSO4+2H2SO4,溶
液紫红色能褪去;若SO2与FeCl3发生反应:SO2+2H2O+
2FeCl3===H2SO4+2HCl+2FeCl2,当向反应后的溶液中加
入酸性高锰酸钾溶液时,会发生反应:MnO4
-+5Fe2++8H
+===Mn2++5Fe3++4H2O,溶液紫红色也能褪去,因此不
能验证A中是否发生了氧化还原反应,错误。
3.(2016·河南洛阳高三期末,16)如图,在注射器
中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接
触纸条为准)。则下列有关说法正确的是( )
A.湿润淀粉碘化钾试纸未变蓝说明SO2不能将I-还
原为I2
B.品红试纸、沾有KMnO4溶液的滤纸均褪色证明了
SO2具有漂白性
C.实验后,可把注射器中的物质推入NaOH溶液,
以减少环境污染
D.蓝色石蕊试纸先变红后褪色
SO2发生装
置
C
氧化
只变红,不退
色
【试题备选】
解析 湿润淀粉碘化钾试纸未变蓝说明SO2不能将I-
氧化为I2,A项错误;品红试纸褪色证明SO2具有漂
白性,沾有KMnO4溶液的滤纸褪色是证明SO2具有
还原性,B项错误;SO2气体有毒,所以实验后,可
把注射器中的物质推入NaOH溶液进行吸收,以减少
环境污染,C项正确;SO2仅能使蓝色石蕊试纸变红,
D项错误。
常
见
的
能
用
于
漂
白
的
物
质
的
比
较
与
分
析
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页