- 1.91 MB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
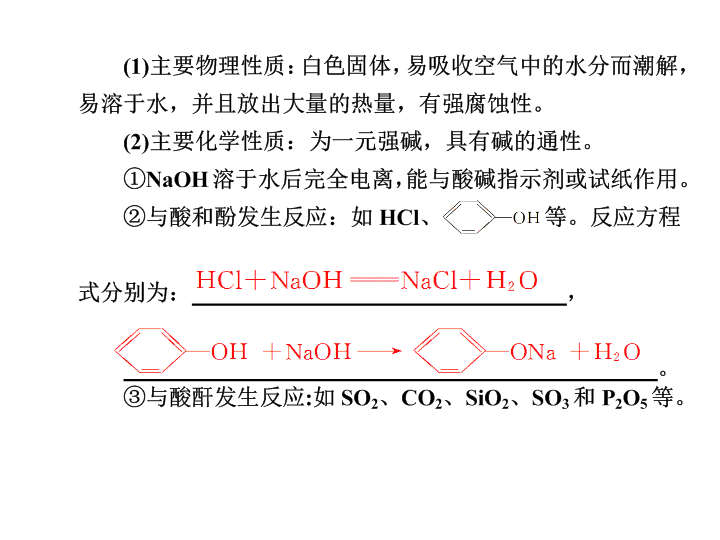
烧碱、火碱、苛性钠
第三章 常见的金属及其化合物
2Al+2NaOH+2H2O===2NaAlO2+3H2↑。
NH4Cl+NaOH NaCl+H2O+NH3↑。
名称(化
学式) 碳酸钠(Na2CO3) 碳酸氢钠
(NaHCO3)
俗名
主
要
性
质
色态 白色晶体 细小白色晶体
水溶
性
易溶于水,
溶液呈碱性
易溶于水(但比
同温下Na2CO3溶
解度小),溶液
呈碱性
稳定
性
不稳定,受热易
分解
纯碱或苏打 小苏打
稳定,但结晶碳酸钠
(Na2CO3·10H2O)
易风化
硫
酸
铝
主
要
性
质
与H+反应 CO +2H+
H2O+CO2↑
HCO +H+ H2O
+CO2↑
与OH-不反应,
但Ca2++CO
CaCO3↓
Ca2++OH-+HCO
CaCO3↓+H2O(碱过量)
Ca2++2OH-+2HCO
CaCO3↓+CO +2H2O
(碱不足)
盐
CaCl2 Ca2++CO
CaCO3↓↓
2Al3++3CO
+
3H2O
2Al(OH)3↓+
3CO2↑
3HCO +Al3+
Al(OH)3↓+3CO2↑
不反应
与碱反应
[Ca(OH)2]
主要用途 玻璃、造纸、
制皂、洗涤
发酵、医药、灭火器
相互转化
提示 以NaOH溶液为代表的碱性溶
液中的OH-可与磨口玻璃塞中裸露
的SiO2反应,生成Na2SiO3,使瓶
塞和瓶体粘连在一起不易打开。
提示 溶液中将析出白色晶体(沉淀)。原因
是:发生Na2CO3+CO2+
H2O===2NaHCO3↓,①同温下,NaHCO3
的溶解度比Na2CO3小,②生成的NaHCO3
的质量比消耗的Na2CO3的大(即106 g
Na2CO3生成168 g NaHCO3),即溶质增加,
③反应消耗了水,即溶剂减少,因此出现沉
淀,主要原因是①。
1
依次增多
依次增大
银白
小 较小 较低
+1
碱
减小
增强
增强
剧烈
增强
物理
黄色
蓝色钴玻璃 黄绿
答案 C
答案 B
答案 D
答案 B
。
答案 D
答案 A
答案 A
答案 C
×
√
。
Na+H2O—Na++OH-+H2
HCO-+2OH-==CO2 +2H2O3
Na2CO3+H2SO4==
Na2SO4+H2O Na2O2
1:1
H2O2 Ⅰ、Ⅳ、Ⅴ
2Na2CO3+Cl2+H2O==NaClO+2NaHCO3+NaCl
3
2-
3
2-
2
-2
2-
2
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页