- 1.71 MB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
水电离产生
的H+或OH
-
弱电解质
水的电离平衡
增大
第十章 水溶液中的离子平衡
可逆
中和
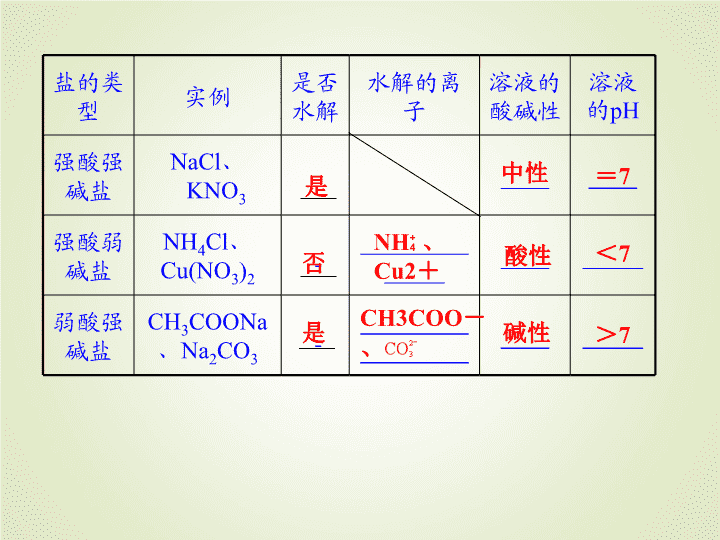
盐的类
型 实例 是否
水解
水解的离
子
溶液的
酸碱性
溶液
的pH
强酸强
碱盐
NaCl、
KNO3 ____ ____
强酸弱
碱盐
NH4Cl、
Cu(NO3)2
_________
_____ ____ _____
弱酸强
碱盐
CH3COONa、
Na2CO3
_________
_________ ____ _____
NH 、
Cu2+
CH3COO-
、CO2
3
中性
酸性
碱性
=7
<7
>7
+
4
是
否
是
弱酸(或弱碱)+OH-(或H+)
NH +H2O
NH3·H2O+H+
+
4
CO +H2O HCO +OH-
Fe3++3H2O Fe(OH)3+3H
+
Al3++3HCO ===Al(OH)3↓+3CO2↑
2-
3
-
3
3
-
越大 越强
右移
右移
右移
增大 增大
增大
增大 减小
减小
增大
减小
减小
减小
答案 C
答案 B
答案 A
答案 C
√
×
解析 显酸性的溶液可能是酸溶液,也可能
是强酸弱碱盐溶液,还可能是酸式盐溶液,如
NaHSO4、NaH2PO4溶液显酸性。
√
解析 0.1 mol/L HA溶液的pH=3,说明HA
为弱酸,则NaA溶液中存在A-的水解平衡。
(4)在滴有酚酞溶液的氨水里,加入NH4Cl至溶
液恰好无色,则此时溶液的pH<7( )
(2010·全国Ⅰ-9B)
×
解析 酚酞的变色范围为8.2~10.0,当溶液
恰好无色时,溶液pH刚刚小于8.2,即可显示无色。
√
解析 酸性CH3COOH>H2CO3>HCO ,CO 的
水解程度比CH3COO-的大。
-3
2-
3
解析 A、D项是电离方程式,B项是CO2溶于
水后的电离过程,C项正确。
C
答案 D
答案 D
答案 A
答案 D
答案 A
答案 B
答案 B
解析 酸性:H2CO3>H2SiO3,根据水解规
律:
Na2SiO3水解程度大于Na2CO3,B项正确。
B
答案 A
BD
A
CO2
3
3HCO
A
TiCl4+xH2O
===TiO2·xH2O+4Cl-
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页