- 1.80 MB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第四节 有机合成
第三章 烃的含氧衍生物
一、有机合成的过程
利用简单、易得的原料,通过有机反应,
生成具有特定结构和功能的有机化合物。
1、有机合成的概念
2、有机合成的任务
有机合成的任务包括目标化合物分子骨架
的构建和官能团的转化。
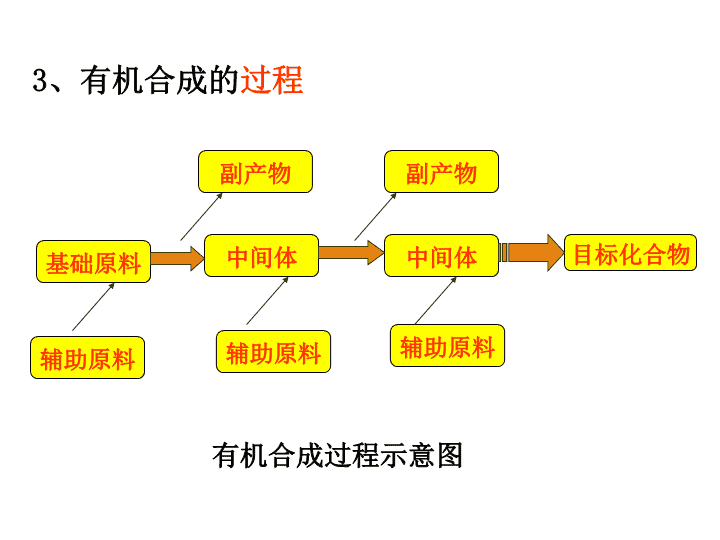
有机合成过程示意图
基础原料
辅助原料
副产物 副产物
中间体 中间体
辅助原料辅助原料
目标化合物
3、有机合成的过程
4、有机合成的设计思路
5、关键:
设计合成路线,即碳骨架的构建、官能团的引入和转化 。
6、有机物的相互转化关系:两碳有机物为例:
CH3-CH3 CH3-CH2-Cl
CH2=CH2
CH2Cl-CH2-Cl
CHCH
CH2=CHCl
[ CH-CH ] n
H Cl
CH3-CH2-OH
CH3-CHO
CH3-COOH
CH3COOC2H
5
CH3COON
a
7、碳骨架的构建和官能团的引入 。
(1).碳骨架构建:
包括碳链增长和缩短 、成环和开环等。
构建方法会以信息形式给出。
(2.官能团的引入和转化:
(1)官能团的引入:
思考与交流
1、引入碳碳双键的三种方法:
卤代烃的消去;醇的消去;炔烃的不完全加成。
2、引入卤原子的三种方法:
醇(或酚)的取代;烯烃(或炔烃)的加成;
烷烃(或苯及苯的同系物)的取代。
(2)官能团的转化:
包括官能团种类变化、数目变化、位置变化等。
3、引入羟基的四种方法:
烯烃与水的加成;卤代烃的水解;酯的水解;醛的还
原。
a.官能团种类变化:
CH3CH2-Br
水解
CH3CH2-
OH
氧化CH3-CHO
b.官能团数目变化:
CH3CH2-Br消去 CH2=CH2
加Br2
CH2Br-CH2Br
c.官能团位置变化:
CH3CH2CH2-Br消去 CH3CH=CH2
加HBrCH3CH-CH3
Br
二、有机合成的方法
1、有机合成的常规方法
(1)官能团的引入
①引入双键(C=C或C=O)
1)某些醇的消去引入C=C
CH3CH2 OH
浓硫酸
170℃
CH2==CH2↑ +H2O
醇
△ CH2=CH2↑+ NaBr+ H2O CH3CH2Br +NaOH
2)卤代烃的消去引入C=C
3)炔烃加成引入C=C
4)醇的氧化引入C=O
②引入卤原子(—X)
1)烃与X2取代
CH4 +Cl2 CH3Cl+ HCl光照
2CH3CH2OH+O2 2CH3CHO+2H2O催化剂
△
CH≡CH + HBr CH2=CHBr 催化剂
△
3)醇与HX取代
CH2==CH2+Br2 CH2BrCH2Br
2)不饱和烃与HX或X2加成
③引入羟基(—OH)
1)烯烃与水的加成
CH2==CH2 +H2O CH3CH2OH
催化剂
加热加压
2)醛(酮)与氢气加成
CH3CHO +H2 CH3CH2OH
催化剂
Δ
C2H5OH + HBr C2H5Br + H2O△
3)卤代烃的水解(碱性)
C2H5Br +NaOH C2H5OH + NaBr
水
△
4)酯的水解
稀H2SO4
CH3COOH+C2H5OHCH3COOC2H5 + H2O △
(2)官能团的消除
①通过加成消除不饱和键
②通过消去或氧化或酯化或取代等消除羟基
③通过加成或氧化消除醛基
④通过消去反应或水解反应可消除卤原子
(3)官能团的衍变
2、正向合成分析法
此法采用正向思维方法,从已知原料入手,
找出合成所需要的直接可间接的中间产物,逐步
推向目标合成有机物。
基础原料 中间体 中间体 目标化合物
正向合成分析法示意图
3、逆向合成分析法
是将目标化合物倒退一步寻找上一步反应的
中间体,该中间体同辅助原料反应可以得到目标
化合物。
基础原料中间体 中间体目标化合物
逆向合成分析法示意图
所确定的合成路线的各步反应,其反应条件
必须比较温和,并具有较高的产率,所使用物基
础原料和辅助原料应该是低毒性、低污染、易得
和廉价的。
2 C2H5OH
C—OC2H5
C—OC2H5
O
O
C—OH
C—OH
O
O
+
草酸二乙酯的合成
H2C—OH
H2C—OH
H2C—Cl
H2C—Cl
CH2
CH2
C—H
C—H
O
O
练习:用2-丁烯、乙烯为原料设计
的合成路线
认目标 巧切断 再切断 …… 得原料 得路线O
O
O
O
NaOH
C2H5O
H
O
O
O
O
1、逆合成分析:
C OH
C OH
O
O +
C H
C H
O
O
CH2
CH2
OH
OH
CH2
CH2
Br
Br
CH2
CH2
NaOH
水
2、合成路线:
CH2
CH2
Br2CH2
CH2
Br
Br
CH2
CH2
OH
OH
O2
Cu C H
C H
O
O
O2 C OH
C OH
O
O
浓H2SO4
OH
OH
Br
Br Br
Br
Br2Br
Br
Br2
Br
BrNaOH
水
OH
OH
O
O
O
O
第四节 有机合成(第二课时)
【预备知识回顾】
1、烷烃、烯烃、炔烃的制法及其主要化学性质
产物还有CH2Cl2、CHCl3、CCl4等。烷
烃及烷烃基的主要化学性质,注意反应条
件为光照
减少C原
子的方法
2
【预备知识回顾】
1、烷烃、烯烃、炔烃的制法及其主要化学性质
A—B为X2、HX、H2、H—OH、H—CN等
3
【预备知识回顾】
1、烷烃、烯烃、炔烃的制法及其主要化学性质
C=C和X2加成:往相邻碳上引入2个卤素原子;
C=C和HX加成:引入1个卤素原子;
C=C和水加成:引入一个羟基(—OH);
C=C和HCN加成:增长碳链。
4
【预备知识回顾】
1、烷烃、烯烃、炔烃的制法及其主要化学性质
化学性质:
和HX、X2、H2、H2O、HCN等加成
5
【预备知识回顾】
1、烷烃、烯烃、炔烃的制法及其主要化学性质
炔烃不完全加成:引入C=C。如:乙炔和
HCl反应生成CH2=CHCl,既引入了C=C
也引入了—X原子;
CH≡CH和水加成产物为乙醛:引入醛基
(或酮基) 。
6
【预备知识回顾】
2、苯及其同系物的化学性质
写出苯与液溴、浓硝酸和浓硫酸混合
液、浓硫酸、氢气反应的化学方程式。
思考:
如何往苯环上引入— X原子、—NO2、
—SO3H?如何将苯环转化为环己基?
7
2、苯及其同系物的化学性质
写出甲苯与浓硝酸和浓硫酸混合液反应的
化学方程式。
甲苯可以被酸性KMnO4溶液氧化为苯甲酸
此为往苯环上引入—COOH的方法
8
【预备知识回顾】
3、卤代烃的制取及其主要化学性质 引入一个卤
素(—X)原子往相邻碳上引
入2个卤素原子
9
【预备知识回顾】
3、卤代烃的制取及其主要化学性质
思考:
1、如何引入C=C?
2、如何引入羟基(—OH)?
化学性质:
请写出溴乙烷分别和NaOH水溶液、
NaOH醇溶液混合加热的化学方程式,
并指出其反应类型。
10
【预备知识回顾】
3、卤代烃的制取及其主要化学性质
一卤代烃的消去反应引入C=C、
一卤代烃的水解引入—OH
11
【预备知识回顾】
4、醇、醛、羧酸、酯的相互转化及其化学性质
请以乙醇为例写出上述转化的化学方程式:
思考:如何引入醇羟基、醛基、羧基、酯基
12
【预备知识回顾】
4、醇、醛、羧酸、酯的相互转化及其化学性质
乙醇的其它化学性质(写出化学方程式):
和金属钠的反应(置换反应) :
分子间脱水生成二乙醚(取代反应):
和HX的反应(取代反应) :
2Na + 2C2H5OH → 2C2H5ONa + H2↑
2C2H5OH ——→ C2H5OC2H5 + H2O
浓硫酸
140℃
HBr + C2H5OH → C2H5Br + H2O
引入卤素原子
的方法之一
13
【预备知识回顾】
4、醇、醛、羧酸、酯的相互转化及其化学性质
乙醛的其它化学性质(写出化学方程式):
和银氨溶液的反应:
和新制Cu(OH)2悬浊液的反应:
CH3CHO + 2Cu(OH)2 ——→
CH3COOH + Cu2O + 2H2O
CH3CHO + 2Ag(NH3)2OH ——→
CH3COONH4 + 2Ag + 3NH3 + H2O
此两反应为将
醛基氧化为羧
基的方法之一
14
5、酚的主要化学性质(写出化学方程式):
苯酚与NaOH溶液的反应(酸碱中和):
苯酚钠溶液中通入CO2气体:
15
C6H5OH+NaOH → C6H5ONa+H2O
C6H5ONa+CO2+H2O → C6H5OH+NaHCO3
【预备知识回顾】
(较强酸 制取 较弱酸)
5、酚的主要化学性质(写出化学方程式):
苯酚与FeCl3溶液反应,显特征的紫色
酚羟基可与羧酸反应生成酯,如:CH3COOC6H5
16
苯酚与溴水的反应(取代反应):
【预备知识回顾】
【归纳总结及知识升华 】
思考:
1、至少列出三种引入C=C的方法:
2、至少列出三种引入卤素原子的方法:
3、至少列出四种引入羟基(—OH)的方法:
4、在碳链上引入醛基和羧基的方法有:
5、如何增加或减少碳链?
17
【归纳总结及知识升华 】
思考:
1、至少列出三种引入C=C的方法:
(1) 卤代烃消去
(2) 醇消去
(3) C≡C不完全加成等
18
【归纳总结及知识升华 】
思考:
2、至少列出三种引入卤素原子的方法:
(1) 醇(或酚)和HX取代
(2) 烯烃(或炔烃)和HX、X2加成
(3) 烷烃(苯及其同系物)和X2的取代等
19
【归纳总结及知识升华 】
思考:
3、至少列出四种引入羟基(—OH)的方法:
(1) 烯烃和水加成
(2) 卤代烃和NaOH水溶液共热(水解)
(3) 醛(或酮)还原(和H2加成)
(4) 酯水解
(5) 醛氧化(引入—COOH中的—OH)等
20
【归纳总结及知识升华 】
思考:
4、在碳链上引入醛基和羧基的方法有:
醛基:
(1) R—CH2OH氧化
(2) 乙炔和水加成
(3) RCH=CHR‘ 适度氧化
(4) RCHX2水解等
21
【归纳总结及知识升华 】
思考:
4、在碳链上引入醛基和羧基的方法有:
羧基:
(1) R—CHO氧化
(2) 酯水解
(3) RCH=CHR' 适度氧化
(4) RCX3水解等
22
【归纳总结及知识升华 】
思考:
5、如何增加或减少碳链?
增加:
① 酯化反应
② 醇分子间脱水(取代反应)生成醚
③加聚反应
④缩聚反应
⑤ C=C或C≡C和HCN加成等
23
【归纳总结及知识升华 】
思考:
5、如何增加或减少碳链?
减少:
① 水解反应:酯水解,糖类、
蛋白质(多肽)水解
② 裂化和裂解反应;
③ 脱羧反应;
④ 烯烃或炔烃催化氧化(C=C或C≡C断开)等
24
【学以致用——解决问题 】
问题一
阅读课本,以乙二酸二乙酯为例,说明
逆推法在有机合成中的应用。
分析:
C — O — C2H5
C — O — C2H5
O
O
HO—
HO— H
H
CH2—OH
CH2—OH
CH2—Br
CH2—Br
请课后在学案中完成上述化学方程式
+H2O
25
【学以致用——解决问题 】
问题二
写出由乙烯制备乙酸乙酯的设计思路,并
写出有关的化学方程式 :
乙烯 乙醇 乙醛 乙酸
乙酸乙酯
请课后在学案中完成相应的化学方程式
26
问题三
化合物A最早发现于酸牛奶中,它是人体内糖代谢
的中间体,A的钙盐是人们喜爱的补钙剂之一。A在某
催化剂的存在下进行氧化,其产物不能发生银镜反应。
在浓硫酸存在下,A可发生如下图所示的反应:
试写出:
(1) 化合物A、B、C的结构简式: 、 、 。
(2) 化学方程式:A→D ,A→E 。
(3) 反应类型:A→D ,A→E 。
27
问题三 分析:
题中说“A的钙盐”,可知A含—COOH;
结合A的分子式,由A→C知,A还含有—OH,
由A在催化剂作用下被氧化的产物不能发生银
镜反应可知:A的—OH不在碳链的末端;3个
碳的碳链只有一种:C—C—C,—OH只能在中
间碳上。综上:A的结构简式为:CH3—CH—COOH
OH
28
问题三 分析:
A的结构简式为:CH3—CH—COOH
OH
则B的结构简式为:CH3—CH—COOC2H5
OH
则C的结构简式为:CH3—CH—O—C—CH3
COOH
O
29
问题三 分析:
A的结构简式为:CH3—CH—COOH
OH
则A→D的化学方程式为:
CH3—CH—COOH
OH
浓硫酸
H2O+CH2=CHCOOH
反应类型:消去反应
30
问题三 分析:
A的结构简式为:CH3—CH—COOH
OH
对比A和E的分子式,我们发现E的C原子
个数是A的2倍,推断可能是2分子的A反应生
成E,再对比H和O原子发现: 2A—E=2H2O,
结合A的结构简式,很明显是它们的羧基和醇
羟基相互反应生成酯基。所以:
31
问题三 分析:
将A的结构简式改写为:
则A生成E可表示为:
O
CH3—CH—C—OH
O
HO
CH3—CH—C—OH
O
H
HO—C—CH—CH3
O
O
H
H2O
H2O
即:
CH—C
CH3 O
O
C—CH
CH3O
O
C C
CC
O
O
32
问题三 分析:
则A→E的化学方程式为:
2CH3—CH—COOH
OH
浓硫酸
2H2O +
CH—C
CH3 O
O
C—CH
CH3O
O
反应类型: 酯化反应
33
【学以致用——解决问题 】
习题1、以2-丁烯为原料合成:
1) 2-氯丁烷
H3C C
H
C
H
CH3 +HCl H3C
H
C
H2
C CH3
Cl2) 2-丁醇H3C C
H
C
H
CH3 +H2O H3C
H
C
H2
C CH3
OH
3) 2,3-二氯丁烷
H3C C
H
C
H
CH3 +Cl2 H3C
H
C
H
C CH3
Cl Cl4) 2,3-丁二醇
H3C C
H
C
H
CH3 +Cl2 H3C
H
C
H
C CH3
Cl Cl
H3C
H
C
H
C CH3
Cl Cl
+2H2O H3C
H
C
H
C CH3
OH
NaOH
加热
OH
+2HCl
5) 1,3-丁二烯
H3C C
H
C
H
CH3 +Cl2 H3C
H
C
H
C CH3
Cl Cl
H3C
H
C
H
C CH3
Cl Cl
+2NaOH
C2H5OH
加热 H2C C
H
C
H
CH2 +2NaCl +2H2O
2、
1) + Cl2
光照
Cl
+ HCl
2)
Cl
+ NaOH C2H5OH
加热 + NaCl +H2O
3) + Cl2
Cl
Cl
4)
Cl
Cl
C2H5OH
加 热 + 2NaCl+ 2H2O+ 2NaOH
5) + Br2
Br
Br
6)Br
Br
+ H2
Br
Br
催化剂
7)Br
Br
加热 + 2NaBr+ 2NaOH
H2O HO
OH
8) + 2CH3COOH
HO
OH
浓硫酸
加热
H3CCOO
OOCCH3
+2H2O
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页