- 1.52 MB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
共用电子对
饱和性 方向性
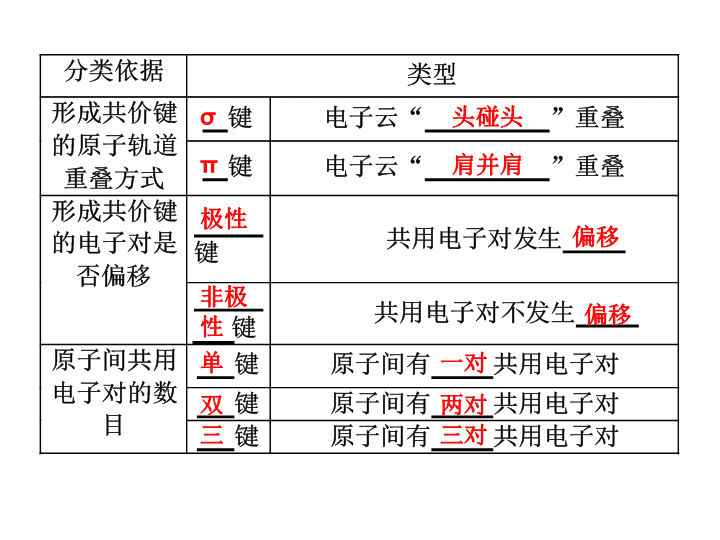
σ
π
头碰头
肩并肩
极性
非极
性
单
双
三
偏移
偏移
一对
两对
三对
大 短
稳定性
立体构型
4. 键参数
(1)概念
能量相近
2
3
4
180°
120°
109°28′
直线形
平面三角
形
四面
体形
BeCl2
BF3
CH4
直线形
平面正三
V形
正四面
三角锥
V形
BeCl2
BF3
SnBr2
CH4
NH3
H2O
角形
体形
形
中心原子的价电子数+每个配位原子提供的价电子数×m
2
重合 对称
不对称不重合
普遍
范德华力 氢键
组成和结构 相
对分子质量 增大
< <
电负性很强
氢原子
方向 饱和
电负性很强
分子内 分子间
升高
非极性溶剂
极性溶剂
越好
答案 C
答案 A
类
型
比较
2.范德华力、氢键、共价键的比较
答案 D
解析 由原子守恒可知A为K2S,其晶体类型
为离子晶体,含有极性共价键的分子为CO2,其中
心原子轨道杂化为sp杂化,N2中含有1个σ键和2个
π键,所以CN-中也含有1个σ键和2个π键,在
HCN中又多了一个H—C σ键,所以在HCN中σ键
和π键各为2个。
答案 ①O>N>C>K ②离子晶体 sp ③1∶ 1
答案 C
答案 D
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页