- 1.02 MB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第 二节
化学计量在实验中的应用
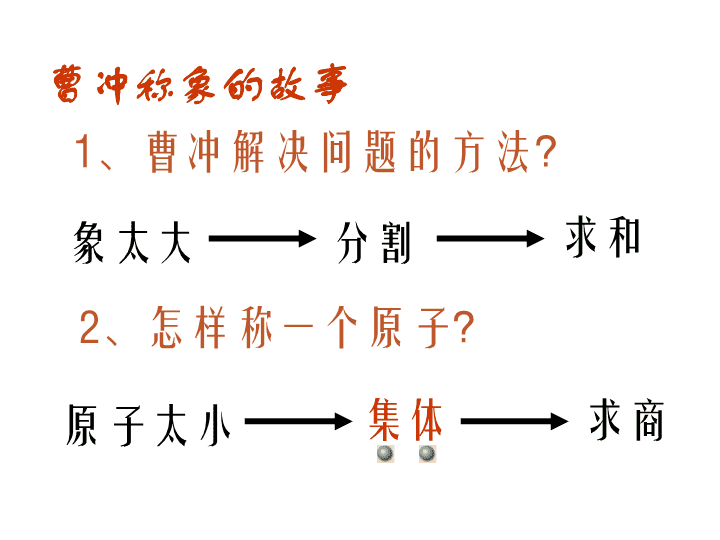
曹冲称象的故事
1、曹冲解决问题的方法?
2、怎样称一个原子?
象太大 分割 求和
原子太小 集体 求商
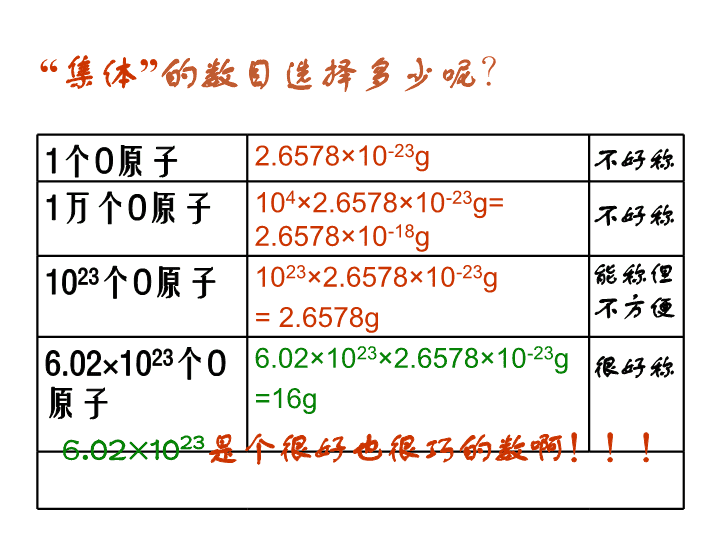
1个O原子 2.6578×10-23g
1万个O原子 104×2.6578×10-23g=
2.6578×10-18g
1023个O原子 1023×2.6578×10-23g
= 2.6578g
6.02×1023个O
原子
6.02×1023×2.6578×10-
23g
=16g
“集体”的数目选择多少呢?
不好称
不好称
能称但
不方便
很好称
6.02×1023是个很好也很巧的数啊!!!
6.02×1023 个H的质量
6.02×1023 个O的质量
6.02×1023 个Fe的质量
6.02×1023 个C的质量
6.02×1023 个OH-的质量
6.02×1023 个SO42-的质量
那么其他的微粒呢?
1g
16g
56g
12g
17g
96g
6.02×1023 个微粒称作1摩尔(1mol)
6.02×1023个O
6.02×1023个C
3.01×1023个H2O
9.03×1023个H
9.03×1023个H+
1.204×1024个NaCl
1.806×1024个SO42-
1mol O
1molC
0.5mol H2O
1.5mol H
1.5mol H+
2mol NaCl
3mol SO42-
16 g
12 g
9 g
1.5 g
1.5 g
117 g
288 g
一、物质的量:
衡量物质所含微粒多少的物理量。单位是摩尔(mol)
•每摩尔物质含有6.02×1023个该物质的微粒
•含有6.02×1023个时,该物质的物质的量为1mol
物质所含微粒数 物质的量(mol)
÷ 6.02×1023
6.02×1023×
•6.02×1023mol-1 叫做阿伏加德罗常数,符号NA
•使用摩尔时,必须指明粒子(原子、分子等)的种类
练习1:6.02×1023 个H的“物质的量”是_____
练习2: 1.204×1024 个H+的“物质的量”是_____
练习3: 1.806×1024 个e-的“物质的量”是_____
练习4: 2.107×1024 个H2O中
水的“物质的量”是_________,
氢原子的“物质的量”是________,
氧原子的“物质的量”是_________。
1 mol
2 mol
3 mol
3.5 mol
7 mol
3.5 mol
练习1:1 mol C中约含有————————个碳原子
练习2:1.5 mol H2O中约含有———————个水分
子
练习3:0.5 mol SO42-中约含有————————个SO42-离子
练习4: 1 mol 的Na2CO3中
含有———————— 个Na+
含有———————— 个CO32-离子,
总共含有———————— 个离子。
6.02×1023
9.03×1023
3.01×1023
1.806 ×1024
1.204×1024
6.02×1023
二、摩尔质量
1mol物质的质量称为该物质的摩尔质量,单位是g ● mol-
1.摩尔质量在数值上等于原子量或分子量、离子的式量。
Fe的摩尔质量是__________ 水的摩尔质量是__________
NaCl的摩尔质量是_________ OH-的摩尔质量是_________
2.摩尔质量的数学计算:
摩尔质量(g ● mol -)
质量(g)
物质的量(mol)
=
56 g · mol- 18 g · mol-
58.5 g · mol- 17 g · mol-
练习1:已知1.5 mol某气体的质量是48 g
(1)求这种气体的摩尔质量
(2)这种气体是_____
A.CO2 B.SO2 C.O2 D.NO
解:已知n=1.5 mol m=48 g
molgmol
g
n
mM ·325.1
48 ∴这种气体是O2
练习2:
(1)已知2.5 mol某物质的质量是75 g,其摩尔质量是
__________
(2)已知2 mol某物质的质量是142g ,其摩尔质量是
__________
30 g . mol-
71 g . mol-
练习2:
(1)1.5molCl2的质量是___________
(2)3molH2的质量是___________
(3)2.5molO2的质量是___________
(4)0.5molNaOH的质量是___________
(5)2molNaCl的质量是___________
(1)解:已知n=1.5 mol,M(Cl2) =71g ·mol-
gmolgmolMnm cl 5.106715.12
106.5 g
6 g
80 g
20 g
117 g
练习3:
(1) 142 g Cl2的物质的量是___________
(2) 24 g O2的物质的量是___________
(3) 60 g NaOH的物质的量是___________
(4) 80 g CuSO4的物质的量是___________
(5) 49 g H2SO4的物质的量是___________
解(1):已知m=142g M( Cl2 )=71g·mol-
molmolg
g
M
mn
cl
271
142
2
2mol
0.75mol
1.5mol
0.5mol
0.5mol
物质所含微粒数 物质的量(mol)
÷ 6.02×1023
6.02×1023×
一、物质的量:
衡量物质所含微粒多少的物理量。单位是摩尔(mol)
二、摩尔质量
1mol物质的质量称为该物质的摩尔质量,单位是g ● mol-
1.摩尔质量在数值上等于原子量或分子量、离子的式量。
2.摩尔质量的数学计算:
摩尔质量(g ● mol-) 质量(g)
物质的量(mol)=
阿伏加德罗常数
NA = 6.02×1023 mol-
用NA表示
微粒数(N) 物质的量(n)
÷ NA
NA×
质量(m)
×M(g·mol-)
M(g·mol-) ÷
要先求物质的量
要先求物质的量
例题:求1.204×1023个SO2的质量
解: molnSO 2.01002.6
10204.1
23
23
2
gmolgmolomSO 8.12642.2
练习:
1.求1.806 ×1023个CO2的质量;2.求9.03 ×1023个H2SO4的质量
例题:求32gSO2中氧原子的个数
解: mol5.0molg64
g32n 2SO
mol1mol5.02n2n 2SOO
练习:
1.求49 g硫酸中氧原子的个数;2.求48 g甲烷中氢原子的个数
2323 10026100261 ..NnN AOO
相关文档
- 2018年高考数学考点突破教学课件:9_2021-07-0242页
- 2018年高考数学考点突破教学课件:112021-07-0142页
- 2018年高考数学考点突破教学课件:2_2021-07-0157页
- 人教版高三数学总复习教学课件:2-52021-07-0163页
- 高中数学选修2-3教学课件:3_1回归分2021-07-0135页
- 高中数学选修2-2教学课件第2讲《函2021-07-0128页
- 人教版高三数学总复习教学课件:9-42021-07-0182页
- 高中数学选修2-3教学课件:独立性检2021-07-0119页
- 人教版高三数学总复习教学课件:7-62021-07-0168页
- 高中数学选修2-3教学课件:离散型随2021-07-0120页