- 298.50 KB
- 2021-08-24 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
四川省仁寿第二中学2020-2021学年高一上学期第一次月考试题
考试时间:90分钟
学校:___________姓名:___________班级:___________考号:___________
题号
一
二
总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题)
请点击修改第I卷的文字说明
评卷人
得分
一、选择题(本题共20道小题,每小题0分,共0分)
1.屠呦呦是我国第一位诺贝尔医学奖获得者,她从青蒿中提取青蒿素的过程中,多次采用萃取操作。该操作中涉及的主要仪器是( )
A. B. C. D.
2.当光束通过下列分散系,能观察到丁达尔效应的是( )
A. 食盐水 B. 豆浆 C. 食醋 D. 白酒
3.关于容量瓶的使用,下列操作正确的是( )
A. 使用前要检验容量瓶是否漏液
B. 用蒸馏水荡洗后必须要将容量瓶烘干
C. 为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
D. 为了使所配溶液浓度均匀,定容后,手握瓶颈,左右振荡
4.实验室欲用如图流程从碘水中获得碘单质(已知碘单质易升华)。下列说法错误的是( )
A. 溶剂X可以是四氯化碳或者无水乙醇
B. 操作2和3均需使用分液漏斗
C. 试剂Y的作用是将有机溶液中的碘单质“反萃取”进入水溶液2
D. 固体碘宜在低温下干燥
5.实验室因上次实验还剩有9.0 mL 的18 mol/L的浓硫酸和大量的9 mol/L的硫酸,实验员为了准备下次实验需要0.5 mol/L的稀硫酸500mL,决定将浓硫酸全部使用,请问本次实验还需要用量筒取9 mol/L的硫酸体积为( )
A. 9.78 mL B. 19.56 mL C. 9.8 mL D. 10.0 mL
6.在配制溶液时,下列情况会使所配溶液浓度偏高的是
A. 溶液转移到容量瓶中后,烧杯及玻璃棒未用蒸馏水洗涤
B. 定容时,仰视容量瓶的刻度线
C. 有些固体溶解会放热,未经冷却后立即将其转移至容量瓶中
D. 定容后摇匀,发现液面降低,又补加少量蒸馏水至刻度线
7.在三个密闭容器中分别充入N2、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A. p(N2)>p(H2)>p(O2) B. p(H2)>p(N2)>p(O2)
C. p(N2)>p(O2)>p(Ne) D. p(O2)>p(N2)>p(H2)
8.配制一定物质的量浓度的硫酸溶液涉及多步操作,其中下列图示操作正确的是( )
A. B.
C. D.
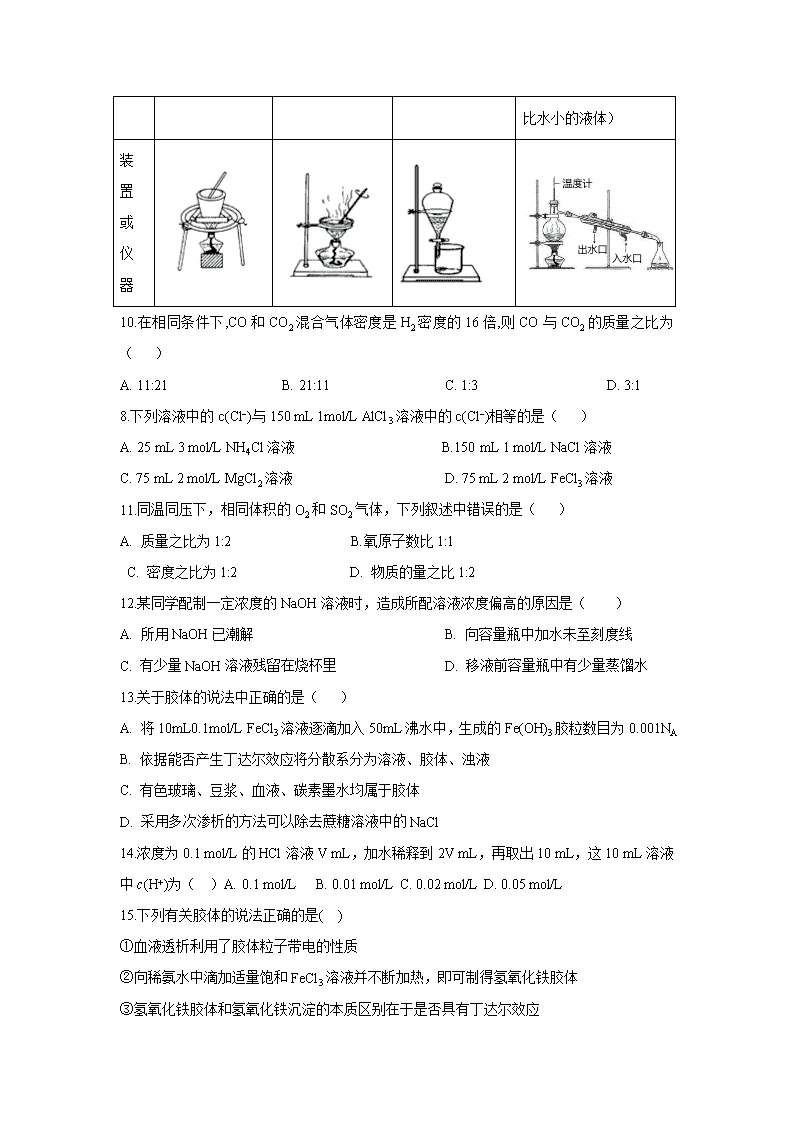
9.完成下列实验所选择的装置或仪器正确的是( )
选项
A
B
C
D
实验
从食盐水中提取NaCl固体
分离碘和泥沙
分离水和四氯化碳
分离Na2SO4
溶液和苯(苯是难溶于水,密度比水小的液体)
装置或仪器
10.在相同条件下,CO和CO2混合气体密度是H2密度的16倍,则CO与CO2的质量之比为( )
A. 11:21 B. 21:11 C. 1:3 D. 3:1
8.下列溶液中的c(Cl−)与150 mL 1mol/L AlCl3溶液中的c(Cl−)相等的是( )
A. 25 mL 3 mol/L NH4Cl溶液 B.150 mL 1 mol/L NaCl溶液
C. 75 mL 2 mol/L MgCl2溶液 D. 75 mL 2 mol/L FeCl3溶液
11.同温同压下,相同体积的O2和SO2气体,下列叙述中错误的是( )
A. 质量之比为1:2 B.氧原子数比1:1
C. 密度之比为1:2 D. 物质的量之比1:2
12.某同学配制一定浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A. 所用NaOH已潮解 B. 向容量瓶中加水未至刻度线
C. 有少量NaOH溶液残留在烧杯里 D. 移液前容量瓶中有少量蒸馏水
13.关于胶体的说法中正确的是( )
A. 将10mL0.1mol/L FeCl3溶液逐滴加入50mL沸水中,生成的Fe(OH)3 胶粒数目为0.001NA
B. 依据能否产生丁达尔效应将分散系分为溶液、胶体、浊液
C. 有色玻璃、豆浆、血液、碳素墨水均属于胶体
D. 采用多次渗析的方法可以除去蔗糖溶液中的NaCl
14.浓度为0.1 mol/L的HCl溶液V mL,加水稀释到2V mL,再取出10 mL,这10 mL溶液中c(H+)为( )A. 0.1 mol/L B. 0.01 mol/L C. 0.02 mol/L D. 0.05 mol/L
15.下列有关胶体的说法正确的是( )
①血液透析利用了胶体粒子带电的性质
②向稀氨水中滴加适量饱和FeCl3溶液并不断加热,即可制得氢氧化铁胶体
③氢氧化铁胶体和氢氧化铁沉淀的本质区别在于是否具有丁达尔效应
④在制备Fe(OH)3胶体实验中,不断搅拌可使反应更充分
⑤向Fe(OH)3胶体中加入过量稀硝酸,先有红褐色沉淀生成,然后沉淀溶解
A. 1个 B. 2个 C. 3个 D. 4个
16.由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比为( )
A. 29∶8∶13 B. 22∶1∶14
C. 13∶8∶29 D. 44∶2∶28
17.三种气体X、Y、Z的相对分子质量关系为Mr(X)ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的_______端口放出,有机层应由分液漏斗的________端口放出(此问填“上”或者“下”) ;
(2)蒸馏
①冷凝装置中冷凝水应该___ ____口进(填“上”或“下”)
②已知碘和四氯化碳的熔沸点数据如下表
②已知碘和四氯化碳的熔沸点数据如下表
熔点
沸点
碘
113.7℃
184.3℃
四氯化碳
-22.6℃
76.8℃
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是__ _______。
24.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读并回答下列问题:
成分
成分的质量(g)
摩尔质量(g•mol﹣1)
蔗糖
25.00
342
硫酸钾
0.87
174
阿司匹林
0.17
180
高锰酸钾
0.316
158
硝酸银
0.02
170
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 mol/L(要求:用原始数据写出表达式即可,不需要化简与计算)
(2)配制上述“鲜花保鲜剂”所的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、 (填所缺仪器的名称).
(3)在溶液配制过程中,下列操作对配制结果没有影响的是 .
A.定容时,俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)若要配制0.5mol/L 500mL的硫酸溶液,则:
①所需质量分数为98%、密度为1.84g.cm﹣3的浓硫酸的体积为 (计算结果保留一位小数)mL;
②如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸稀释,稀释时操作方法是 .
25.I.甘肃马家密遗址出土的青铜刀是我国最早治炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜録”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
(1)从物质分类标准看,“铜绿”属于______(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:____________。
(3)请写出铜録与盐酸反应的化学方程式:________________________。
(4)上述转化过程中属于化合反应的是_______________(填序号)
II.胶体是一种常见的分散系,回答下列问题。用Fe(OH)3胶体进行下列实验:
(5)将其装入U型管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色_______,这说明_________,这种现象称为____________________________。
(6)向其中滴入过量稀硫酸,现象是___________,其原因是______________________。
【参考答案】
1.D 2.B 3.A 4.A 5.C 6.C 7.B 8.D 9.C 10.B 11.D 12.B .13.C 14.D 15.A 16.C17.B
18.C 19.A 20.D
21.(1)9.03×1023 33.6 18 (2) 2:3
(3)4:5 4:5 (4) 64g/mol (5)0.025mol
(第二小问2分,其余每空1分)
22. (1) B;(2) D;(3) C;(4) A;(5) A。
II.(1)① B ② 检查是否漏液;
③ 下, 上;
(2)① 下 ②四氯化碳。(每空1分)
23.(1)坩埚(或蒸发皿或试管) 酒精灯
(2)溶液中引入新的杂质离子NO3-
(3)取少量上层清液加入BaCl2溶液,若无白色沉淀说明SO42-已除尽
(4)除去过量的Ba2+
(5)除去溶解在溶液中的CO2和HCl(每空2分)
24.(1)0.024mol/L;
(2)500mL容量瓶;胶头滴管;
(3)BD;
(4)①13.6;②15;③将浓硫酸沿烧杯壁注入水中并用玻 璃棒不断搅拌;
(除第4小题第二空1分以外每空2分)
25.(1)C(1分) (2)CuO (3)Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑ (3分)
(4)①(1分) (5)加深 胶体粒子带(正)电荷 电泳
(6)先出现红褐色沉淀后沉淀溶解
开始加入稀硫酸时,胶体发生聚沉生成氢氧化铁沉淀,当酸过量时,又将氢氧化铁溶解
(除标注外每空2分)