- 279.52 KB
- 2021-08-24 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
专题十八 水的电离和溶液的酸碱性
考点1 水的电离
1.[2020福建三明第一中学模拟]某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述不正确的是( )
A.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性
B.该温度高于25 ℃
C.加入NaHSO4晶体抑制了水的电离
D.该溶液中由水电离出来的H+浓度是1.0×10-10 mol·L-1
2.[2020浙江宁波新高考适应性考试]下列说法正确的是( )
A.25 ℃时某溶液中水电离出的c水(H+)=1.0×10-12 mol·L-1,其pH一定是12
B.某温度下,向氨水中通入CO2,随着CO2的通入,c(OH-)c(NH3·H2O)不断增大
C.恒温恒容下,反应X(g)+3Y(g)2Z(g),起始时充入3 mol X和3 mol Y,当X的体积分数不变时,反应达到平衡
D.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,该温度下加入等体积pH=10的NaOH溶液可使反应后的溶液恰好呈中性
3.[2020广东惠州第二次调研]如图是不同温度(T1、T2)下溶液中水的离子积常数Kw变化曲线,有关说法正确的是( )
A.图中温度T1A=D=E
9
D.E、D两点水的电离均被抑制,而Kw相等
4.[2019贵州贵阳监测考试,6分]25 ℃时,有pH均为9的NaOH溶液和CH3COONa溶液。回答下列问题:
(1)两溶液中c(H+)·c(OH-)= 。
(2)各取10 mL上述溶液,分别加水稀释至100 mL,pH较大的是 溶液。
(3)各取10 mL上述溶液,分别加热至90 ℃,pH较小的是 溶液。
(4)两溶液中由水电离出的c(OH-)分别为NaOH溶液 ;CH3COONa溶液 。
(5)取10 mL CH3COONa溶液,加水稀释至100 mL,c(CH3COO-)c(OH-)的值 (填“增大”“减小”或“不变”)。
考点2 溶液的酸碱性与pH
5.[2020福建三明一中模拟]常温下,关于溶液的稀释下列说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.将1 L 0.1 mol·L-1的Ba(OH)2溶液稀释为2 L,pH=13
C.pH=4的H2SO4溶液加水稀释100倍,溶液中由水电离产生的c水(H+)=1.0×10-6 mol·L-1
D.pH=8的NaOH溶液稀释100倍,其pH=6
6.[2020河南洛阳第一次联考]常温下0.1 mol·L-1的①CH3COOH 溶液、②NaOH溶液、③CH3COONa溶液,下列叙述正确的是( )
A.①中c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合后,溶液呈酸性,则c(Na+)>c(CH3COO-)>c(H+)
D.①②等体积混合后,水的电离程度比①③等体积混合后的电离程度小
9
考点3酸碱中和滴定
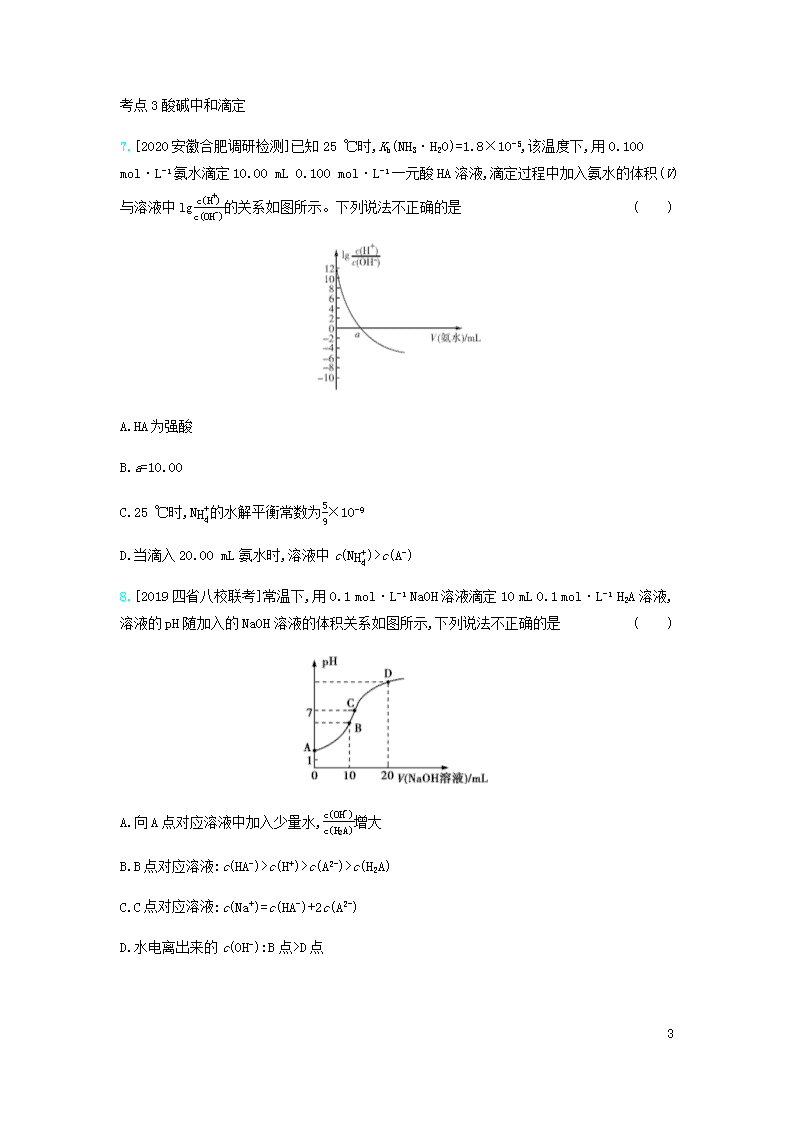
7.[2020安徽合肥调研检测]已知25 ℃时,Kb(NH3·H2O)=1.8×10-5,该温度下,用0.100 mol·L-1氨水滴定10.00 mL 0.100 mol·L-1一元酸HA溶液,滴定过程中加入氨水的体积(V)与溶液中lgc(H+)c(OH-)的关系如图所示。下列说法不正确的是( )
A.HA为强酸
B.a=10.00
C.25 ℃时,NH4+的水解平衡常数为59×10-9
D.当滴入20.00 mL氨水时,溶液中c(NH4+)>c(A-)
8.[2019四省八校联考]常温下,用0.1 mol·L-1 NaOH溶液滴定10 mL 0.1 mol·L-1 H2A溶液,溶液的pH随加入的NaOH溶液的体积关系如图所示,下列说法不正确的是( )
A.向A点对应溶液中加入少量水,c(OH-)c(H2A)增大
B.B点对应溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
C.C点对应溶液:c(Na+)=c(HA-)+2c(A2-)
D.水电离出来的c(OH-):B点>D点
9
一、选择题
1.[2020四川成都摸底测试]下列有关电解质溶液的说法正确的是( )
A.0.1 mol·L-1氨水中滴入等浓度等体积的醋酸溶液,溶液导电性增强
B.适当升高温度,CH3COOH溶液pH增大
C.稀释0.1 mol·L-1 NaOH溶液,水的电离程度减小
D.向CH3COONa溶液中加入少量CH3COOH,c(CH3COO-)c(CH3COOH)·c(OH-)减小
2.[2020四川成都外国语学校模拟]25 ℃时,将0.01 mol·L-1 NaOH溶液滴入20 mL 0.01 mol·L-1 CH3COOH溶液的过程中,溶液中由水电离出的c水(H+)与加入NaOH溶液体积的关系如图所示。下列说法正确的是( )
A.x=20,a点的纵坐标为1.0×10-12
B.b点和d点所示溶液的pH相等
C.滴定过程中,c(CH3COO-)c(OH-)逐渐增大
D.e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)
3.[2020山东潍坊期中考试]将等浓度的H2SO4、NaHSO4溶液分别滴入两份相同的Ba(OH)2溶液中,溶液电导率与滴入溶液的体积的关系如图所示。下列分析正确的是( )
9
A.b→d反应的离子方程式为H++OH-H2O
B.d点所示溶液中,Na+与SO42-的物质的量之比为1∶1
C.c点所示溶液导电能力相同,所以两溶液中含有相同量的OH-
D.a、b两点所示溶液中Ba2+均沉淀完全,所以对应的溶液均显中性
4.[水的离子积常数的应用]已知:pOH=-lg c(OH-)、pKw=-lg Kw、AG= lgc(H+)c(OH-)。在某弱酸HX及其钠盐NaX的混合溶液中(HX和NaX的含量不确定),c(H+)和 c(OH-)存在如图所示的关系,则下列说法不正确的是( )
A.T2>T1=25 ℃
B.AG=14-2pH
C.AB线段上任意点对应的溶液均有pH=pOH=pKw2
D.图中D点对应的溶液中c(Na+)c(HY-)>c(H+)>c(OH-)
8.[一元碱滴定一元酸溶液中的微粒分布分数图像]常温下,往一定浓度的醋酸溶液中加入NaOH溶液,所得溶液pX(X表示CH3COOH或CH3COO-,pX表示对应微粒物质的量浓度的负对数)与pH的关系如图所示。下列叙述错误的是( )
A.曲线A代表pX(X表示CH3COO-)与pH的关系
B.常温下,Ka(CH3COOH)的数量级为10-5
C.水的电离程度:X
相关文档
- 2020高考化学刷题冲刺含最新模拟题2021-08-2412页
- 2020高考化学刷题冲刺(含最新模拟题2021-08-2426页
- 2020高考化学刷题冲刺(含最新模拟题2021-08-2411页
- 2020高考化学刷题冲刺含最新模拟题2021-08-2413页
- 2020高考化学刷题冲刺(含最新模拟题2021-08-2416页
- 2020高考化学刷题冲刺含最新模拟题2021-08-2317页
- 2020高考化学刷题冲刺含最新模拟题2021-08-2313页
- 2020高考化学刷题冲刺含最新模拟题2021-08-2317页
- 2020高考化学刷题冲刺(含最新模拟题2021-08-2312页
- 2020高考化学刷题冲刺(含最新模拟题2021-08-2312页