- 263.50 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019年湖南省岳阳市中考化学试卷
一、选择题(每小题只有一个选项符合题意,本题共15道小题,每小题3分,共45分)
1.(3分)中华传统文化博大精深。下列成语中涉及化学变化的是( )
A.刻舟求剑 B.滴水成冰 C.钻木取火 D.掩耳盗铃
2.(3分)下列物质属于纯净物的是( )
A.干冰 B.石油 C.生理盐水 D.水泥砂浆
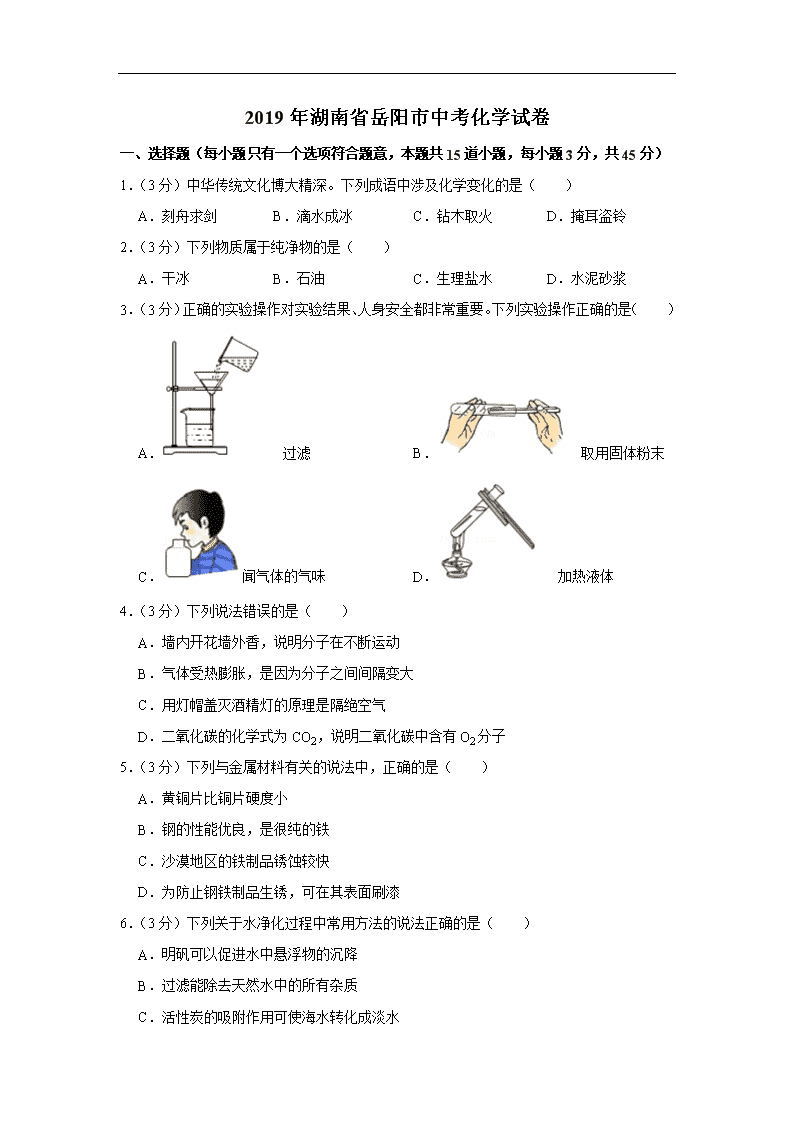
3.(3分)正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是( )
A. 过滤 B. 取用固体粉末
C.闻气体的气味 D. 加热液体
4.(3分)下列说法错误的是( )
A.墙内开花墙外香,说明分子在不断运动
B.气体受热膨胀,是因为分子之间间隔变大
C.用灯帽盖灭酒精灯的原理是隔绝空气
D.二氧化碳的化学式为CO2,说明二氧化碳中含有O2分子
5.(3分)下列与金属材料有关的说法中,正确的是( )
A.黄铜片比铜片硬度小
B.钢的性能优良,是很纯的铁
C.沙漠地区的铁制品锈蚀较快
D.为防止钢铁制品生锈,可在其表面刷漆
6.(3分)下列关于水净化过程中常用方法的说法正确的是( )
A.明矾可以促进水中悬浮物的沉降
B.过滤能除去天然水中的所有杂质
C.活性炭的吸附作用可使海水转化成淡水
D.过滤或加热均能使硬水转化成软水
7.(3分)金属钒被誉为“金属的维生素”,其化合物五氧化二钒是工业制硫酸的催化剂,五氧化二钒(V2O5)中钒元素的化合价是( )
A.﹣3 B.+1 C.+3 D.+5
8.(3分)锑是一种重要的稀土金属,湖南是锑的主要产地之一。下列关于锑的说法正确的是( )
A.相对原子质量为51
B.元素符号为Sb
C.原子的核外电子数为121.8
D.该元素为非金属元素
9.(3分)下列有关实验现象的描述,错误的是( )
A.木炭在氧气中燃烧,生成无色气体
B.硫在氧气中燃烧,发出淡蓝色火焰
C.红磷在空气中燃烧,产生大量白烟
D.铁丝在氧气中燃烧,火星四射,生成黑色固体
10.(3分)空气是一种宝贵的自然资源。下列有关空气的说法正确的是( )
A.氮气约占空气体积的21%
B.氧气能助燃,可以作燃料
C.稀有气体化学性质不活泼,不与任何物质发生反应
D.空气中二氧化碳含量过高会加剧温室效应
11.(3分)如图是两种粒子结构示意图,从图中获得的信息不正确的是( )
A.①和②的核外电子层数不同
B.②易得到6个电子形成稳定结构
C.②表示原子
D.①表示阴离子
12.(3分)习近平总书记视察岳阳时,殷殷嘱托“守好一江碧水。”作为岳阳的主人,你认为下列做法正确的是( )
A.工业废水随意排放
B.生活垃圾直接扔入江河
C.挖砂船常年日夜不停采砂
D.生活污水实现集中处理和排放
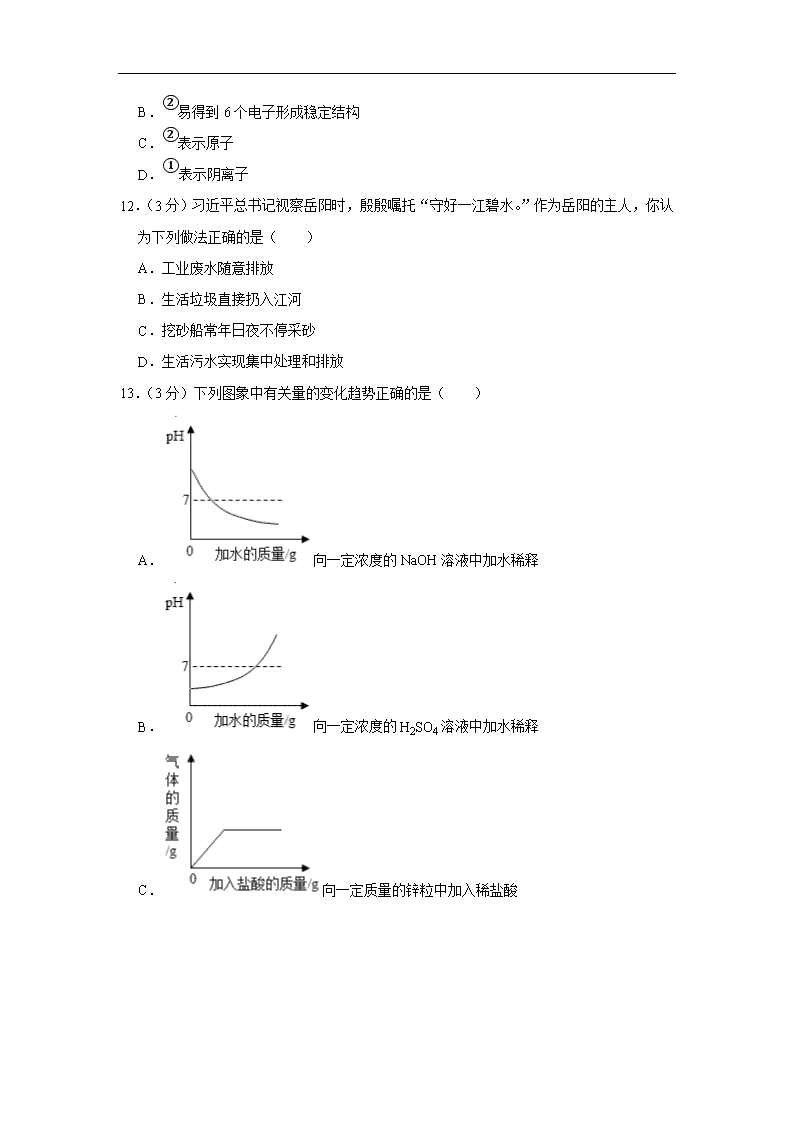
13.(3分)下列图象中有关量的变化趋势正确的是( )
A.向一定浓度的NaOH溶液中加水稀释
B.向一定浓度的H2SO4溶液中加水稀释
C.向一定质量的锌粒中加入稀盐酸
D.向接近饱和的KNO3溶液中加入KNO3晶体
14.(3分)下列实验操作或方法能达到实验目的是( )
选项
实验目的
实验操作或方法
A
鉴别稀硫酸和氯化钠溶液
滴加酚酞溶液
B
从粗盐中得到纯净的氯化钠
溶解、过滤、洗涤、干燥
C
鉴别K2SO4、Cu(NO3)2、Ba(OH)2、NaOH
不另加试剂
D
除去CO2中含有的少量CO
点燃
A.A B.B C.C D.D
15.(3分)向AgNO3和Cu(NO3)2的混合液中加入一定量的Fe、Cu的混合粉末,充分反应后过滤、洗涤,得到滤液和滤渣。下列说法正确的是( )
A.滤渣中一定有Ag,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3
B.当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Fe
C.向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag
D.向滤液中加入KCl溶液,无明显现象,则滤液中一定有 Fe(NO3)2、Cu(NO3)2,滤渣中可能有Fe、Cu
二、填空与简答题(本题共5道小题,每空2分,共32分)
16.(4分)用正确的化学符号填空:
(1)氮分子 ;
(2)氧化铁 。
17.(6分)现有下列物质①大理石②稀硫酸③干冰④碳酸氢钠⑤氦气,请选择合适物质的序号填空:
(1)常用于人工降雨的是 ;
(2)常用于焙制糕点的是 ;
(3)常用于建筑材料的是 。
18.(6分)A、B、C三种晶体(不含结晶水)的溶解度曲线如图,请回答:
(1)P点的含义是 ;
(2)t2℃时,将30gA物质加入50g水中可以得到 g溶液;
(3)欲将适量B物质的不饱和溶液变成饱和溶液,可采用的方法是 (任答一种即可)。
19.(10分)能源、材料、健康和安全关系着社会的发展。请回答:
(1)煤、石油、天然气属于 能源(填“可再生”或“不可再生”);
(2)岳阳三荷机场航站楼采用了钢结构和索膜结构的施工技术。索膜结构膜面材料的主要成分是聚四氟乙烯,俗称“塑料王”。聚四氟乙烯属于 材料(填“金属”或“有机合成”);
(3)华为开创了“中国芯”时代。“中国芯”的主要材料是高纯度的单质硅,工业上可用SiO2和碳单质在高温条件下反应来制取,反应同时生成一种可燃性气体。请写出该反应的化学方程式 ;
(4)安全是一个永恒的话题,下列做法错误的是 (填序号);
A.燃气泄漏,用打火机检验 B.电器着火,先关闭电源
C.点燃氢气前先检验纯度 D.不食用发霉的蛋糕
(5)小丽设计了一份中考期间的食谱:米饭、红烧肉、清蒸鱼、牛奶,你认为还应该增加的食物是 (填序号)。
A.牛肉 B.鸡肉 C.蔬菜
20.(6分)A、B、C、D、E、F是初中化学常见的物质,按单质、氧化物、酸、碱、盐分类,它们分别属于其中的四类物质。它们相互转化的关系如图所示(部分生成物和反应条件已省略)。已知:A物质由三种元素组成,其中两种元素的质量比为1:2;F为一种红色固体:D、F属同一类物质,C、E属同一类物质。请回答:
(1)C与D反应的基本类型为 ;
(2)A的化学式为 ;
(3)A与B反应的化学方程式为 。
三、实验与探究题(本题共2道小题,每小题8分,共16分)
21.(8分)实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
(1)实验室制取二氧化碳所选用的收集装置是 ,反应的化学方程式是 。
(2)若用高锰酸钾制取氧气,并用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是 (填字母)。
A.③④①②⑤
B.④③①②⑤
C.④③①⑤②
D.①②③④⑤
(3)若要除去氧气中混有的水蒸气,气体应从F装置的 端进入。
22.(8分)某化学课堂正在进行,以下是教学片断。请你参与他们的学习并完成相关任务。
【演示实验】老师按如图所示连接好装置,加入NaHCO3粉末,点燃酒精灯,对试管预热后集中加热,烧杯中澄清石灰水变浑浊,说明生成了CO2.继续加热至无气体产生后撤出导管,熄灭酒精灯。
【问题提出】实验后,同学们对试管中剩余的固体粉末产生了兴趣:剩余粉末由什么物质组成?
【猜想假设】在老师的指导下,同学们对固体粉末作出了如下猜想:
猜想一:NaOH;猜想二:NaOH和Na2CO3;猜想三:Na2CO3。
【实验探究】
实验方案
实验操作
实验现象
方案一
取适量粉末溶于水后向溶液中滴入2滴酚酞溶液,摇匀
溶液由无色变红色
小明根据实验现象认为猜想一成立。小组讨论后,大家认为小明的结论不合理,理由是 。
实验方案
实验操作
实验现象
实验结论
方案二
步骤一
取适量粉末溶于水后加
入过量的BaCl2溶液
猜想一不成立
步骤二
取步骤一的上层清液加入MgCl2溶液2﹣3mL
无明显现象
猜想三成立
【评价交流】小华认为步骤二也可以用MgSO4代替MgCl2,大家不同意他的观点,理由是 。
【拓展延伸】请你总结上述实验成果,写出碳酸氢钠受热分解的化学方程式 。
四、计算题(本题共2道小题,第46题2分,第47题5分,共7分)
23.(2分)葡萄中含有丰富的白藜芦醇(化学式(C14H12O3
),它具有抗癌作用,能抑制癌细胞的增生。请计算:
(1)一个白藜芦醇分子由 个原子构成;
(2)白藜芦醇中氢元素和氧元素的质量比为 (填最简整数比)。
24.(5分)现有一含NaCl杂质的Na2CO3样品,取13.9g样品溶于水,配成104.4g溶液,此溶液与100g某浓度的盐酸恰好完全反应,得到200g溶液。请计算:
(1)生成的二氧化碳的质量为 g;
(2)所得溶液中NaCl的质量分数(写出计算步骤)。
2019年湖南省岳阳市中考化学试卷
参考答案与试题解析
一、选择题(每小题只有一个选项符合题意,本题共15道小题,每小题3分,共45分)
1.(3分)中华传统文化博大精深。下列成语中涉及化学变化的是( )
A.刻舟求剑 B.滴水成冰 C.钻木取火 D.掩耳盗铃
【分析】有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化,刻舟求剑、滴水成冰、掩耳盗铃都属于物理变化。化学变化的特征是:有新物质生成。判断物理变化和化学变化的依据是:是否有新物质生成。
【解答】解:A、刻舟求剑没有新物质生成,属于物理变化;故选项错误;
B、滴水成冰没有新物质生成,属于物理变化;故选项错误;
C、钻木取火,燃烧属于化学变化;故选项正确;
D、掩耳盗铃没有新物质生成,属于物理变化;故选项错误;
故选:C。
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决。本考点主要出现在选择题和填空题中。
2.(3分)下列物质属于纯净物的是( )
A.干冰 B.石油 C.生理盐水 D.水泥砂浆
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,石油、生理盐水、水泥砂浆都属于混合物;纯净物是由一种物质组成。纯净物又分为单质和化合物。由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物。
【解答】解:A、干冰是二氧化碳的固体,属于纯净物;故选项正确;
B、石油中有汽油、煤油、柴油等,属于混合物;故选项错误;
C、生理盐水中有氯化钠和水,属于混合物;故选项错误;
D、水泥砂浆中有多种物质,属于混合物;故选项错误;
故选:A。
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基本概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
3.(3分)正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是( )
A. 过滤 B. 取用固体粉末
C.闻气体的气味 D. 加热液体
【分析】A、过滤液体时,注意“一贴、二低、三靠”的原则。
B、根据向试管中装粉末状固体药品的方法(“一斜、二送、三直立”)进行分析判断。
C、根据闻气体的气味时的方法(招气入鼻法)进行分析判断。
D、根据给试管中的液体加热的方法进行分析判断。
【解答】解:A、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错误。
B、取用粉末状药品,试管横放,用药匙或纸槽把药品送到试管底部,图中所示操作正确。
C、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作错误。
D、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的,图中液体超过试管容积的,图中所示操作错误。
故选:B。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
4.(3分)下列说法错误的是( )
A.墙内开花墙外香,说明分子在不断运动
B.气体受热膨胀,是因为分子之间间隔变大
C.用灯帽盖灭酒精灯的原理是隔绝空气
D.二氧化碳的化学式为CO2,说明二氧化碳中含有O2分子
【分析】A、根据分子的基本性质,进行分析判断。
B、根据分子的基本性质,进行分析判断。
C、根据灭火原理:①清除或隔离可燃物,②隔绝氧气或空气,③使温度降到可燃物的着火点以下,进行分析判断。
D、根据二氧化碳的微观构成,进行分析判断。
【解答】解:A、墙内开花墙外香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,故选项说法正确。
B、气体受热膨胀,是因为温度升高,分子之间间隔变大,故选项说法正确。
C、用灯帽盖灭酒精灯的原理是隔绝氧气,故选项说法正确。
D、二氧化碳是由二氧化碳分子构成的,不含氧分子,故选项说法错误。
故选:D。
【点评】本题难度难度,掌握灭火的原理、分子的基本性质、常见物质的微观构成是正确解答本题的关键。
5.(3分)下列与金属材料有关的说法中,正确的是( )
A.黄铜片比铜片硬度小
B.钢的性能优良,是很纯的铁
C.沙漠地区的铁制品锈蚀较快
D.为防止钢铁制品生锈,可在其表面刷漆
【分析】A、根据合金的性质,进行分析判断。
B、根据钢是铁的合金,进行分析判断。
C、铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果。
D、铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈。
【解答】解:A、合金的硬度比组成它的纯金属的硬度大,黄铜片比铜片硬度大,故选项说法错误。
B、钢的性能优良,钢是铁的合金,不是很纯的铁,故选项说法错误。
C、沙漠地区的铁制品,不易与水蒸气接触,不易生锈,故选项说法错误。
D、为防止钢铁制品生锈,可在其表面刷漆,以隔绝氧气和水,故选项说法正确。
故选:D。
【点评】本题难度不大,掌握铁锈蚀的条件、防止铁制品生锈的原理(隔绝氧气和水)与措施是正确解答本题的关键。
6.(3分)下列关于水净化过程中常用方法的说法正确的是( )
A.明矾可以促进水中悬浮物的沉降
B.过滤能除去天然水中的所有杂质
C.活性炭的吸附作用可使海水转化成淡水
D.过滤或加热均能使硬水转化成软水
【分析】A、明矾可以促进水中悬浮物的沉降正确;B、过滤是把不溶性固体与液体分开的一种方法;C、活性炭的吸附作用可使海水转化成淡水错误;D、降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏。
【解答】解:A、明矾可以促进水中悬浮物的沉降正确,故选项正确;
B、过滤能除去天然水中的所有杂质错误,不能除去可溶性杂质;故选项错误;
C、活性炭的吸附作用可使海水转化成淡水错误,故选项错误;
D、过滤或加热均能使硬水转化成软水错误,故选项错误;
故选:A。
【点评】本考点属于结合课本知识的信息,也体现了性质决定用途,用途反映性质的理念。还结合了新课标中的一个新的考点硬水与软水的区分,一定要加强记忆,综合应用。本考点主要出现在填空题和选择题中。
7.(3分)金属钒被誉为“金属的维生素”,其化合物五氧化二钒是工业制硫酸的催化剂,五氧化二钒(V2O5)中钒元素的化合价是( )
A.﹣3 B.+1 C.+3 D.+5
【分析】根据在化合物中正负化合价代数和为零,结合五氧化二钒的化学式进行解答即可。
【解答】解:氧元素显﹣2价,设钒元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(﹣2)×5=0,则x=+5价。
故选:D。
【点评】本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题。
8.(3分)锑是一种重要的稀土金属,湖南是锑的主要产地之一。下列关于锑的说法正确的是( )
A.相对原子质量为51
B.元素符号为Sb
C.原子的核外电子数为121.8
D.该元素为非金属元素
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】解:A、根据元素周期表中的一格可知,左上角的数字为51,表示原子序数为51,不是相对原子质量,故选项说法错误;
B、根据元素周期表中的一格可知,字母表示该元素的元素符号,该元素的元素符号是Sb,故选项说法正确。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为121.8,不是原子的核外电子数,故选项说法错误;
D、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锑,属于金属元素,故选项说法错误。
故选:B。
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力。
9.(3分)下列有关实验现象的描述,错误的是( )
A.木炭在氧气中燃烧,生成无色气体
B.硫在氧气中燃烧,发出淡蓝色火焰
C.红磷在空气中燃烧,产生大量白烟
D.铁丝在氧气中燃烧,火星四射,生成黑色固体
【分析】A、根据木炭在氧气中燃烧的现象进行分析判断。
B、根据硫在氧气中燃烧的现象进行分析判断。
C、根据红磷在空气中燃烧的现象进行分析判断。
D、根据铁丝在氧气中燃烧的现象进行分析判断。
【解答】解:A、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的无色气体,故选项说法正确。
B、硫在氧气中燃烧,发出明亮的蓝紫色火焰,产生一种具有刺激性气味的气体,故选项说法错误。
C、红磷在空气中燃烧,产生大量的白烟,故选项说法正确。
D、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
故选:B。
【点评】本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别。
10.(3分)空气是一种宝贵的自然资源。下列有关空气的说法正确的是( )
A.氮气约占空气体积的21%
B.氧气能助燃,可以作燃料
C.稀有气体化学性质不活泼,不与任何物质发生反应
D.空气中二氧化碳含量过高会加剧温室效应
【分析】A、氮气约占空气体积的78%;B、氧气能助燃,不具有可燃性,不能作燃料;C、稀有气体化学性质不活泼,不易与任何物质发生反应;D、空气中二氧化碳含量过高会加剧温室效应,导致温室效应的主要气体是二氧化碳。
【解答】解:A、氮气约占空气体积的78%,故A错;
B、氧气能助燃,不具有可燃性,不能作燃料,故B错;
C、稀有气体化学性质不活泼,不易与任何物质发生反应,故C错;
D、空气中二氧化碳含量过高会加剧温室效应,导致温室效应的主要气体是二氧化碳,D正确。
故选:D。
【点评】解答本题关键是熟悉空气组成,及其性质和用途。
11.(3分)如图是两种粒子结构示意图,从图中获得的信息不正确的是( )
A.①和②的核外电子层数不同
B.②易得到6个电子形成稳定结构
C.②表示原子
D.①表示阴离子
【分析】根据原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层,根据质子数与电子数的关系分析是原子还是离子;据此进行分析解答即可。
【解答】解:A.由粒子结构示意图可知,①和②的核外电子层数不同,故正确;
B、②的最外层电子数数2,小于4,易失去2个电子形成稳定结构,故不正确;
C.在②中质子数等于电子数,表示原子,故正确;
D.在①中质子数=8<电子数=10,表示阴离子,故正确;
故选:B。
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、原子结构示意图的含义是正确解答本题的关键。
12.(3分)习近平总书记视察岳阳时,殷殷嘱托“守好一江碧水。”作为岳阳的主人,你认为下列做法正确的是( )
A.工业废水随意排放
B.生活垃圾直接扔入江河
C.挖砂船常年日夜不停采砂
D.生活污水实现集中处理和排放
【分析】根据常见的水体污染的原因、防治措施进行分析判断。
【解答】解:A、工业废水随意排放,会造成水体污染,故选项错误。
B、生活垃圾直接扔入江河,会造成水体污染,故选项错误。
C、挖砂船常年日夜不停采砂,会破坏河道、污染水体,故选项错误。
D、生活污水实现集中处理和排放,有利于防治水体污染,故选项正确。
故选:D。
【点评】本题难度不大,了解常见的水体污染的原因、防治措施是正确解答本题的关键。
13.(3分)下列图象中有关量的变化趋势正确的是( )
A.向一定浓度的NaOH溶液中加水稀释
B.向一定浓度的H2SO4溶液中加水稀释
C.向一定质量的锌粒中加入稀盐酸
D.向接近饱和的KNO3溶液中加入KNO3晶体
【分析】A.根据碱溶液稀释后仍然是碱溶液分析;
B.根据酸溶液稀释后仍然是酸溶液进行分析;
C.根据锌和稀盐酸反应生成氢气进行分析;
D.根据接近饱和的KNO3溶液中加入KNO3晶体变成饱和溶液后不再继续溶解硝酸钾进行分析。
【解答】解:A.向一定浓度的NaOH溶液中加水稀释,随着水的加入,溶液的pH可以无限的接近7,但不会等于7,更不会小于7,故A错误;
B.向一定浓度的H2SO4溶液中加水稀释,随着水的加入,溶液的pH可以无限的接近7,但不会等于7,更不会大于7,故B错误;
C.一定质量的锌粒中加入稀硫酸,当反应停止时,氢气的质量不变,故C正确;
D.向接近饱和的KNO3溶液中加入KNO3晶体,当溶液达到饱和时,就不在溶解KNO3晶体,溶液的质量就会保持不变,故D错误。
故选:C。
【点评】此题是对化学反应及图象的考查,解题的重点是能正确的分析变化的过程,读懂图象并与反应相结合是解题的关键所在。
14.(3分)下列实验操作或方法能达到实验目的是( )
选项
实验目的
实验操作或方法
A
鉴别稀硫酸和氯化钠溶液
滴加酚酞溶液
B
从粗盐中得到纯净的氯化钠
溶解、过滤、洗涤、干燥
C
鉴别K2SO4、Cu(NO3)2、Ba(OH)2、NaOH
不另加试剂
D
除去CO2中含有的少量CO
点燃
A.A B.B C.C D.D
【分析】显碱性溶液能使酚酞试液变红色,显中性溶液和显酸性溶液都不能使酚酞试液变色;
氯化钠易溶于水,泥沙不溶于水;
硝酸铜溶液是蓝色溶液,和氢氧化钠反应生成蓝色沉淀氢氧化铜和硝酸钠,和氢氧化钡反应生成蓝色沉淀氢氧化铜和硝酸钡;
二氧化碳不能燃烧,不支持燃烧。
【解答】解:A、滴加酚酞试液,都无明显现象,不能区分稀盐酸和氯化钠溶液,该选项不能达到实验目的;
B、溶解、过滤、洗涤、干燥不能得到纯净的氯化钠,该选项不能达到实验目的;
C、蓝色溶液是硝酸铜溶液,把硝酸铜溶液分别滴加到其它溶液中,产生蓝色沉淀的是氢氧化钠或氢氧化钡,不产生沉淀的是硫酸钾,把硫酸钾滴加到氢氧化钠或氢氧化钡中,产生白色沉淀的是氢氧化钡,另一种是氢氧化钠,该选项能够达到实验目的;
D、二氧化碳中的一氧化碳不能被点燃,该选项不能达到实验目的。
故选:C。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
15.(3分)向AgNO3和Cu(NO3)2的混合液中加入一定量的Fe、Cu的混合粉末,充分反应后过滤、洗涤,得到滤液和滤渣。下列说法正确的是( )
A.滤渣中一定有Ag,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3
B.当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Fe
C.向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag
D.向滤液中加入KCl溶液,无明显现象,则滤液中一定有 Fe(NO3)2、Cu(NO3)2,滤渣中可能有Fe、Cu
【分析】铁比铜活泼,铜比银活泼,向AgNO3和 Cu(NO3)2混合溶液中加入一定量的Fe和Cu的混合粉末时,铁先和硝酸银、硝酸铜反应,最后是铜和硝酸银反应。
【解答】解:A、滤渣中一定有铁和硝酸银反应生成的Ag,如果Fe、Cu的混合粉末很少,硝酸银有剩余,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3,该选项说法正确;
B、当滤液为蓝色时,滤渣中一定有Ag,不一定有Cu,这是因为滤液为蓝色时,溶液中含有铜离子,则硝酸铜可能部分反应,也可能没有反应,也可能是铜和硝酸银反应生成了硝酸铜,该选项说法不正确;
C、向滤渣中加入盐酸,有气泡产生,则铁一定过量,则滤渣中一定有Fe、Cu、Ag,该选项说法正确;
D、向滤液中加入KCl溶液,无明显现象,说明硝酸银完全反应,则滤液中一定有Fe(NO3)2,可能有Cu(NO3)2,滤渣中一定有Ag,可能有Fe、Cu,该选项说法不正确。
故选:AC。
【点评】要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来。
二、填空与简答题(本题共5道小题,每空2分,共32分)
16.(4分)用正确的化学符号填空:
(1)氮分子 N2 ;
(2)氧化铁 Fe2O3 。
【分析】(1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字。
(2)氧化铁中铁元素显+3价,氧元素显﹣2价,写出其化学式即可。
【解答】解:(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则氮分子可表示为:N2。
(2)氧化铁中铁元素显+3价,氧元素显﹣2价,其化学式为:Fe2O3。
故答案为:
(1)N2;
(2)Fe2O3。
【点评】本题难度不大,掌握常见化学用语(分子符号、化学式等)的书写方法是正确解答此类题的关键。
17.(6分)现有下列物质①大理石②稀硫酸③干冰④碳酸氢钠⑤氦气,请选择合适物质的序号填空:
(1)常用于人工降雨的是 ③ ;
(2)常用于焙制糕点的是 ④ ;
(3)常用于建筑材料的是 ① 。
【分析】(1)根据干冰的用途进行分析;
(2)根据碳酸氢钠的用途进行分析;
(3)根据大理石的用途进行分析。
【解答】解:(1)干冰升华会吸收大量的热,可用于人工降雨;
(2)碳酸氢钠受热易分解生成碳酸钠、水和二氧化碳,常用于焙制糕点;
(3)大理石是名贵的建筑材料。
故答案为:
(1)③;
(2)④;
(3)①。
【点评】本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键。
18.(6分)A、B、C三种晶体(不含结晶水)的溶解度曲线如图,请回答:
(1)P点的含义是 在t1℃时,B、C的溶解度相等 ;
(2)t2℃时,将30gA物质加入50g水中可以得到 75 g溶液;
(3)欲将适量B物质的不饱和溶液变成饱和溶液,可采用的方法是 加入溶质或蒸发溶剂或降低温度 (任答一种即可)。
【分析】根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;(1)P点的含义是:在t1℃时,B、C的溶解度相等;
(2)有关的计算要准确;
(3)欲将适量B物质的不饱和溶液变成饱和溶液,可采用的方法是:加入溶质、蒸发溶剂、降低温度。
【解答】解:(1)P点的含义是:在t1℃时,B、C的溶解度相等;故答案为:在t1℃时,B、C的溶解度相等;
(2)t2℃时,将30gA物质加入50g水中可以得到溶液的质量=25g+50g=75g;故答案为:75;
(3)欲将适量B物质的不饱和溶液变成饱和溶液,可采用的方法是:加入溶质、蒸发溶剂、降低温度;故答案为:加入溶质或蒸发溶剂或降低温度;
【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关饱和溶液与不饱和溶液的转化、溶液的计算等,有关的计算要准确,本考点主要出现在选择题和填空题中。
19.(10分)能源、材料、健康和安全关系着社会的发展。请回答:
(1)煤、石油、天然气属于 不可再生 能源(填“可再生”或“不可再生”);
(2)岳阳三荷机场航站楼采用了钢结构和索膜结构的施工技术。索膜结构膜面材料的主要成分是聚四氟乙烯,俗称“塑料王”。聚四氟乙烯属于 有机合成 材料(填“金属”或“有机合成”);
(3)华为开创了“中国芯”时代。“中国芯”的主要材料是高纯度的单质硅,工业上可用SiO2
和碳单质在高温条件下反应来制取,反应同时生成一种可燃性气体。请写出该反应的化学方程式 SiO2+2CSi+2CO↑ ;
(4)安全是一个永恒的话题,下列做法错误的是 A (填序号);
A.燃气泄漏,用打火机检验 B.电器着火,先关闭电源
C.点燃氢气前先检验纯度 D.不食用发霉的蛋糕
(5)小丽设计了一份中考期间的食谱:米饭、红烧肉、清蒸鱼、牛奶,你认为还应该增加的食物是 C (填序号)。
A.牛肉 B.鸡肉 C.蔬菜
【分析】(1)根据煤、石油和天然气属于不可再生能源进行解答;
(2)根据聚四氟乙烯是索膜结构膜面材料,属于塑料分析;
(3)根据化学反应的原理结合生成可燃性气体分析;
(4)A、根据燃气泄漏的正确处理方法分析;
B、根据电器着火的正确处理方法分析;
C、根据点燃可燃性气体前要检验纯度,防止爆炸分析;
D、根据发霉的食物会产生致癌的黄曲霉素分析;
(5)根据合理膳食营养均衡分析。
【解答】解:(1)煤、石油和天然气属于不可再生能源,故填:不可再生;
(2)聚四氟乙烯是索膜结构膜面材料,属于塑料,属于有机合成材料,故填:有机合成;
(3)SiO2和碳单质反应制取单质硅,根据质量守恒定律,反应后的可燃性气体又碳元素和氧元素组成,故应为一氧化碳,反应的化学方程式为SiO2+2CSi+2CO↑;故填:SiO2+2CSi+2CO↑;
(4)A、燃气泄漏时应先关闭泄漏阀门,开窗通风,用打火机检验易引起爆炸,故A错误;
B、电器着火应先切断电源,故B正确;
C、点燃可燃性气体前要检验纯度,防止爆炸,故C正确;
D、发霉的食物会产生致癌的黄曲霉素,不能食用,故D正确;
故选:A;
(5)米饭中富含糖类,红烧肉、清蒸鱼富含蛋白质油脂,牛奶中富含蛋白质以及无机盐钙元素,食谱中缺乏维生素,蔬菜和水果中富含维生素,故应增加的食物是蔬菜,故选:C。
【点评】能源、材料、健康和安全关系着社会的发展,是中考的热点之一,根据已有知识解题即可。
20.(6分)A、B、C、D、E、F是初中化学常见的物质,按单质、氧化物、酸、碱、盐分类,它们分别属于其中的四类物质。它们相互转化的关系如图所示(部分生成物和反应条件已省略)。已知:A物质由三种元素组成,其中两种元素的质量比为1:2;F为一种红色固体:D、F属同一类物质,C、E属同一类物质。请回答:
(1)C与D反应的基本类型为 置换反应 ;
(2)A的化学式为 H2SO4 ;
(3)A与B反应的化学方程式为 CuO+H2SO4=CuSO4+H2O 。
【分析】根据A、B、C、D、E、F是初中化学常见的物质,按单质、氧化物、酸、碱、盐分类,它们分别属于其中的四类物质,A物质由三种元素组成,其中两种元素的质量比为1:2,F为一种红色固体,所以F是铜,D、F属同一类物质,C、E属同一类物质,D和C反应生成铜,所以C是铜的盐溶液,A和B反应会生成C,所以A是硫酸,B是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,所以C是硫酸铜,D可以是铁,铁和硫酸铜反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,所以E是硫酸亚铁,然后将推出的物质进行验证即可。
【解答】解:(1)A、B、C、D、E、F是初中化学常见的物质,按单质、氧化物、酸、碱、盐分类,它们分别属于其中的四类物质,A物质由三种元素组成,其中两种元素的质量比为1:2,F为一种红色固体,所以F是铜,D、F属同一类物质,C、E属同一类物质,D和C反应生成铜,所以C是铜的盐溶液,A和B反应会生成C,所以A是硫酸,B是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,所以C是硫酸铜,D可以是铁,铁和硫酸铜反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,所以E是硫酸亚铁,经过验证,推导正确,所以C与D的反应是铁和硫酸铜反应生成硫酸亚铁和铜,基本类型为:置换反应;
(2)A的化学式为H2SO4;
(3)A与B的反应是氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4=CuSO4+H2O。
故答案为:(1)置换反应;
(2)H2SO4;
(3)CuO+H2SO4=CuSO4+H2O。
【点评】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
三、实验与探究题(本题共2道小题,每小题8分,共16分)
21.(8分)实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
(1)实验室制取二氧化碳所选用的收集装置是 C ,反应的化学方程式是 CaCO3+2HCl═CaCl2+H2O+CO2↑ 。
(2)若用高锰酸钾制取氧气,并用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是 C (填字母)。
A.③④①②⑤
B.④③①②⑤
C.④③①⑤②
D.①②③④⑤
(3)若要除去氧气中混有的水蒸气,气体应从F装置的 a 端进入。
【分析】凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳能够溶于水,密度比空气大。
【解答】解:(1)二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
反应的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑。
故填:C;CaCO3+2HCl═CaCl2+H2O+CO2↑。
(2)正确的操作顺序:检查装置的气密性,加入药品并固定仪器,点燃酒精灯并收集气体,从水槽中撤出导管,熄灭酒精灯。
故填:C。
(3)若要除去氧气中混有的水蒸气,气体应从F装置的a端进入。
故填:a。
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。
22.(8分)某化学课堂正在进行,以下是教学片断。请你参与他们的学习并完成相关任务。
【演示实验】老师按如图所示连接好装置,加入NaHCO3粉末,点燃酒精灯,对试管预热后集中加热,烧杯中澄清石灰水变浑浊,说明生成了CO2.继续加热至无气体产生后撤出导管,熄灭酒精灯。
【问题提出】实验后,同学们对试管中剩余的固体粉末产生了兴趣:剩余粉末由什么物质组成?
【猜想假设】在老师的指导下,同学们对固体粉末作出了如下猜想:
猜想一:NaOH;猜想二:NaOH和Na2CO3;猜想三:Na2CO3。
【实验探究】
实验方案
实验操作
实验现象
方案一
取适量粉末溶于水后向溶液中滴入2滴酚酞溶液,摇匀
溶液由无色变红色
小明根据实验现象认为猜想一成立。小组讨论后,大家认为小明的结论不合理,理由是 碳酸钠溶液呈碱性,也能使无色酚酞试液变红色 。
实验方案
实验操作
实验现象
实验结论
方案二
步骤一
猜想一不成立
取适量粉末溶于水后加
入过量的BaCl2溶液
溶液变浑浊,有白色沉淀生成
步骤二
取步骤一的上层清液加入MgCl2溶液2﹣3mL
无明显现象
猜想三成立
【评价交流】小华认为步骤二也可以用MgSO4代替MgCl2,大家不同意他的观点,理由是 MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验 。
【拓展延伸】请你总结上述实验成果,写出碳酸氢钠受热分解的化学方程式 2NaHCO3Na2CO3+H2O+CO2↑ 。
【分析】【实验探究】
方案一:
根据碳酸钠溶液呈碱性进行分析
方案二:
步骤一:根据碳酸钠和氯化钡反应生成白色沉淀进行分析;
【评价交流】
根据MgSO4能和过量的BaCl2反应生成白色沉淀;
【拓展延伸】
根据反应物、生成物和反应条件书写化学方程式。
【解答】解:【实验探究】
方案一:
碳酸钠溶液呈碱性,也能使无色酚酞试液变红色,所以不能因为溶液能使无色酚酞试液变红色,就认为溶液是氢氧化钠溶液;
方案二:
步骤一:因为方案一不成立,所以溶液中含有碳酸钠,碳酸钠和氯化钡反应生成碳酸钡白色沉淀,故现象为:溶液变浑浊,有白色沉淀生成;
【评价交流】
不能用MgSO4代替MgCl2,因为MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验;
【拓展延伸】
根据以上实验可知碳酸氢钠受热反应生成氯化钠、水和二氧化碳,化学方程式为:2NaHCO3 Na2CO3+H2O+CO2↑。
故答案为:
【实验探究】
方案一:
碳酸钠溶液呈碱性,也能使无色酚酞试液变红色;
方案二
步骤一:溶液变浑浊,有白色沉淀生成;
【评价交流】
MgSO4能和过量的氯化钡反应生成白色沉淀,影响氢氧根离子的检验
【拓展延伸】
2NaHCO3 Na2CO3+H2O+CO2↑。
【点评】此题通过碳酸氢钠受热分解考查了化学方程式的书写,实验方案设计、实验操作以及实验方案的评价,解答时要全面审题,认真解答。
四、计算题(本题共2道小题,第46题2分,第47题5分,共7分)
23.(2分)葡萄中含有丰富的白藜芦醇(化学式(C14H12O3),它具有抗癌作用,能抑制癌细胞的增生。请计算:
(1)一个白藜芦醇分子由 29 个原子构成;
(2)白藜芦醇中氢元素和氧元素的质量比为 1:4 (填最简整数比)。
【分析】根据化学式的意义进行相关的计算,注意要结合题目要求以及使用正确的相对原子质量进行分析和解答。
【解答】解:
(1)一个白藜芦醇分子由14+12+3=29个原子构成;
(2)白藜芦醇中氢元素和氧元素的质量比为(1×12):(16×3)=1:4。
故答案为:
(1)29;
(2)1:4。
【点评】根据化学式计算首先要确保化学式本身正确,其次过程中使用相对原子质量要准确。
24.(5分)现有一含NaCl杂质的Na2CO3样品,取13.9g样品溶于水,配成104.4g溶液,此溶液与100g某浓度的盐酸恰好完全反应,得到200g溶液。请计算:
(1)生成的二氧化碳的质量为 4.4 g;
(2)所得溶液中NaCl的质量分数(写出计算步骤)。
【分析】(1)根据质量守恒定律分析;
(2)根据二氧化碳的质量和化学方程式计算氯化钠的质量,进一步计算所得溶液中NaCl的质量分数。
【解答】解:(1)由质量守恒定律可知,生成的二氧化碳的质量为104.4g+100g﹣200g=4.4g;故填4.4;
(2)设碳酸钠的质量为y,生成氯化钠的质量为x
NaCO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
x=10.6g,y=11.7g
所得溶液中NaCl的质量分数为×100%=7.5%
答:所得溶液中NaCl的质量分数为7.5%。
【点评】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2019/6/27 16:16:19;用户:初中校园号;邮箱:wjwl@xyh.com;学号:24424282
相关文档
- 2020年四川省乐山市中考化学试卷【2021-11-065页
- 湖北省随州市2020年中考化学试卷(解2021-11-0612页
- 2019年台湾省中考化学试卷2021-11-0611页
- 【2020年中考化学,含答案,word版,可再2021-11-069页
- 浙江省宁波市2012年中考化学试卷(含2021-11-069页
- 2020年湖南省株洲市中考化学试卷【2021-11-068页
- 2020年湖北省孝感市中考化学试卷【2021-11-065页
- 2020年湖南省永州市中考化学试卷【2021-11-064页
- 2020年甘肃省陇南市中考化学试卷【2021-11-066页
- 河北省中考化学试卷2021-05-133页