- 163.00 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
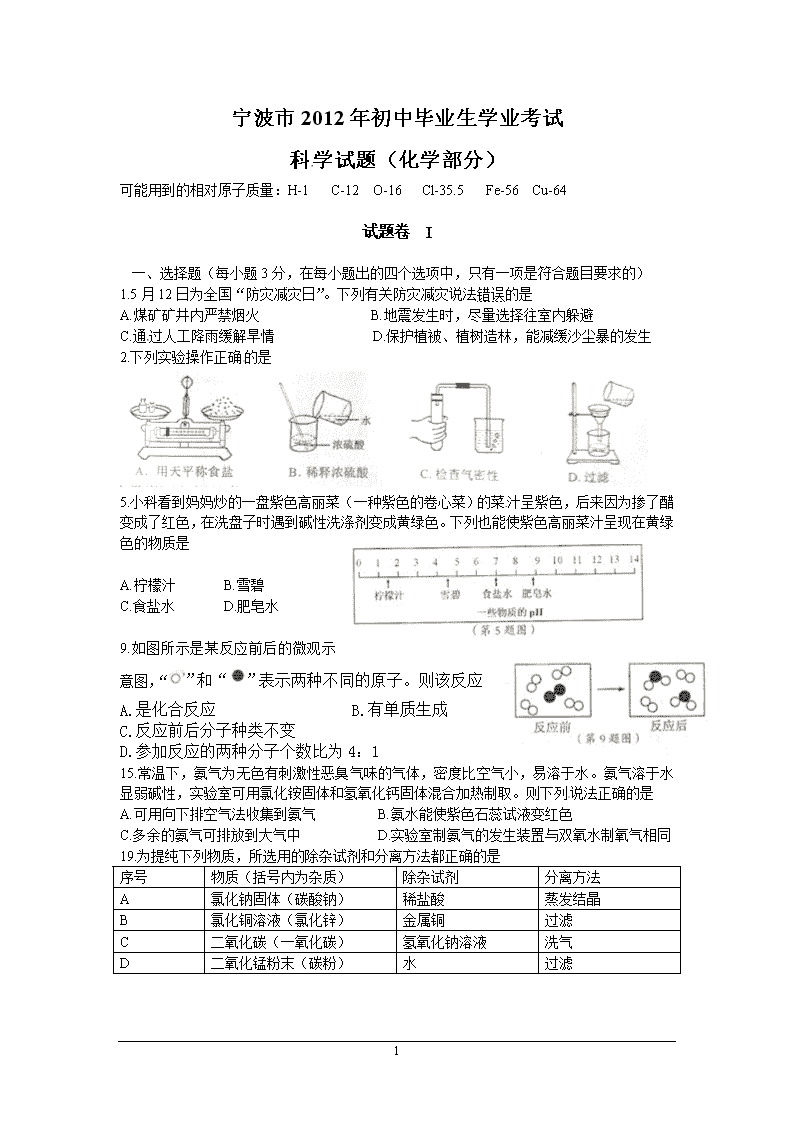
宁波市2012年初中毕业生学业考试
科学试题(化学部分)
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Fe-56 Cu-64
试题卷 I
一、选择题(每小题3分,在每小题出的四个选项中,只有一项是符合题目要求的)
1.5月12日为全国“防灾减灾日”。下列有关防灾减灾说法错误的是
A.煤矿矿井内严禁烟火 B.地震发生时,尽量选择往室内躲避
C.通过人工降雨缓解旱情 D.保护植被、植树造林,能减缓沙尘暴的发生
2.下列实验操作正确的是
5.小科看到妈妈炒的一盘紫色高丽菜(一种紫色的卷心菜)的菜汁呈紫色,后来因为掺了醋变成了红色,在洗盘子时遇到碱性洗涤剂变成黄绿色。下列也能使紫色高丽菜汁呈现在黄绿色的物质是
A.柠檬汁 B.雪碧
C.食盐水 D.肥皂水
9.如图所示是某反应前后的微观示意图,“”和“”表示两种不同的原子。则该反应
A.是化合反应 B.有单质生成
C.反应前后分子种类不变
D.参加反应的两种分子个数比为4:1
15.常温下,氨气为无色有刺激性恶臭气味的气体,密度比空气小,易溶于水。氨气溶于水显弱碱性,实验室可用氯化铵固体和氢氧化钙固体混合加热制取。则下列说法正确的是
A.可用向下排空气法收集到氨气 B.氨水能使紫色石蕊试液变红色
C.多余的氨气可排放到大气中 D.实验室制氨气的发生装置与双氧水制氧气相同
19.为提纯下列物质,所选用的除杂试剂和分离方法都正确的是
序号
物质(括号内为杂质)
除杂试剂
分离方法
A
氯化钠固体(碳酸钠)
稀盐酸
蒸发结晶
B
氯化铜溶液(氯化锌)
金属铜
过滤
C
二氧化碳(一氧化碳)
氢氧化钠溶液
洗气
D
二氧化锰粉末(碳粉)
水
过滤
4
试题卷II
一、 简答题(每空2分)
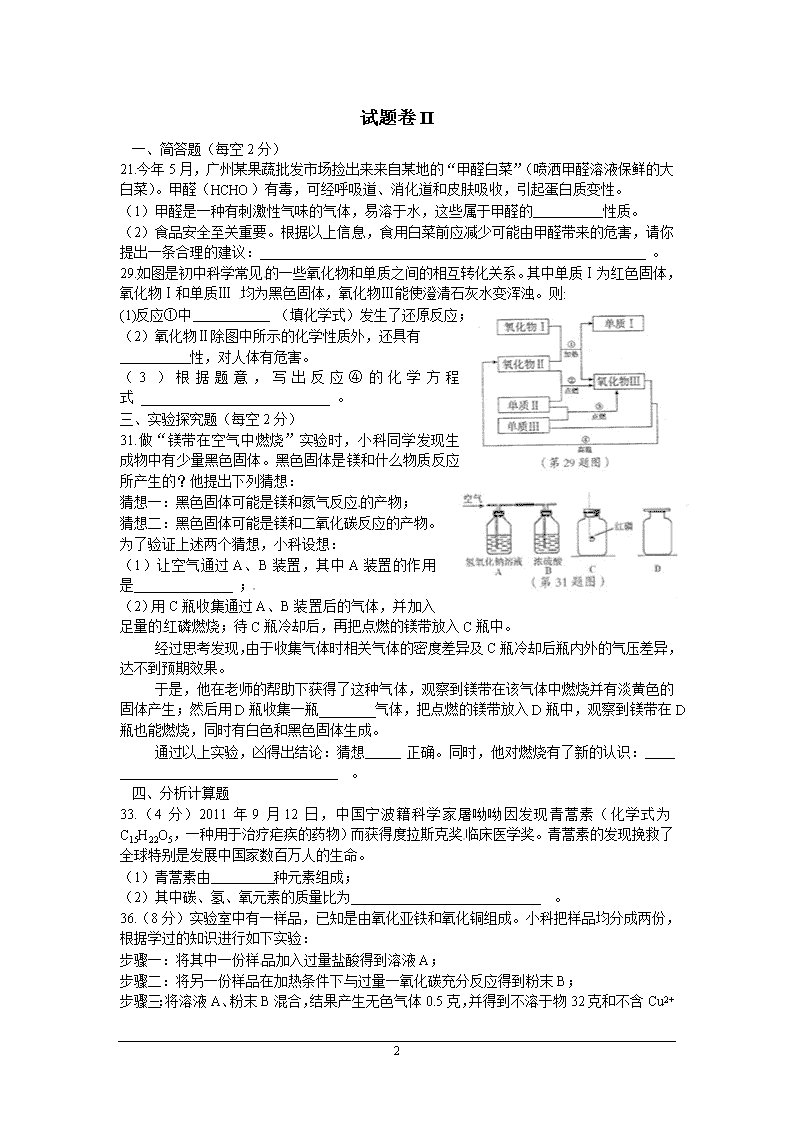
21.今年5月,广州某果蔬批发市场捡出来来自某地的“甲醛白菜”(喷洒甲醛溶液保鲜的大白菜)。甲醛(HCHO)有毒,可经呼吸道、消化道和皮肤吸收,引起蛋白质变性。
(1)甲醛是一种有刺激性气味的气体,易溶于水,这些属于甲醛的 性质。
(2)食品安全至关重要。根据以上信息,食用白菜前应减少可能由甲醛带来的危害,请你提出一条合理的建议: 。
29.如图是初中科学常见的一些氧化物和单质之间的相互转化关系。其中单质Ⅰ为红色固体,氧化物Ⅰ和单质Ⅲ 均为黑色固体,氧化物Ⅲ能使澄清石灰水变浑浊。则:
(1)反应①中 (填化学式)发生了还原反应;
(2)氧化物Ⅱ除图中所示的化学性质外,还具有
性,对人体有危害。
(3)根据题意,写出反应④的化学方程式 。
三、实验探究题(每空2分)
31.做“镁带在空气中燃烧”实验时,小科同学发现生成物中有少量黑色固体。黑色固体是镁和什么物质反应所产生的?他提出下列猜想:
猜想一:黑色固体可能是镁和氮气反应的产物;
猜想二:黑色固体可能是镁和二氧化碳反应的产物。
为了验证上述两个猜想,小科设想:
(1)让空气通过A、B装置,其中A装置的作用是 ;
(2)用C瓶收集通过A、B装置后的气体,并加入足量的红磷燃烧;待C瓶冷却后,再把点燃的镁带放入C瓶中。
经过思考发现,由于收集气体时相关气体的密度差异及C瓶冷却后瓶内外的气压差异,达不到预期效果。
于是,他在老师的帮助下获得了这种气体,观察到镁带在该气体中燃烧并有淡黄色的固体产生;然后用D瓶收集一瓶 气体,把点燃的镁带放入D瓶中,观察到镁带在D瓶也能燃烧,同时有白色和黑色固体生成。
通过以上实验,凶得出结论:猜想 正确。同时,他对燃烧有了新的认识:
。
四、 分析计算题
33.(4分)2011年9月12日,中国宁波籍科学家屠呦呦因发现青蒿素(化学式为C15H22O5,一种用于治疗疟疾的药物)而获得度拉斯克奖临床医学奖。青蒿素的发现挽救了全球特别是发展中国家数百万人的生命。
(1)青蒿素由 种元素组成;
(2)其中碳、氢、氧元素的质量比为 。
36.(8分)实验室中有一样品,已知是由氧化亚铁和氧化铜组成。小科把样品均分成两份,根据学过的知识进行如下实验:
步骤一:将其中一份样品加入过量盐酸得到溶液A;
步骤二:将另一份样品在加热条件下与过量一氧化碳充分反应得到粉末B;
步骤三:将溶液A、粉末B混合,结果产生无色气体0.5克,并得到不溶于物32克和不含Cu2+
4
的强酸性溶液。
(1)溶液A的溶质中,除生成的氯化亚铁和氯化铜外,还含有 ;
(2)计算原样品中氧化铜的质量;
(3)计算粉末B中铁的质量;
(4)原样品中氧化亚铁和氧化铜的质量比为多少?
4
宁波市2012年初中毕业生学业考试
科学试题(化学部分)参考答案及评分标准
一、选择题:
1.B 2.C 5.D 9.A 15.A 19.A
二、简答题(每空2分)
21.(1)物理 (2)用水多次冲洗(合理的给分)
29.(1)CuO (2)毒 (3)CO2+C 2CO
三、实验探究题(每空2分)
31.(1)除去空气中的二氧化碳 (2)二氧化碳 二 燃烧不一定需要氧气(合理的给分
四、分析计算题(每空2分)
33.(1) (2)90:11:40
36.(1)HCl (2分)
(2)解:32g÷Cu/CuO (1分)
=32g÷64/80×100%=40g (1分)
答:原样品中氧化铜的质量为40g。
(3)解:设与盐酸反应的铁粉的质量为x,与氯化铜反应的铁粉的质量为y
32g÷2=16g
Fe + 2HCl = FeCl2 + H2↑ Fe +CuCl2 = FeCl2 + Cu
56 2 56 64
x 0.5g y 16g
56:2 = x:0.5g 56:64 = y :16g y = 14g
x = 14g (1分) 14g +14g = 28 g (1分)
答:粉末B中铁粉的质量为28g。
(4)28×2÷Fe/FeO×100% (1分)
=56÷56/72×100%=72g 72g/40g=9/5 (1分)
答:原样品中氧化亚铁和氧化亚铜的质量比为9:5。
4
相关文档
- 2019年中考化学试题分类:考点17 科2021-11-101页
- 呼和浩特专版2020中考化学复习方案2021-11-1021页
- 2019年全国各地中考化学试题-贵州2021-11-104页
- 中考化学一轮专题复习:基本概念与原2021-11-104页
- 中考化学一轮专题复习:化学元素 12021-11-102页
- 2019年中考化学试题分类:考点11 水 2021-11-103页
- 2012中考化学复习精品 离子2021-11-105页
- 2019年湖南省郴州市中考化学试卷(解2021-11-1018页
- 2020年云南省红河州建水县中考化学2021-11-1030页
- 2019年全国各地中考化学试题-安徽(2021-11-105页