- 77.50 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课题2 离子
★ 教学目标
1.知识与技能:
(1)、初步了解原子核外的电子是分层排布的;
(2)、了解原子结构的表示方法;
(3)、了解原子结构与元素化学性质的关系;
(4)、了解离子的形成过程,认识离子是构成物质的一种粒子。
2.过程与方法:
(1)、通过学生间相互讨论、交流,增强学生归纳知识、获取知识的能力;
(2)、运用多媒体动画片、课文插图等辅助手段,演示离子的形成过程,化抽象为直观,增强学习的效果。
3.情感、态度与价值观:
(1)、初步体会物质构成的奥秘,培养学生的抽象思维能力、想象力和分析推理能力;
(2)、树立“结构决定性质”、“物质的微粒性”等辩证唯物主义观点。
★ 教学资源分析
在第三单元的学习中,学生已经知道许多物质是由原子、分子构成的,在本单元中介绍离子是构成物质的另一种粒子,使学生所学有关物质构成的知识完整化。
本课题包括“核外电子的排布”和“离子的形成”两部分内容,“离子的形成”是本课题的核心,“核外电子的排布”(介绍原子核外电子的分层排布和金属、非金属、稀有气体元素的原子核外电子层结构的特征与其化学性质的关系)为它的教学作了一个铺垫。
★ 教学策略分析
本课题的内容较抽象,远离学生的生活经验,学生学习时有一定的困难,是教学的难点。教学中,要充分利用书上的插图和电教手段,为学生创设学习氛围,让学生仔细观察、细心体会,展开讨论,将抽象知识形象化、具体化。
★ 教学重、难点
重点:离子的形成。
难点:核外电子排布的概念。
★ 教学准备
1.自制的有关投影片、离子形成的动画片、复印的课文插图;
2.网上下载的原子结构示意图。
★ 课时建议
1课时
★ 教学过程
教学流程
教师活动
学生活动
设计意图
创
设
情
境
富有感情地朗读学生作品——科普小论文《漫游原子世界》,要求学生根据小论文的内容在草稿纸上画出原子的构成。(内容见
“资料链接”。)
评价学生所画内容。
欣赏作品;
发挥想象力、画图。
(两个同学在黑板上
画。)
创设问题情境,从巩固已有的知识切入,形成和
谐、活跃的课堂气氛。
教学流程
教师活动
学生活动
设计意图
5
导
入
新
课
(提问式讲解)
同学们,你们知道氢、碳、氧、钠、硫等原子核外各有几个电子吗?
(可提示学生参考教材P68
表4—2。)
原子核对这些电子的吸引力是否相同?这些电子的排布有没有
规律可寻呢?
(板书)
一、核外电子的排布
猜测;
查阅资料;
回答。
充分利用教材资源,激发学生的好奇心。
导入课题。
阅
读
小
结
创
意
绘
画
引
出
问
题
学
得
新
知
指导学生阅读教材P76有关内容后提问:核外电子是怎样排布的?
用两个字概括。
阅读课本;
讨论、交流;
寻找最佳词语。
培养学生的阅读、总结、概括能力。
(过渡)那么,电子究竟是怎样
分层排布的呢?
思考、猜想;查书。
自然过渡;层层深入。
请同学们利用教材P68表4—2的数据,进行创意绘画:(1)氢原子结构图。(2)氧原子结构
图。
自由创意画图:各种氢原子结构创意图很快画好;画氧原子结构创意图时遇到问题:含有8个电子的氧原子中,这8个电子究竟怎样绕核外高速运动呢?
画画是学生感兴趣的活动,再加上又是抽象画,
学生非常兴奋;培养学生的创造性思维能力。
请同学们打开书本,看教材P76图4—9,介绍电子层概念。
(投影)
氢原子结构示意图和氧原子结构示意图。介绍原子结构示意图
及各部分表示的意义。
知道电子是分层运动
的。
回忆原子结构,初步了解原子结构的表示方法及各部分表示的意义。
从问题着手,引出新知。
注意知识的前后连贯。
议
论
交
流
(投影)
核电荷数从1—18的各元素的原子结构示意图。
仔细观察:不同原子的核外电子排布有无一定规律?
分组讨论后交流。
教学流程
教师活动
学生活动
设计意图
5
归
纳
小
结
形
成
结
论
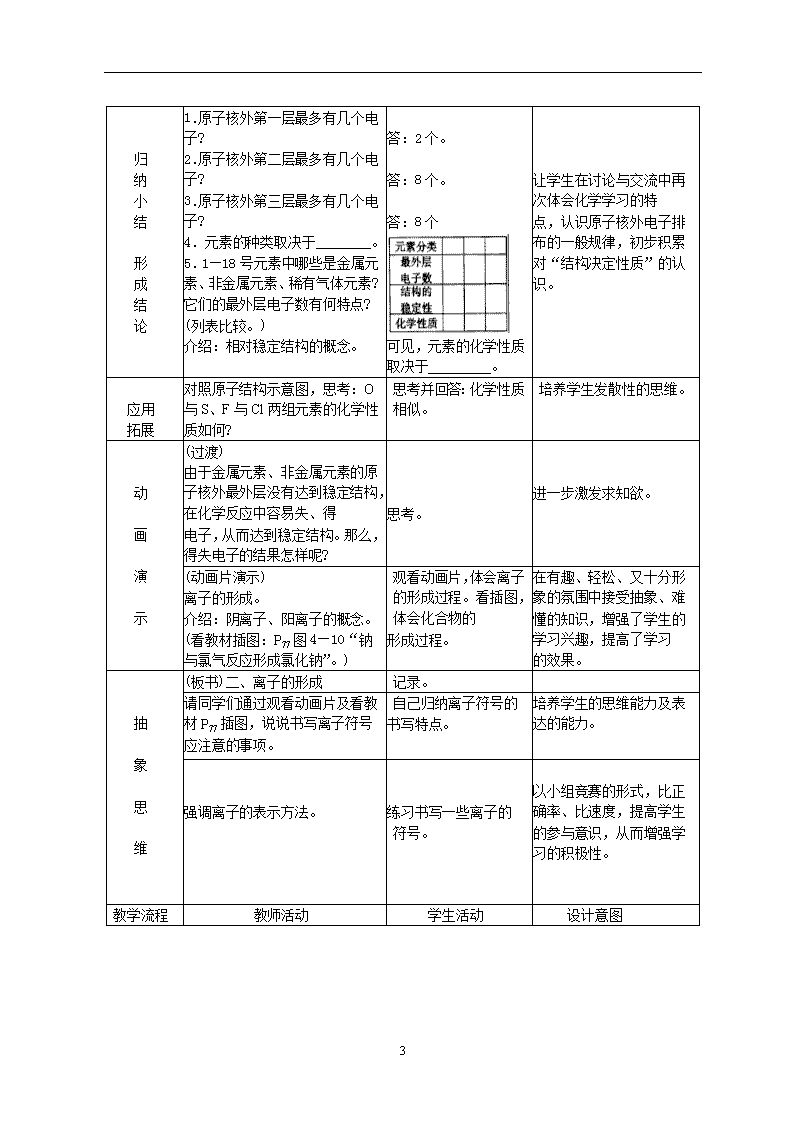
1.原子核外第一层最多有几个电子?
2.原子核外第二层最多有几个电子?
3.原子核外第三层最多有几个电子?
4.元素的种类取决于________。
5.1—18号元素中哪些是金属元素、非金属元素、稀有气体元素?它们的最外层电子数有何特点?
(列表比较。)
介绍:相对稳定结构的概念。
答:2个。
答:8个。
答:8个
可见,元素的化学性质取决于_________。
让学生在讨论与交流中再次体会化学学习的特
点,认识原子核外电子排布的一般规律,初步积累对“结构决定性质”的认识。
应用
拓展
对照原子结构示意图,思考:O与S、F与Cl两组元素的化学性质如何?
思考并回答:化学性质相似。
培养学生发散性的思维。
动
画
演
示
(过渡)
由于金属元素、非金属元素的原子核外最外层没有达到稳定结构,在化学反应中容易失、得
电子,从而达到稳定结构。那么,得失电子的结果怎样呢?
思考。
进一步激发求知欲。
(动画片演示)
离子的形成。
介绍:阴离子、阳离子的概念。
(看教材插图:P77图4—10“钠与氯气反应形成氯化钠”。)
观看动画片,体会离子的形成过程。看插图,体会化合物的
形成过程。
在有趣、轻松、又十分形象的氛围中接受抽象、难
懂的知识,增强了学生的学习兴趣,提高了学习
的效果。
抽
象
思
维
(板书)二、离子的形成
记录。
请同学们通过观看动画片及看教材P77插图,说说书写离子符号
应注意的事项。
自己归纳离子符号的
书写特点。
培养学生的思维能力及表达的能力。
强调离子的表示方法。
练习书写一些离子的
符号。
以小组竞赛的形式,比正确率、比速度,提高学生
的参与意识,从而增强学习的积极性。
教学流程
教师活动
学生活动
设计意图
5
对
比
分
析
理
解
概
念
(投影)
原子、离子的比较。
分组讨论;
代表发言。
在讨论中培养学生的合作意识,训练分析、归纳、
表达的能力。
学 练
以 习
致 巩
用 固
小结:构成物质的粒子有哪几种?举例说明。
师生共同填表:
氧气由_____构成;水由_____构成;二氧化
碳由______构成;铁由______构成;硅由____构成;氢气由____构成;氯化钠由
__________构成。
进一步确立物质的微观概念。
小 完
结 善
归 提
纳 高
请学生以图表的形式归纳出:元素、原子、分子、离子、单质、化合物之间的关系。
(投影)
物质与其构成粒子之间的关系。
尝试用图表表示。
学习用图表、化学用语归纳知识,培养学生的分析推理能力。
资料
漫游原子世界
我是一个小、小、小电子,在原子内部很大的空间中围绕着原子核这个小老头不停地转动;我们在飞,却怎么也飞不高。因为这老头长得很特别:虽然占据原子中央很小的地盘,却是由中子和质子构成,中子不带电,质子带正电,因此,这小老头也带正电,很有能耐,正好把我们身上的负电深深吸引,所以我们很难脱离原子核的怀抱。
★ 板书设计
课题2 离 子
一、核外电子的排布
1.排布规律:分层。
2.原子结构示意图:
5
3.决定元素的化学性质:最外层电子数。
二、离子的形成
1.定义:带电荷的原子。
2.形成过程:
三、小结
金属元素:最外层电子数一般小于4,易失去电子,形成带正电的阳离子;
非金属元素:最外层电子数一般大于4,易得到电子,形成带负电的阴离子;
稀有气体元素:最外层电子数一般等于8(氦为2),不易得到也不易失去电子;
相对稳定结构:最外层为8个电子(只有一个电子层的具有2个电子)的结构,如稀有气体。
★ 教后小记
___________________________________________ ________
___________________________________________ ________
___________________________________________ ________
5