- 954.05 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2021年初中学业水平考试人教版化学学科
阶段测试 (二)(第五—七单元)
(时间:90分钟 满分:100分)
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5
第I卷(选择题,45分)
一、选择题(本大题共20个小题,其中1~15小题,每小题2分,第16~20小题,每小题3分,共45分。每小题只有一个选项符合题意,多选、错选或不选均不得分)
1.学校防控新冠肺炎所用消毒液成分之一是次氯酸钠 ,以下反应可生成次氯酸钠, Cl2+2NaOH=== NaCl+X+H2O ,其中X的化学式为 ( A )
A.NaClO
B.Na2O
C.NaOH
D.NaClO3
2.下列叙述符合实际且化学方程式书写正确的是 ( B )
A.用氢氧化钠治疗胃酸过多:NaOH+HCl=== NaCl+H2O
B.碳酸钠溶液能使澄清的石灰水变浑浊:Na2CO3+Ca(OH)2=== 2NaOH+CaCO3↓
16
C.实验室用过氧化氢溶液与二氧化锰混合制取氧气:H2O2 H2↑+O2↑
D.高炉炼铁的反应原理:Fe2O3+3CO Fe+3CO2
3.下列位置或场所的标识,错误的是 ( B )
A.存放浓硫酸的试剂柜
B.运输酒精的槽罐车
C.面粉加工厂
D.居民住宅区
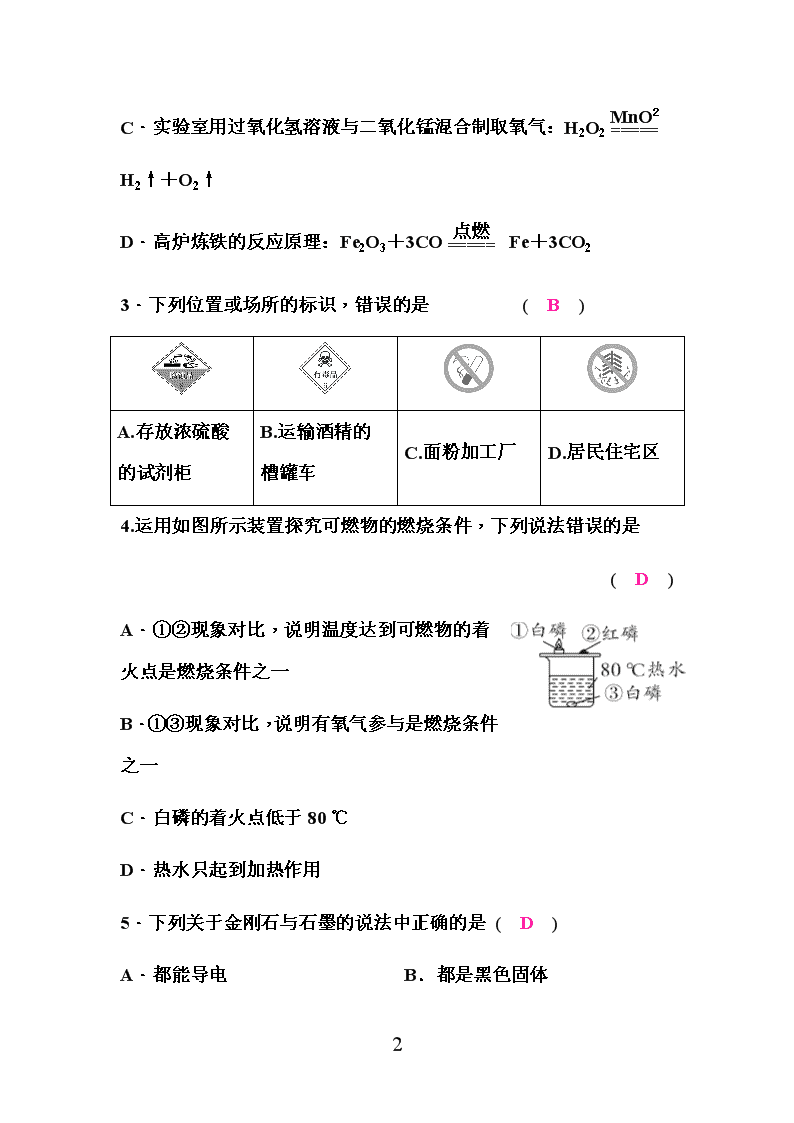
4.运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是
( D )
A.①②现象对比,说明温度达到可燃物的着火点是燃烧条件之一
B.①③现象对比,说明有氧气参与是燃烧条件之一
C.白磷的着火点低于80 ℃
D.热水只起到加热作用
5.下列关于金刚石与石墨的说法中正确的是 ( D )
A.都能导电 B.都是黑色固体
16
C.硬度都很小 D.都由碳元素组成
6.大气中二氧化碳含量的增加会引起全球气候变暖。今年1月全球平均气温为 13.14 ℃,成为自1880年有气象记录以来最热的1月。下列关于二氧化碳的认识不正确的是 ( A )
A.结构:由原子直接构成 B.性质:能与水反应
C.类别:非金属氧化物 D.用途:做气体肥料
7.煤和燃油的燃烧是造成空气污染的重要原因,下列排放物能形成酸雨的是 ( A )
A.SO2、NO2 B.CO、CO2
C.烟尘 D.未充分燃烧的汽油
8.下列有关碳和碳的氧化物的说法错误的是 ( B )
A.CO和CO2的化学性质不同,是因为分子的构成不同
B.金刚石和石墨的物理性质不同,是因为碳原子的构成不同
C.清明上河图至今图案清晰可见,是因为常温下碳单质的化学性质稳定
D.CO2通入紫色石蕊溶液中,溶液变成红色的原因是CO2能和水反应生成酸
9.下列关于燃烧的解释或分析正确的是 ( D )
16
图① 图② 图③ 图④
A.图①中将煤球制成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B.图②中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C.图③中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D.由图④的现象可知,金属镁燃烧不能用二氧化碳灭火
10.下列有关可燃冰的叙述中正确的是( B )
A.可燃冰是一种纯净物
B.可燃冰在常温常压下不易长久保存
C.可燃冰的成功开发利用使“水变油”成为可能
D.可燃冰作为一种清洁能源对环境没有任何危害
11.下图是密闭体系中某反应的微观示意图,“”和“”分别表示两种不同元素的原子,下列说法错误的是
( C )
A.参加反应的化合物与单质分子个数比为2∶1
B.反应前后原子种类没有改变
16
C.反应后该密闭体系中没有单质存在
D.该反应是化合反应
12.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是 ( D )
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
13.甲、乙、丙、丁都是含碳的物质,它们有如下关系:①甲与丙在高温的条件下反应生成乙;②乙与氧气在点燃的条件下反应生成丙;③常温下丁能分解生成丙。则甲、乙、丙、丁分别是 ( B )
A.C、CO、CO2、CaCO3 B.C、CO、CO2、H2CO3
C.CO、C、CO2、CaCO3 D.CO2、C、CO、H2CO3
14.从化学的角度分析,下列做法正确的是 ( A )
A.发生火灾时,蹲下靠近地面迅速离开着火区域
B.天然气泄漏时,立即打开排气扇
16
C.电器着火时,立即用大量水泼灭
D.为了防止CO中毒,在火炉旁放一盆水
15.下列实验设计不能实现其对应实验目的的是 ( C )
A.验证质量 B.测定空气 C.探究分子 D.验证CO2能与氢
守恒定律 中氧气含量 在不断运动 氧化钠溶液发生反应
16.下列对某一主题的知识归纳,有错误的一组是 ( D )
A.物质鉴别
B.物质除杂
①用食醋鉴别食盐和纯碱
②用灼烧并闻气味鉴别羊毛纤维与合成纤维
①稀盐酸中混有硫酸,可以加适量氧化钡溶液后过滤
②木炭粉中混有铁粉可以用磁铁吸引
C.安全知识
D.化学与健康
①电器着火,切断电源,再用干粉灭火器灭火
②家用煤气泄漏,
①缺钙会导致佝偻病或骨质疏松
②缺维生素C会引起贫血
16
应先关闭阀门,同时打开门窗透气
17.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O=== Ca(OH)2。下列说法不正确的是 ( C )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥氯化氢气体
D.此反应可制备氢氧化钙
18.在一个密闭容器中放入P、Q、R、W四种物质,在一定条件 下发生化学反应,一段时间后, 测得有关数据如下表。则关于此反应的认识正确的是 ( D )
物质
P
Q
R
W
反应前的质量(g)
5
2
14
18
反应后的质量(g)
20
x
4
13
A.参加化学反应的P和W的质量比为3∶2
B.该反应用化学方程式表示为:3P+Q=== 2R+W
C.反应后容器中R与Q的质量比为1∶2
D.Q在反应中可能作催化剂
16
19.如图为CO还原CuO“微型”实验装置(夹持仪器等略)。已知HCOOH H2O+CO↑。下列说法错误的是 ( D )
A.实验中所需CO可现制现用
B.此装置可节约用品,污染小,现象明显
C.此装置内空间较小,空气易排空,实验危险系数小
D.澄清石灰水是检验CO的还原产物
20.下列说法合理的有 ( D )
①化合物一定由不同种元素组成
②除去二氧化碳气体中混有的少量一氧化碳气体, 可将气体通过灼热的氧化铜
③一定质量的某有机物在氧气中充分燃烧生成4.4 g CO2和1.8 g H2O,该有机物中碳、氢原子个数比为1∶2
④显碱性的溶液不一定是碱溶液,但碱溶液一定显碱性
⑤白色粉末A由Na2SO4、Na2CO3、 BaCl2、 NaCl中的三种混合而成。把A加入到适量水中后,可得到白色沉淀B和溶液C,则溶液C中一定存在的溶质是NaCl
16
A.2条 B.3条 C.4条 D.5条
第Ⅱ卷(非选择题,共55分)
二、填空与简答(本大题有5个小题,化学方程式每空2分,其余每空1分,共33分)
21.(6分)(1) 请填写符合要求的化学用语。
①铁元素:__Fe; ②2个铝原子:__2Al; ③2个氢分子:__2H2;
④氢氧根离子:__OH-; ⑤标出氧化铜中铜元素的化合价:__CO。
(2)“3Ca2+”中“2+”的含义是__每个钙离子带两个单位的正电荷。
22.(7分)(1)通过一年的化学学习,我们认识了许多物质。请从①一氧化碳;②活性炭;③尿素;④氢气,选取相应物质的序号填空(每种物质限选一次)。
①最清洁的燃料是__④;
②可用于冰箱除异味的是__②;
③可用作化肥的是__③;
④用于工业炼铁且有毒的气体是__①。
(2)化石燃料中天然气的主要成分是__甲烷(填名称), 目前正进行燃气灶改换为天然气灶的工程,其中进风口调大的目的是__
16
补充充足的空气(或氧气),__以使燃烧更充分。
(3)煤的气化是把煤变为清洁能源的重要环节之一,其中一个重要的反应是:C+X CO+H2 ,其中X的化学式是__H2O。
23.(7分)实验创新可以使现象更明显,操作更简便。Y型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y型管设计了如图三个实验进行探究活动,请回答下列问题。
图1 图2 图3
(1)据如图1所示实验,其设计的目的是__验证二氧化碳能与水反应。一段时间后,观察到Y型管右侧湿润的蓝色石蕊试纸变红,写出发生反应的化学方程式__CO2+H2O===__H2CO3。
(2)如图2所示实验中,一段时间后,缓慢倾斜Y型管,将右侧的稀硫酸部分倒入左侧,依据__右侧无明显现象,左侧产生大量气泡(填实验现象) ,可得出结论:Zn的金属活动性比Cu__强。
(3)如图3所示实验中,根据Y型管左右两侧现象对比,可得到的实验结论是__燃烧的条件之一是温度需要达到着火点。该实验中,Y型管顶端气球的主要作用是__防止红磷燃烧产生的五氧化二磷污染空气。
24.(8分)新能源页岩气,正在冲击传统能源体系。据报道,
16
我国页岩气储量排名世界第一,合理开采将有利于改善我国的能源结构,川南页岩气田分布在泸州等地。页岩气是藏身于地下3 000多米的页岩层裂缝中的天然气,在此高压环境中,还有部分溶解于裂缝中存在的少量石油里。目前,开采页岩气时从地表钻井到页岩层,向地下压入大量水和沙,使页岩气所在的地层产生缝隙,因压强降低,页岩气将从其藏匿处逸岀。这些水和沙将被抽回地面,形成返排液。回答下列问题:
(1)页岩气中主要成分的化学式是__CH4,溶解在石油中的页岩气逸出的原因__压强降低,气体溶解度随压强减小而减小。
(2)页岩气中还可能含有乙烷(C2H6),写出乙烷完全燃烧的化学方程式:__2C2H6+7O2__4CO2+6H2O。
(3)返排液是油、水溶液和沙组成的混合物。从返排液中分离出沙的实验操作名称是__过滤;下表是某返排液中水溶液的主要成分及其含量,质量分数最高的金属离子是__Ca2+,这些离子的含量远高于自然水。
离子
K+
Ca2+
Mg2+
HCO
Cl-
含量(mg/L)
310
491
129
470
26.1
(4)结合上文分析简答:开采时可能产生的主要环保问题是__水体污染(写一点),你的解决建议是__对返排液集中净化处理。
25.★(5分)A、B、C、D是初中化学常见的四种物质。
16
(1)若A、B、C、D为硫酸铜、稀盐酸、氧化铜、铁粉中的某一种,其关系如右图所示,图中“→”表示转化关系,“—”表示相互能反应(部分反应物、生成物及反应条件已略去),B的水溶液为蓝色。则C的化学式为__HCl,A→B的化学方程式为__CuO+H2SO4 === CuSO4+H2O。
(2)若A为黑色固体单质,B是有刺激性气味的气体,且组成元素的质量比为1∶1,C是植物光合作用的主要原料,D是相对分子质量最小的氧化物。A在加热的条件下能与一种浓酸溶液反应生成B、C、D三种物质,该反应的化学方程式为
__C+2H2SO4__(浓)__2SO2↑+CO2↑+2H2O。
三、实验与探究(本大题共2个小题,化学方程式每空2分,其余每空1分,共16分)
26.(8分)请结合如图回答问题:(友情提示:二氧化碳不能溶于饱和碳酸氢钠溶液)
A B C D E F
16
(1) 写出标号仪器的名称:①__长颈漏斗。
(2) 实验室选用A、D装置可制取O2,化学反应方程式:__2KClO32KCl+3O2↑;若改用C装置收集,检验气体收集满的方法是__把带火星的木条放在集气瓶口,若木条复燃则集满。
(3) 选择发生装置B可以用于实验室制取CO2,若将发生装置由B改为F,其优点是__能够控制反应的发生与停止。为了得到纯净、干燥的CO2,按下图除杂装置,导管按气流方向连接的顺序应是__cdab(填字母)。检验CO2的化学反应方程式:__Ca(OH)2+CO2===__CaCO3↓+H2O。
27.(8分)水蒸气通过灼热的焦炭后得到的混合气体有哪些成分?某化学兴趣小组在老师的指导下,对此进行了实验探究。
【猜想与假设】①该混合气体只含有一氧化碳、氢气;
②该混合气体含有一氧化碳、二氧化碳、氢气和水蒸气;
③该混合气体只含有二氧化碳、氢气和水蒸气;
④该混合气体只含有一氧化碳、二氧化碳和氢气。
【査阅资料】①无水硫酸铜遇水由白色变为蓝色;
②碱石灰是固体氢氧化钠和氧化钙的混合物;
16
③氢气与一氧化碳都具有还原性。
【收集证据】同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去),并进行了实验。
(1)装置A中无水硫酸铜由白色变为蓝色,装置B中澄清石灰水变浑浊,由此得出的结论为混合气体中有__水蒸气和二氧化碳。B中发生反应的化学方程式为__Ca(OH)2+CO2===__CaCO3↓+H2O。
(2)反应前装置C中的药品为__氢氧化钠溶液。
(3)反应后E中红色氧化铁粉末变为黑色,F中无水硫酸铜由白色变为蓝色,G中澄清石灰水变浑浊,说明混合气体中还存在的气体是__氢气和一氧化碳。
【实验结论】猜想_② 正确。
【实验反思】经过讨论,同学们将上图装置进行了简化,
16
只用如图所示装置并自选必要试剂就能完成探究(假设每步都完全反应)。实验过程中干燥的凉烧杯内壁能观察到的现象是__有水珠(或水雾),应补充的最后一步实验操作及现象是__迅速将小烧杯倒转,并向其中倒入澄清石灰水,石灰水变浑浊。
四、分析与计算(本大题共1个小题,共6分)
28.(6分)某同学向一定质量的碳酸钠溶液中加入50 g的稀盐酸,并将实验数据绘制成如图曲线,请回答:
(1)反应过程中产生气体的质量为__2.2__g。
(2)计算所用稀盐酸的溶质的质量分数。(结果精确到0.1%)(化学方程式:Na2CO3+2HCl=== 2NaCl+CO2↑+H2O)
解:(1)由图示可知生成的二氧化碳的质量为2.2 g;故答案为:2.2 g;
(2)设消耗氯化氢的质量为x。
Na2CO3+2HCl=== 2NaCl+CO2↑+H2O
73 44
x 2.2 g
16
= x=3.65 g
所用稀盐酸的溶质的质量分数×100%=9.1%
答:所用稀盐酸的溶质的质量分数9.1%。
16
相关文档
- 黑龙江省哈尔滨市第四十七中学20202021-11-109页
- 2010中考数学眉山考试试题2021-11-1012页
- 徐州专版2020中考化学复习方案第82021-11-103页
- 【2020年中考语文,含答案,word可编辑2021-11-108页
- 呼和浩特专版2020中考道德与法治复2021-11-105页
- 济南市济阳区2019-2020学年八年级2021-11-109页
- 包头专版2020中考生物复习方案专题2021-11-1013页
- 2020年江苏省盐城市中考数学试卷【2021-11-1010页
- 湖北省2021年中考历史模拟试题及答2021-11-1013页
- 2012年江苏省南京市中考数学试题(含2021-11-1013页