- 247.87 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
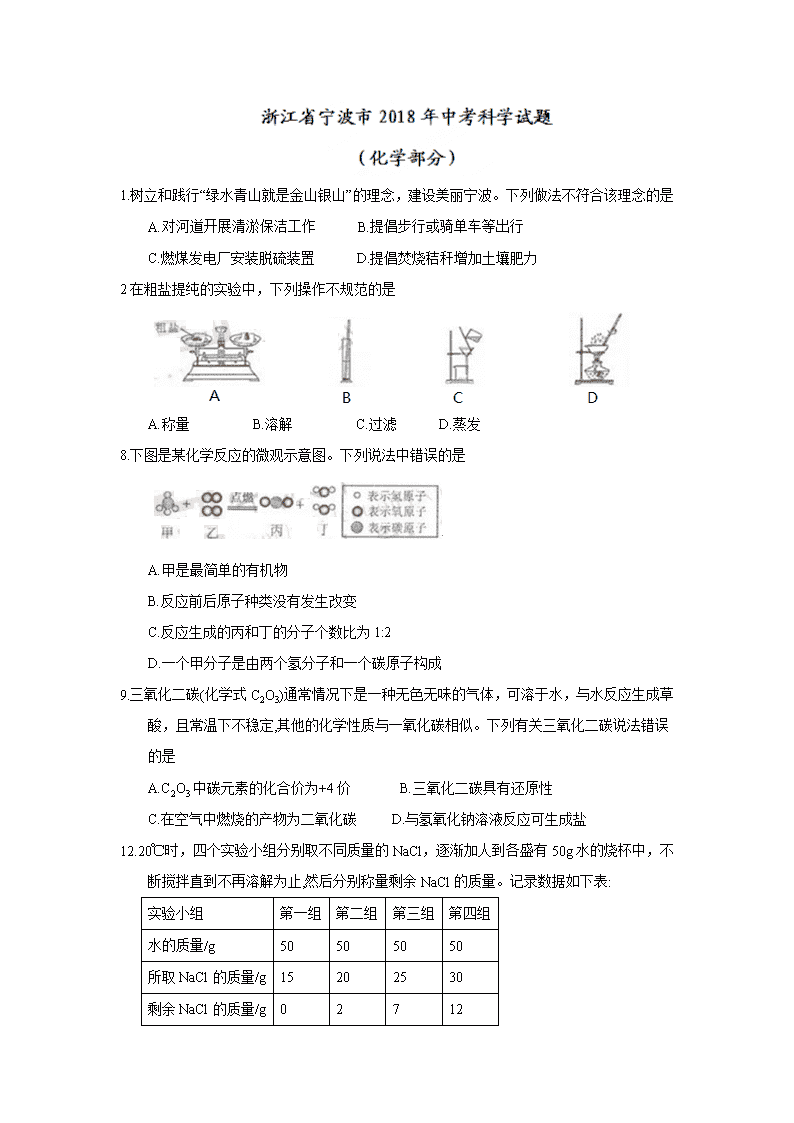
1.树立和践行“绿水青山就是金山银山”的理念,建设美丽宁波。下列做法不符合该理念的是
A.对河道开展清淤保洁工作 B.提倡步行或骑单车等出行
C.燃煤发电厂安装脱硫装置 D.提倡焚烧秸秆增加土壤肥力
2在粗盐提纯的实验中,下列操作不规范的是
A.称量 B.溶解 C.过滤 D.蒸发
8.下图是某化学反应的微观示意图。下列说法中错误的是
A.甲是最简单的有机物
B.反应前后原子种类没有发生改变
C.反应生成的丙和丁的分子个数比为1:2
D.一个甲分子是由两个氢分子和一个碳原子构成
9.三氧化二碳(化学式C2O3)通常情况下是一种无色无味的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其他的化学性质与一氧化碳相似。下列有关三氧化二碳说法错误的是
A.C2O3中碳元素的化合价为+4价 B.三氧化二碳具有还原性
C.在空气中燃烧的产物为二氧化碳 D.与氢氧化钠溶液反应可生成盐
12.20℃时,四个实验小组分别取不同质量的NaCl,逐渐加人到各盛有50g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。记录数据如下表:
实验小组
第一组
第二组
第三组
第四组
水的质量/g
50
50
50
50
所取NaCl的质量/g
15
20
25
30
剩余NaCl的质量/g
0
2
7
12
下列说法错误的是
A.20℃时,50gNaCl饱和溶液中含有18gNaCl
B.用蒸发的方法可以使不饱和溶液变成饱和溶液
C.第二组所得溶液的溶质与溶剂的质量比为9:25
D.相同温度下,NaCl在水里的溶解度与水的质量无关
14. 向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是
19.如图是用铜丝绕成的锥形螺旋罩,置于酒精灯火焰上方。随着铜丝罩的垂直下移,可观察到酒精灯火焰越来越小,最终完全熄灭。
(1)铜丝在空气中受热,表面会产生黑色的_______(填化学式)。
(2)表面变黑的铜丝下移过程中遇到酒精蒸气,又会变光亮的红色,这是因为黑色物质发生了_______反应。(填“氧化”或“还原“)
(3)铜丝具有良好的导热性,能将热量很快散失,使酒精蒸气的温度低于_______,从而使酒精灯火焰熄灭。
21.右图是铁盐酸氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“—”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。
①2类 ②3类 ③4类 ④5类
26.小科从标签得知雪碧成分中有水、二氧化碳、柠檬酸、柠檬酸钠等。查阅资料知道1体积雪碧中含有约3体积二氧化碳,柠檬酸的含量约为2.8g/1000mL。柠檬酸与碳酸钠反应的化学方程式为:
2C6H8O7+3Na2CO3==2C6H5O2Na3+3CO2↑+3H2O。
他用一瓶500mL的雪碧做了如下实验:。
实验步骤
步骤一
步骤二
步骤三
步骤四
操作过程
倒出三分之二雪碧,测其pH
在剩余雪碧中加入约6g Na2CO3
立即盖上瓶盖,摇匀。
测溶液pH
现象或结果
pH约为3
产生大量气泡
气泡消失,瓶子略瘪
pH约为9
【发现问题】CO2去哪儿了?
【提出猜想】①CO2被溶解了;②CO2与H2O发生了反应;③CO2与Na2CO3溶液发生了反应。小思否定了猜想①和②,其理由是___________。
【设计实验】对猜想③进行实验探究。
实验编号
实验一
实验二
实验三
实验四
实验装置
Na2CO3
Na2CO3
收集一瓶CO2
操作过程
溶液中滴加CaCl2溶液
溶液中通入过量CO2后,滴加CaCl2溶液
,加入30mL饱和Na2CO3溶液,盖上瓶盖摇匀
将实验三的溶液低温蒸发、干燥,得到的白色粉末按如图所示装置进行实验
实验現象
产生白色沉淀
无明显变化
瓶变瘪,瓶底有晶体析出
A试管口有水滴,澄清石灰水变浑浊
根据实验探究过程,回答下列问题:
(1)设计实验一的作用是________ 。
(2)实验四中A试管口略向下倾斜,其目的是_______ 。
(3)根据实验探究得出:CO2与Na2CO3溶液反应的化学方程式:_________。
28.丁酸乙所是无色有菠萝香昧的液体,其密度为0.87g/cm3,难溶于水,可与油类互溶。现取11.6g丁酸乙酯在氧气中完全燃烧,只产生26.4gCO2和10.8gH2O。
(1)含有丁酸乙酯的物品应远离火源。若丁酸乙酯燃烧,____ (填“能”或不能”)用水来灭火。
(2)丁酸乙酯可与油类互溶,这种性质属于______性质。
(3)丁酸乙酯中碳元素和氢元素的质量比为______。
32.为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:
①取200g混合溶液加人足量的AgNO3溶液,经过滤、洗涤、干燥、称量,得到143.5gAgCl固体;
②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别
一
二
三
四
五
混合溶液质量/g
200
200
200
200
200
铁屑质量/g
6
9
12
15
18
析出铜的质量/g
6.4
9.6
m
16
16
请分析计算:
(1)表中第三组实验的m值为_______。
(2)第_____组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少? (计算结果精确到0.1%)
(4)原混合溶液中FeCl2 的质量分数为多少? (计算结果精确到0.1%)
浙江省宁波市2018中考科学试题化学部分
参考答案
1D 2B 8D 9A 12A 14B
19、(1)CuO;(2)还原;(3)着火点
21、(1)Fe;(2)复分解反应;(3)③
26、原CO2在溶液中已经饱和
(1)与实验二对照;
(2)防止试管口冷凝的水倒流导致试管底部破裂
(3)CO2+Na2CO3+H2O==2NaHCO3
28、(1)不能;(2)物理;(3)6:1
32.(1)12.8;(2)四;(3)93.3%;(4)15.9%
相关文档
- 2020年黑龙江省哈尔滨市中考数学试2021-11-1023页
- 江苏省2018-2020年三年中考物理真2021-11-108页
- 2020-2021年中考语文一轮复习专题2021-11-1018页
- 2020年初三中考复习世界近现代史资2021-11-104页
- 【精品试卷】中考数学一轮复习 专2021-11-106页
- 2019广西历史中考真题2021-11-102页
- 15届 山东省临沂地理中考试题2021-11-108页
- 2019年湖北省黄石市中考数学试卷2021-11-1025页
- 辽宁省锦州市2013年中考化学模拟试2021-11-109页
- 中考物理必考实验 专题实验03探究2021-11-1013页