- 177.00 KB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
1
5.3 二氧化碳的性质和制法
教学目标
通过探究活动了解二氧化碳的性质。
教学重点
二氧化碳的性质。
教学难点
二氧化碳性质的探究过程和方法。
教学用具
二氧化碳发生装置、集气瓶、玻璃片、烧杯、试管、导管、铁架台。酒精灯、火柴。
药品准备 石灰石、稀盐酸、石蕊溶液、澄清石灰水。
本节考点 二氧化碳的性质及应用。
教学过程
[复习提问]听写化学方程式
[讲述]碳完全燃烧的产物是二氧化碳,它是与人类生活密切相关的物质,我们有必要更多
地认识它。
[板书].二氧化碳的性质
1.物理性质:无色、无味的气体。标准状况下密度为 1.977g/L。加压降温后变为液体,
进而凝固为白色雪状固体,叫做“干冰”。干冰可升华,即由固体直接转化为气体。
[探究活动]
问题 二氧化碳有哪些性质?
【实验 5-5】在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,将一瓶二氧
化碳通过漏斗向烧杯倾倒。
现象 蜡烛自下向上依次熄灭
推断 (1)二氧化碳密度比空气大
(2)二氧化碳不燃烧,不支持燃烧
【实验 5-6】取一只试管,滴进适量紫色石蕊溶液,然后通入二氧化碳直至变色,
再将试管加热,又有什么现象产生?
现象 紫色石蕊溶液变成红色,加热后又变成紫色
推断 二氧化碳可溶于水,跟水反应生成碳酸
【实验 5-7】取一只盛澄清石灰水的试管,通过玻璃管,往石灰水里吹一会儿气,
有什么现象发生?
现象 澄清石灰水中出现白色不溶物
推断 二氧化碳与氢氧化钙反应生成白色不溶物
[板 书]2.化学性质
2
①二氧化碳不燃烧也不支持燃烧
②二氧化碳可溶于水,跟水反应生成碳酸
碳酸能使紫色石蕊试液变红色
碳酸不稳定,受热容易发生分解
③二氧化碳跟氢氧化钙反应生成白色的碳酸钙沉淀
该反应常用来检验二氧化碳
[小 结]二氧化碳的性质
1.物理性质:无色、无味的气体。标准状况下密度为 1.977g/L。加压降温后
变为液体,进而凝固为白色雪状固体,叫做“干冰”。干冰可升华,即有固体界转化为气体。
2.化学性质
①二氧化碳不燃烧也不支持燃烧
②
③
[聚焦考点]
1、二氧化碳的下述用途没有利用其化学性质的是(C)
A.CO2 用作气体肥料 B、CO2 用于灭火
C.干冰用于人工降雨 D、CO2 用来制 Na2CO3
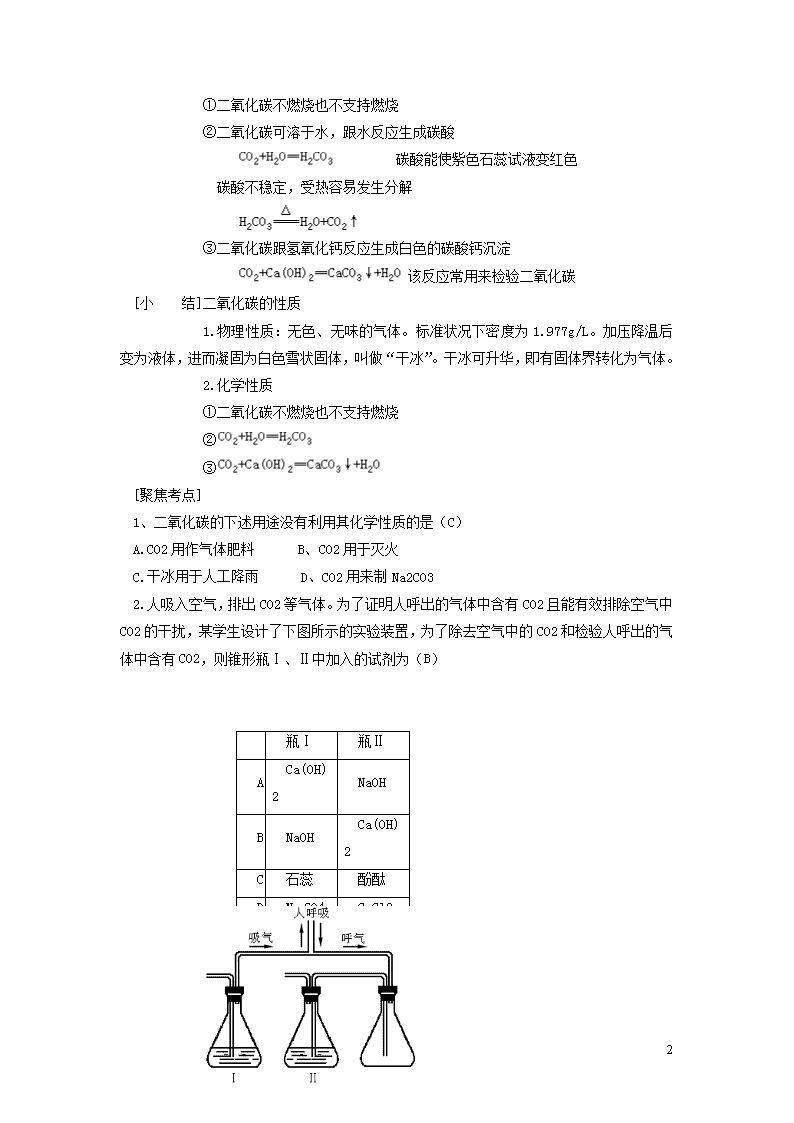
2.人吸入空气,排出 CO2 等气体。为了证明人呼出的气体中含有 CO2 且能有效排除空气中
CO2 的干扰,某学生设计了下图所示的实验装置,为了除去空气中的 CO2 和检验人呼出的气
体中含有 CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为(B)
瓶Ⅰ 瓶Ⅱ
A
Ca(OH)
2
NaOH
B NaOH
Ca(OH)
2
C 石蕊 酚酞
D Na2SO4 CaCl2
3
3.小强在进行二氧化碳的性质实验时,经过认真分析研究,对课本中的气体发生装置(图
A)进行了改进(图 B)。
(1)改进后装置的优点是___________。
(2)将制得的二氧化碳气体通入盛有澄清石灰水的试管中,观察到的现象是___________,
该反应的化学方程式为 。
(3)将 D 中的 CO2 倒入 C 中做性质实验时,操作方法是 ;观察到的现象是 。
此实验说明二氧化碳 ,且 。
4. 在学习碳的化学性质时,碳和氧化铜反应生成的气体是一氧化碳还是二氧化碳?或者
是两者都有呢?某学习小组对此展开了探究。
(l)甲、乙同学分别提出了检验一氧化碳的方案,但都被大家否定了。请在下表中写出乙
方案不可行的原因(写出一种即可)。
(2)在老师的指导下,同学们把滤纸浸泡在磷钼酸与氯化金钯的黄色混合液中,制成试
纸(试纸遇一氧化碳立刻变蓝色,而遇二氧化碳不反应).按如图装置进行实验,发现 B 装
置中的试纸没有变色,C 装置中的澄清石灰水变浑浊。请写出 A 装置中发生的化学反应方程
式______________________________。
(3)如果调换 B、C 装置,实验结束时先停止加热.将会出现什么现象_______________。
检验方案 不可行的原因
甲
把小动物放在收集的气体
中,观察能否存活
即使没有一氧化碳,小动物也可能
会窒息死亡
乙
点燃生成的气体,观察能
否燃烧
_____________________________
4
[布置作业]
第二课时 探究二氧化碳的实验室制法和用途
教学目标
初步学会制取 CO2,了解实验室内制备气体的思路和方法。
教学重点
二氧化碳的实验室制法
教学难点
二氧化碳制法的探究过程和方法
教学用具
二氧化碳发生装置、集气瓶、玻璃片。
石灰石、稀盐酸。
酒精灯、火柴。
本节考点 实验室制取气体的方法
教学过程
[复习提问]听写化学方程式
[讲 述]碳燃烧可以得到二氧化碳,但是这种方法所制得的二氧化碳既不纯净又难收
集,所以,实验室常用稀盐酸和大理石或石灰石(主要成分是碳酸钙)在常温下反应来制取
二氧化碳。
[探究活动]【实验 5-8】装置好仪器,在左边锥形瓶中放入适量大理石碎块,通过长颈漏
斗加入稀盐酸,产生的二氧化碳通过导管收集到右边的集气瓶里,用玻璃片盖好。
现象 产生大量气泡
[讨论]实验室制取二氧化碳时,能否用稀硫酸代替稀盐酸?能否用浓盐
酸?
[讲解]都不能。CaCO3 + H2SO4 === CaSO4 + H2O + CO2↑ ,CaSO4 微溶于水,覆盖在大
理石表面,阻止反应的进行。而浓盐酸能挥发出氯化氢气体,使制得的二氧化碳不纯。
[板书]五.二氧化碳的实验室制法
1.反应原理:大理石或石灰石跟稀盐酸反应
CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
2.发生装置:固-液不加热型(同氢气)
锥形瓶(或广口瓶、大试管)装固体,长颈漏斗加酸液,双孔橡皮塞,导气管
3.操作:检——装——收
4.收集装置:向上排空气法
5
集气瓶,玻璃片
5.检验:a.通入澄清石灰水中,石灰水变浑浊(验证)
b.燃着的木条(验满)
[讨论]P.145 讨论与交流
[小结]二氧化碳的实验室制取原理、装置、收集方法、检验方法。
[聚焦考点]
1.某课外活动小组的同学用下列装置探究 CO2 的实验室制法。
(1)甲同学用大理石
与稀盐酸反应制取 CO2,
应 该 选 用 的 发 生 装 置
是 ,收集装置是 发生反应的化学方程式为;
(2)加热固体碳酸氢钠或固体碳酸氢铵都能产生 CO2,其方程式分别是:
NH4HCO3 △ NH3↑+H2O+CO2↑
2NaHCO3 △ Na2CO3+H2O+CO2↑
乙同学利用加热碳酸氢钠的方法制取 CO2,应该选用的发生装置是 。他不选
用碳酸氢铵制取 CO2 的理由是 。
2.下图是实验室制取 CO2 和验证 CO2 性质的装置:
(1)写出图 中 标 号 为 a 的 仪 器 名
称: ;
(2)A 装置中发生反应的化学方程式为 ;
(3)将 A 与 B 相连还可制取的气体有(填标号) 。
用 H2O2 溶液和 MnO2 混合制 O2 ②用 Zn 粒和稀 H2SO4 制 H2 ③用 KMnO4 制 O2
(4)若 a 中的酸换为浓盐酸,某同学为验证浓盐酸的挥发性和碳酸的不稳定性,设计了两
个实验方案:
①将 A 与 C 相连观察到紫色石蕊试液变红色,就可证明浓盐酸的挥发性;
②将上述变红色的石蕊试液加热煮沸就可证明碳酸的不稳定性。
6
试评价上述实验方案是否合理:
方案① ;
方案② ;
[布置作业]
相关文档
- 人教版九年级化学上册教案(第七单元2021-11-115页
- 九年级化学上册第五章燃料5-4古生2021-11-114页
- 【沪教版】九年级化学:4-4《化石燃2021-11-1120页
- 九年级化学上册各单元知识点考点梳2021-11-118页
- 九年级化学上册第五章燃料5-1洁净2021-11-113页
- 九年级化学上册第五章燃料5-2组成2021-11-104页
- 2007-2011五年全国各地中考化学试2021-11-1056页
- 中考化学总复习(人教版)精讲精练:第72021-11-1014页
- 8年中考(2005-2012)全国各地中考化学2021-11-1086页
- 化石燃料的利用 学案2021-11-104页