- 13.15 MB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第 10 课时
化合价与化学式 物质的分类
主题二 物质构成的奥秘
考点一 化学式
1.定义:用 表示物质组成的式子。
2.书写
(1)单质
①稀有气体:用元素符号表示,如氦写为He,氖写为Ne。
②金属和固态非金属:用元素符号表示(碘除外),如铁写为Fe,碳写为C。
③气态非金属:用元素符号和数字表示,如氧气写为O2。
(2)化合物中,正左负右、标价交叉、化简复查,如氯化镁写为 。
元素符号和数字的组合
MgCl2
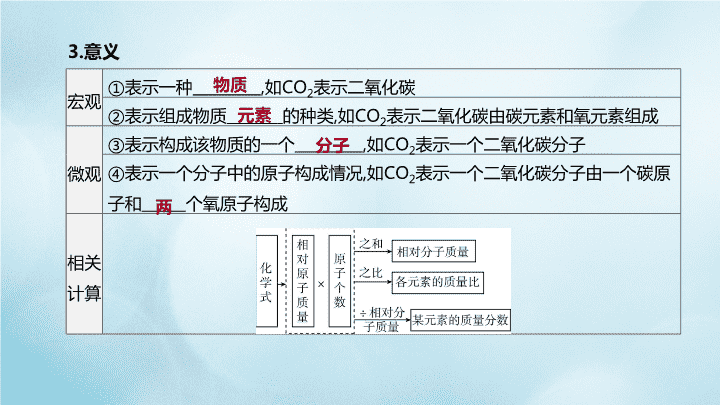
宏观
①表示一种 ,如CO2表示二氧化碳
②表示组成物质 的种类,如CO2表示二氧化碳由碳元素和氧元素组成
微观
③表示构成该物质的一个 ,如CO2表示一个二氧化碳分子
④表示一个分子中的原子构成情况,如CO2表示一个二氧化碳分子由一个碳原
子和 个氧原子构成
相关
计算
3.意义
物质
元素
分子
两
考点二 化合价
1.规定:化合价是元素的原子在形成化合物时表现出来的性质,化合价有_______
和 之分。
2.标写方法:通常在元素和原子团的正上方标出,正负号在前,数字在后,如 ,
当化合价中的数字为“1”时不省略。
3.规律
(1)金属元素与非金属元素化合时,金属元素显 价,非金属元素显 价。
(2)在化合物中,元素化合价的代数和为 。
(3)在单质里,元素的化合价为 。
正价
负价
正 负
0
0
4.常见元素及原子团的化合价
(1)常见元素化合价口诀
(2)常见原子团的化合价
5.应用
(1)应用化合价检验和书写已知物质的化学式或离子符号。
①排序(正左负右);
②标价交叉;
③化简复查。
如 。
(2)根据化学式或离子符号计算某元素的化合价。
考点三 化学符号周围数字的含义
图10-1
考点四 物质的分类
物
质
纯净物
(由①
物质组成)
单质(由②
元素组
成的纯净物)
金属单质,如Fe、Cu、Hg、Zn
非金属单质,如C、P、O2、H2、He
化合物(由
③ 元
素组成的纯
净物)
有机物(含碳元素的化
合物,CO、CO2、
H2CO3、碳酸盐除外)
有机小分子化合物,如CH4、
C2H5OH、C6H12O6
有机高分子化合物,如淀粉、
蛋白质、聚乙烯
一种
同种
不同种
物
质
纯净物
(由①
物
质组成)
化合物(由
③_________
元素组成的
纯净物)
无机物(不含
碳元素的化合
物,但包括CO、
CO2、H2CO3、
碳酸盐)
氧化物(由④
元素
组成,其中一种
是⑤
的化合物)
金属氧化物,如CuO、
Fe2O3、MnO2
含氧化合
物不一定
是氧化物,
如KMnO4
非金属氧化物,如
CO、H2O、SO2
(续表)
一种
不同种
两种
氧元素
物
质
纯净物
(由①
物
质组成)
化合物(由
③_________
元素组成的
纯净物)
无机物(不含碳元
素的化合物,但包
括CO、CO2、
H2CO3、碳酸盐)
酸:在水溶液中能解离出H+和酸根离
子,如HCl、H2SO4、HNO3
碱:在水溶液中能解离出金属离子(或
NH4+)和OH-,如NaOH、Ca(OH)2、
NH3·H2O
盐:由金属离子(或N)和酸根离子构成,
如NaCl、CaCO3、NH4Cl
混合物:由⑥ 或⑦ 以上的物质组成,如空气、合金、溶液
(续表)
一种
不同种
两种 两种
考向一 化学式的意义
1.[2019·泰安]我国女科学家屠呦呦因发现青蒿素荣获2015年诺贝尔生理学或
医学奖。青蒿素(C15H22O5)是一种用于治疗疟疾的药物。下列有关青蒿素的叙
述正确的是 ( )
A.从宏观上看:青蒿素分子由碳、氢、氧三种元素组成
B.从微观上看:青蒿素中含有15个碳原子、22个氢原子和5个氧原子
C.从变化上看:青蒿素在氧气中完全燃烧生成一氧化碳和水
D.从质量上看:青蒿素中碳、氧元素的质量比为9:4
[答案] D
[解析]从宏观上看,青蒿素由碳、氢、氧三种元素组成;青蒿素是由青蒿素分子
构成的,1个青蒿素分子中含有15个碳原子、22个氢原子和5个氧原子;由质量
守恒定律,反应前后元素种类不变可知,青蒿素在氧气中完全燃烧生成二氧化
碳和水;青蒿素中碳、氧元素的质量比为(12×15):(16×5)=9:4。
考向二 化学用语
2.[2019·连云港]下列化学用语表示正确的是 ( )
A.高锰酸钾的化学式:K2MnO4
B.60个碳原子:C60
C.2个氯离子:2Cl-
D.Mg2+的结构示意图:
[答案] C
[解析]高锰酸钾化学式
为KMnO4;60个碳原子
可以表示为60C;Mg2+
的结构示意图中,核内
质子数是12;2个氯离子
可以表示为2Cl-。
3.[2019·泰安]对下列化学用语中数字“2”含义的说法正确的是 ( )
①2H ②2NH3 ③SO2 ④
⑤Mg2+ ⑥2OH- ⑦H2O
A.表示离子个数的是⑤⑥
B.表示分子中原子个数的是③⑦
C.表示离子所带电荷数的是④⑤
D.表示分子个数的是①②
[答案] B
[解析]⑤中的“2”不能表示离子个数,表示每个镁离子带2个单位正电荷,A
不正确;③中的“2”表示每个二氧化硫分子含有2个氧原子,⑦中的“2”表
示每个水分子含有2个氢原子,B正确;④中的“2”表示氧化铜中铜元素化合
价是+2,⑤中的“2”表示每个镁离子带2个单位正电荷,C不正确;①中的
“2”表示2个氢原子,②中的“2”表示2个氨分子,D不正确。
4.[2019·西宁]用适当的化学用语填空。
(1)氦气 。
(2)由3个氧原子构成的单质分子 。
(3)碳酸氢根离子 。
(4)标出硫酸铝中铝元素的化合价 。
He
O3
考向三 化学式与化合价(6年6考)
5.[2019·泰安]“天宫二号”太空舱利用NiFe2O4
作催化剂,将航天员呼出的二氧化碳转化为氧气。
已知Fe元素的化合价为+3,则Ni元素的化合价为
( )
A.+1 B.+2
C.+3 D.+4
[答案] B
[解析]NiFe2O4中Fe元素的
化合价为+3,氧元素显-2
价,设镍元素的化合价是x,
根据在化合物中各元素正
负化合价代数和为零,可得
x+(+3)×2+(-2)×4=0,则
x=+2。
6.[2019·攀枝花]某同学制作的试剂标签如下,其中化学式书写不正确的是( )
图10-2
[答案] C
[解析]氧化镁中镁元素显+2价,氧元素显-2价,其化学式为MgO,标签中化学式
书写正确;氢氧化钾中钾元素显+1价,氢氧根显-1价,其化学式为KOH,标签中
化学式书写正确;氯化铝中铝元素显+3价,氯元素显-1价,其化学式为AlCl3,标
签中化学式书写错误;硝酸钠中钠元素显+1价,硝酸根显-1价,其化学式为
NaNO3,标签中化学式书写正确。
考向四 有关化学式的计算
7.[2019·德州]甲醇是一种无色、有特殊香味、易
挥发的液体,可用于制造甲醛和农药等。已知:甲醇
由碳、氢、氧三种元素组成,其中氢元素的质量分
数为12.5%,氧元素的质量分数为50%;一个甲醇分
子中含有4个氢原子。请通过计算回答下列问题。
(1)甲醇的相对分子质量是 。
[答案] (1)32
[解析] (1)每个甲醇分子中
有4个氢原子,而甲醇中氢
元素的质量分数为12.5%,
则甲醇的相对分子质量为
=32。
7.[2019·德州]甲醇是一种无色、有特殊香味、易挥
发的液体,可用于制造甲醛和农药等。已知:甲醇由
碳、氢、氧三种元素组成,其中氢元素的质量分数
为12.5%,氧元素的质量分数为50%;一个甲醇分子
中含有4个氢原子。请通过计算回答下列问题。
(2)一个甲醇分子中含氧原子的个数是 。
[答案] (2)1
[解析] (2)甲醇的相对分
子质量是32,甲醇中氧元
素的质量分数为50%,则
每个甲醇分子中氧原子的
个数为 =1。
8.[2019·平凉]如图10-3是某化肥的部分信
息。
请根据该信息计算:
(1)硫酸钾中钾、硫、氧三种元素的质量比为
。
图10-3
[答案] (1)39:16:32
[解析] (1)硫酸钾中钾、硫、氧
三种元素的质量比为(39×2):
32:(16×4)=39:16:32。
8.[2019·平凉]如图10-3是某化肥的部
分信息。
请根据该信息计算:
(2)该钾肥中钾元素的质量分数最高为
(精确至0.1%)。
[答案] (2)44.8%
[解析] (2)因为杂质不含钾元素,所以钾
肥中不含杂质时,钾元素质量分数最高,
故该钾肥中钾元素的质量分数最高为
×100%≈44.8%。
图10-3
考向五 物质的分类(6年6考)
9.[2019·巴中]分类是化学学习中常用
的思维方法。下列有关物质分类正确
的是 ( )
A.氧化物:干冰 冰水混合物 氧化铁
B.碱:烧碱 纯碱 氨水
C.混合物:合金 海水 高锰酸钾
D.有机物:甲烷 乙醇 碳酸钙
[答案] A
[解析]干冰、冰水混合物、氧化铁都属
于氧化物;烧碱和氨水属于碱,纯碱属于
盐;合金和海水属于混合物,高锰酸钾属
于纯净物;甲烷和乙醇属于有机物,碳酸
钙属于无机化合物。
10.[2019·聊城]归纳是化学学习过程中常用的方法。下列归纳中不正确的是
( )
A.单质:氩气、液氧、铝粉
B.常量元素:钙、碳、氧
C.铵态氮肥:尿素、氯化铵、硝酸铵
D.新能源:氢能、太阳能、核能
C
11.[2018·巴中]建立模型是学习化学的重要方法。下列有关模型正确的是( )
图10-4
[答案] D
[解析]可燃物的着火点一般不变;原子核由质子和中子构成,模型中质子不在原
子核内;纯净物包括化合物和单质,模型中化合物没包括在纯净物中;按体积计
算,空气由78%N2、21%O2和1%其他成分组成,模型描述与事实相符。
1.[2019·安徽]我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为
H25N34O3Cl),该物质是超高能材料,在航空航天上可作推进剂。下列有关该物
质的说法正确是 ( )
A.属于有机物
B.由四种非金属元素组成
C.H25N34O3Cl中原子总数为62
D.氢、氮、氧、氯的原子个数比为1∶7∶8∶17
[答案] B
[解析]本题考查的是化学式的意义。从全氮阴离子盐的化学式H25N34O3Cl可
以看出该物质中不含有碳元素,有机物是含碳元素的化合物,故该物质不属于
有机物;从全氮阴离子盐的化学式H25N34O3Cl可以看出该物质是由氢、氮、
氧、氯四种非金属元素组成的;1个H25N34O3Cl分子中原子总数为25+34+3
+1=63;从全氮阴离子盐的化学式H25N34O3Cl可以看出氢、氮、氧、氯的原
子个数比为25∶34∶3∶1。
2.[2017·安徽]据报道,我国科学家发现一种氦钠化合物(化学式为Na2He)。下
列说法正确的是 ( )
A.Na2He中Na为+1价,He为-1价
B.Na2He中Na、He元素的质量比为2∶1
C.Na2He中既含金属元素,又含非金属元素
D.稀有气体很稳定,不与任何物质发生反应
[答案] C
[解析]根据在化合物中各元素正、负化合价的代数和为零,Na为+1价,则He为
-2价;Na2He中Na、He元素的质量比为(23×2)∶4=23∶2;Na2He中Na为金
属元素,He为非金属元素,则Na2He中既含金属元素,又含非金属元素;稀有气
体很稳定,但在一定条件下也可与某些物质发生反应。
相关文档
- 包头专版2020中考化学复习方案主题2021-11-1110页
- 河北专版2020中考化学复习方案主题2021-11-1133页
- 徐州专版2020中考化学复习方案第32021-11-114页
- 2020九年级化学上册 第三单元 物质2021-11-114页
- 九年级化学单元测试卷 第三单元 2021-11-116页
- 包头专版2020中考化学复习方案主题2021-11-1119页
- 2020九年级化学上册第三单元物质构2021-11-116页
- 徐州专版2020中考化学复习方案第32021-11-115页
- 江西专版2020年中考化学复习方案第2021-11-1137页
- 2020中考化学复习方案主题一物质构2021-11-115页