- 338.00 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2013年中考化学综合能力一及答案
初三综合能力题一
A、(本题包括2小题,共18分)
①
D
③
②
A
X
B
C
X
E
F
B
20.(8分)已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质。它们相互转化的关系如右图所示
(图中反应条件略去)。
(1)X在反应①中起 作用。
(2)写出有关物质的化学式:
A 、C 。
(3)若F不溶于稀硫酸,写出反应③的化学方程式 ,
该反应的基本类型是__________。与D具有相同化学性质,并能与E发生反应,且反应基本类型与③相同的物质有 。
21.(10分)人类社会的发展离不开能源。当今社会,人类利用的能源主要来自化石燃料。
(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属__________变化。化石燃料中主要含有碳、氢元素,完全燃烧的产物是_____________,还含有硫、氮等元素,燃烧时会转化为_________________。
(2)西气东输,将改变我市居民的气体燃料结构。下表是几种气体燃料的价格和热值:
燃烧物
煤气
液化石油气
天然气
价格
1.4元/千克
6.0元/千克
1.8元/千克
热值
1.56×104kJ/kg
4.5×104kJ/kg
3.9×104kJ/kg
综合考虑,你将选用哪种燃料? 理由是_______________________________。
(3)化石燃料不仅是优质的能量资源,还是宝贵的化工资源。聚乙烯是一种最常用的塑料,它是以石油裂解气体乙烯(CH2=CH2)为原料,经许多乙烯分子打开双键(-CH2-CH2-)连在一起,聚合成大分子而形成的。下图是聚乙烯分子形成过程的示意图,卡通画中单个小人代表一个乙烯分子。聚乙烯其中的部分结构可表示为:… …。
(4)开发和利用清洁高效而又用之不竭的新能源,是21世纪人类面临的重要课题。
①2006年1月起,我省苏北四市推广使用乙醇汽油。乙醇可利用农作物发酵制得,农作物在催化剂作用下转化为葡萄糖(C6H12O6),然后葡萄糖在酒化酶的作用下转化为乙醇和二氧化碳,写出葡萄糖转化为乙醇的化学方程式 。
②氢气是一种未来理想的能源。现通过生物法制得的氢气中混有CO2、O2和水蒸气等(氢气的体积分数通常为60℅~90℅),为了得到纯净的氢气,将混合气体依次通过NaOH溶液、灼热的Cu丝和干燥装置。该除杂方案是否正确? ,理由是
。
B、(本题包括2小题。共18分)
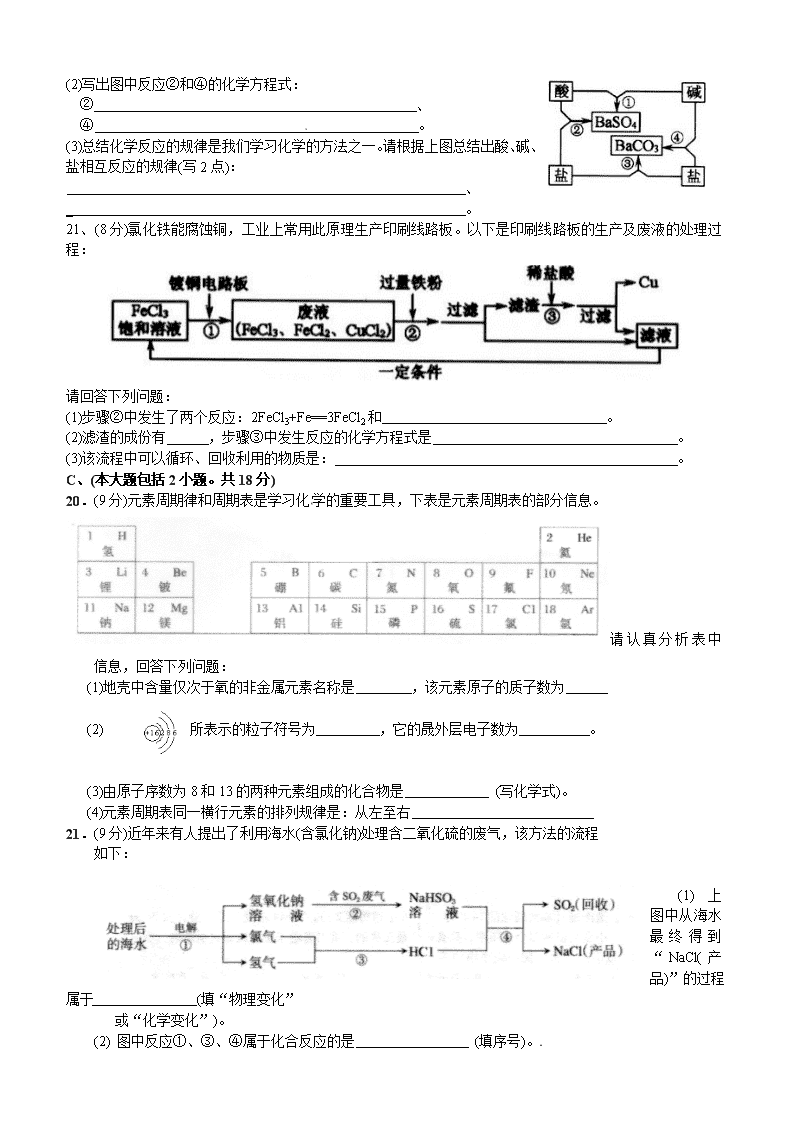
20、(10分)右图是常见酸、碱、盐之间的相互转化关系。
(1)写出图中相应物质的化学式:酸 、碱 。
(2)写出图中反应②和④的化学方程式:
② 、
④ 。
(3)总结化学反应的规律是我们学习化学的方法之一。请根据上图总结出酸、碱、盐相互反应的规律(写2点):
、
_ 。
21、(8分)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:[来源:www.shulihua.net]
(1)步骤②中发生了两个反应:2FeCl3+Fe==3FeCl2和 。
(2)滤渣的成份有 ,步骤③中发生反应的化学方程式是 。
(3)该流程中可以循环、回收利用的物质是: 。
C、(本大题包括2小题。共18分)
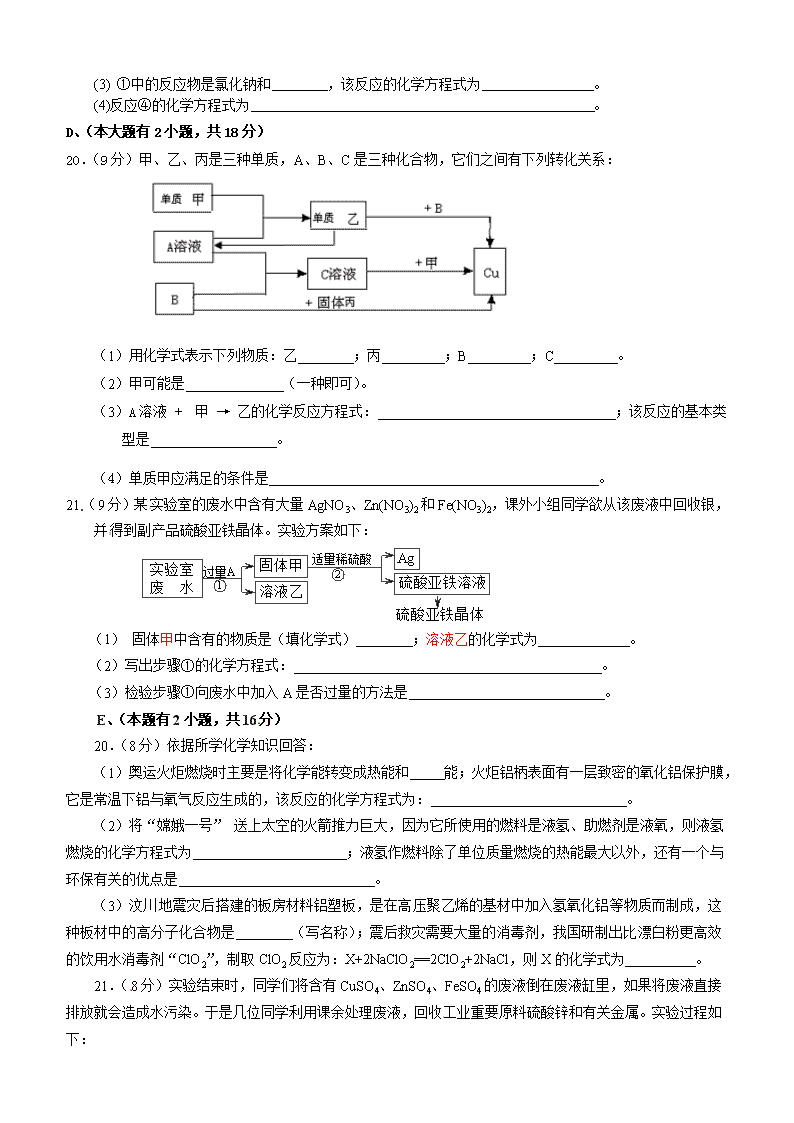
20.(9分)元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是 ,该元素原子的质子数为
(2) 所表示的粒子符号为 ,它的晟外层电子数为 。
(3)由原子序数为8和13的两种元素组成的化合物是 (写化学式)。
(4)元素周期表同一横行元素的排列规律是:从左至右
21.(9分)近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程
如下:[来源:www.shulihua.net]
(1) 上图中从海水最终得到“NaCl(产品)”的过程属于 (填“物理变化”
或“化学变化”)。
(2) 图中反应①、③、④属于化合反应的是 (填序号)。
(3) ①中的反应物是氯化钠和 ,该反应的化学方程式为 。
(4)反应④的化学方程式为 。
D、(本大题有2小题,共18分)
20.(9分)甲、乙、丙是三种单质,A、B、C是三种化合物,它们之间有下列转化关系:
(1)用化学式表示下列物质:乙 ;丙 ;B ;C 。
(2)甲可能是 (一种即可)。
(3)A溶液 + 甲 → 乙的化学反应方程式: ;该反应的基本类型是 。
(4)单质甲应满足的条件是 。
21.(9分)某实验室的废水中含有大量AgNO3、Zn(NO3)2和Fe(NO3)2,课外小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体。实验方案如下:
[来源:www.shulihua.netwww.shulihua.net]
(1) 固体甲中含有的物质是(填化学式) ;溶液乙的化学式为 。
(2)写出步骤①的化学方程式: 。
(3)检验步骤①向废水中加入A是否过量的方法是 。
E、(本题有2小题,共16分)
20.(8分)依据所学化学知识回答:
(1)奥运火炬燃烧时主要是将化学能转变成热能和 能;火炬铝柄表面有一层致密的氧化铝保护膜,它是常温下铝与氧气反应生成的,该反应的化学方程式为: 。
(2)将“嫦娥一号” 送上太空的火箭推力巨大,因为它所使用的燃料是液氢、助燃剂是液氧,则液氢燃烧的化学方程式为 ;液氢作燃料除了单位质量燃烧的热能最大以外,还有一个与环保有关的优点是 。
(3)汶川地震灾后搭建的板房材料铝塑板,是在高压聚乙烯的基材中加入氢氧化铝等物质而制成,这种板材中的高分子化合物是 (写名称);震后救灾需要大量的消毒剂,我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,制取ClO2反应为:X+2NaClO2==2ClO2+2NaCl,则X的化学式为 。
21.(8分)实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染。于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是 ;固体B的化学式为 。
(2)写出步骤①其中一个反应的化学方程式 ;
步骤④发生反应的化学方程式为 。
(3)要检验步骤④中加入的稀硫酸是否足量的方法是
。
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和 。
初三综合能力题一答案
A、(共18分)
20.(8分)(1) 催化 (1分) (2) H2O2、O2 (各1分)
(3) H2 + CuO Cu + H2O (2分) 置换反应 (1分) C、Mg (各1分)
21.(10分)(1) 物理 (1分) CO2 H2O (1分) SO2和氮的氧化物 (1分) [来源:www.shulihua.net数理化网]
(2) 天然气 (1分) 热值高,价格相对较低,对环境污染较小 (1分)
酒化酶
(3) …-CH2- CH2- CH2- CH2- CH2- CH2-… (1分)
葡萄糖
(4) ① C6H12O6 2C2H5OH + 2CO2 (2分)
② 不正确 (1分) 通过灼热的Cu丝时,混合气体可能发生爆炸 (1分)
B、(本大题包括2小题,共18分)
20、(10分)
(1)(2分)H2SO4 Ba(OH)2
(2)(4分)H2SO4+BaCl2==BaSO4↓+2HCl (2分,其它合理答案都给分)
Ba(OH)2+Na2CO3==BaCO3↓+2NaOH (2分,其它合理答案都给分)
(3)(4分)酸与碱反应生成盐和水;酸与盐反应生成新酸和新盐:碱与盐反应生成新碱和新盐;盐与盐反应生成两新盐(写对一点给2分。任意两点均可,其它合理答案都给分)
21、(8分)
(1)(2分)Fe+CuCl2==FeCl2+Cu
(2)(4分)Fe、Cu(或铁、铜,2分) 2HCl+Fe==FeCl2+H2↑(2分)
(3)(2分)FeCl3、Cu或FeCl2、Cu
C、(本大题包括2小题,共18分)
20.(9分)
(1) (2分)硅 14 (2) (2分) S 6 (3)(2分) A12O3
(4) (3分)原子序数(核电荷数)依次增大(或由金属逐渐过渡到非金属)
21.(9分)通电
(1)(1分)化学变化 (2) (1分) ③
(3)(4分)水(或H2O)(1分) 2NaCl+2H2O 2NaOH+Cl2↑+H2↑(3分)
(4)(3分)NaHSO3+HCl====NaCl+ SO2↑+ H2O
D、(本大题有2小题,共18分)
20.(9分)(1) H2 ; C; CuO ; CuCl2 (每空1分,共4分)
(2) Mg或Al或Zn或Fe (或写名称) (1分)
(3)2HCl+Mg=MgCl2+H2↑(2分)(其它合理得分,反应条件、配平、箭号等写错扣1分,化学式错误不给分,下同) 置换反应(1分)
(4)在金属活动顺序中位于氢的前面(1分)
21.(9分)
(1)Ag、Fe、Zn(漏写一种扣1分,写错一种不得分,共2分) Zn(NO3)2(1分)
(2)Zn+2AgNO3 ===Zn(NO3)2+2Ag (2分)
Zn+ Fe(NO3)2==Zn(NO3)2+ Fe (2分)
(3)取少量上层清液,加入少量锌粒(1分),若锌粒上有固体析出,则A不过量,若锌粒上无固体析出,则A过量(1分)(共2分)
E、(本题有2小题,共16分)[来源:www.shulihua.net]
20.(8分)
点燃
(1)(3分)光(1分) 4Al + 3O2 ==2 Al2O3(2分)
(2)(3分)2H2+O2=====2H2O(2分) 燃烧产物无污染(或产物是水,1分)
(3)(2分)聚乙烯 Cl2
21.(8分)
(1)(2分)硫酸锌(1分) Fe(1分)
(2)(2分)Zn+CuSO4 =ZnSO4 +Cu 或Zn+ FeSO4== ZnSO4+ Fe(1分) Zn+H2SO4 =ZnSO4 +H2↑
(1分)
(3)(2分)取步骤④的滤渣于试管中加入少量稀硫酸(1分),若有气泡产生则酸不足量(或若无气泡
产生,则酸已足量,1分)
(4)(2分)硫酸锌的质量(1分)、锌粉的质量(1分)[或硫酸锌、固体B、固体C、铜的质量,每说到2个给1分、全对给2分]