- 91.00 KB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
上海市2006年中考化学试题
(满分150分,考试时间100分钟)
化学部分
相对原子质量:H-1、C-12、O-16、S-32、Cl-35.5、K-39、Ca-40
六、填表题(共10分)
27、在下表的空格中写出相应的物质名称、化学式或物质的类别(指单质、氧化物、酸、碱、盐)。
物质名称
氢氧化钾
氯化钠
化学式
MgO
HNO3
物质类别
单质(金属)
七、单项选择题(共10分)
28、下列变化中属于化学变化的是( )
A、榨取果汁 B、粉碎废纸 C、切割玻璃 D、燃放烟花
29、水是生命的源泉,下列“水”中属于纯净物的是( )
A、矿泉水 B、蒸馏水 C、雨水 D、自来水
30、农作物生长需要氮、磷、钾等营养元素,下列化学肥料中属于钾肥的是( )
A、(NH4)2SO4 B、NH4HCO3 C、NH4NO3 D、K2CO3
31、“笑气”(N2O)在医学上曾被用作麻醉剂,其中N元素的化合价是( )
A、-1 B、+1 C、+2 D、+3
32、根据反应3NO2 + H2O → 2HNO3 + X,推断X的化学式为( )
A、N2 B、NO C、N2O3 D、N2O5
33、鉴别两瓶失去标签的盐酸和硫酸溶液,可使用下列试剂中的( )
A、酚酞试液 B、石蕊试液 C、BaCl2溶液 D、Na2CO3溶液
34、将甲、乙两种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是( )
A、甲>铜>乙 B、乙>铜>甲 C、铜>甲>乙 D、甲>乙>铜
35、下列实验操作中错误的是( )
A、实验室制取气体,要先对装置的气密性进行检查
B、可燃性气体点燃之前必须检查其纯度
C、给玻璃仪器加热时都需垫石棉网
D、实验产生的废液应倒入指定的容器内
36、下列变化中,氢元素由化合态变成游离态的是( )
A、电解水 B、燃烧氢气 C、氢气液化 D、碳酸分解
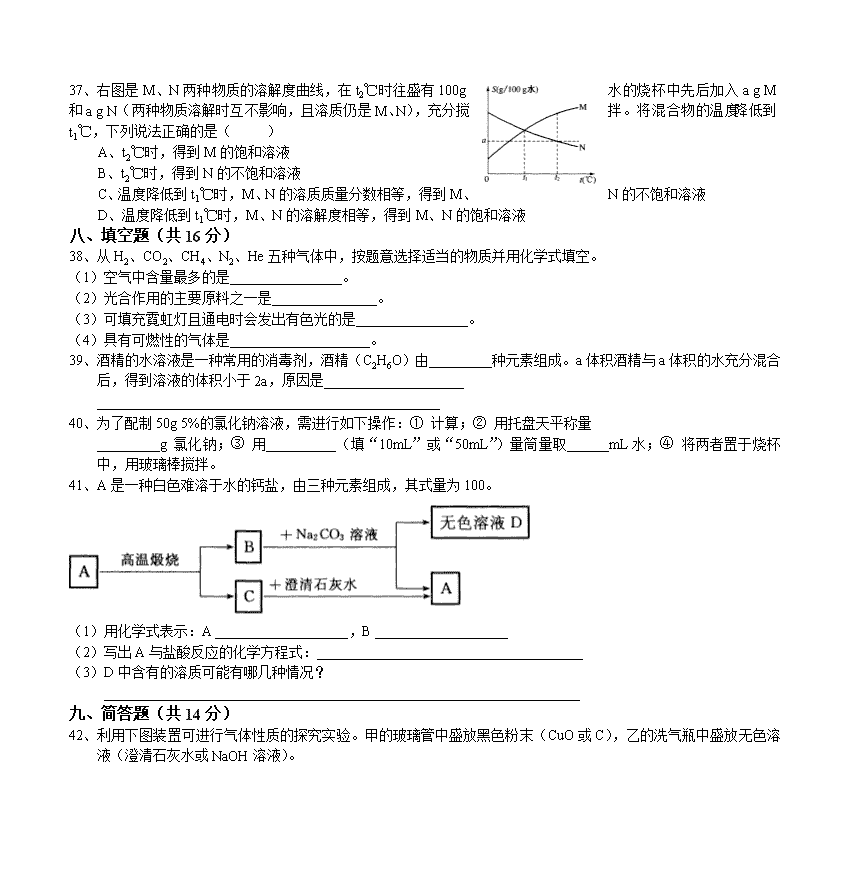
37、右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入a g M和a g N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌。将混合物的温度降低到t1℃,下列说法正确的是( )
A、t2℃时,得到M的饱和溶液
B、t2℃时,得到N的不饱和溶液
C、温度降低到t1℃时,M、N的溶质质量分数相等,得到M、N的不饱和溶液
D、温度降低到t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
八、填空题(共16分)
38、从H2、CO2、CH4、N2、He五种气体中,按题意选择适当的物质并用化学式填空。
(1)空气中含量最多的是________________。
(2)光合作用的主要原料之一是_______________。
(3)可填充霓虹灯且通电时会发出有色光的是________________。
(4)具有可燃性的气体是____________________。
39、酒精的水溶液是一种常用的消毒剂,酒精(C2H6O)由_________种元素组成。a体积酒精与a体积的水充分混合后,得到溶液的体积小于2a,原因是____________________
_________________________________________________
40、为了配制50g 5%的氯化钠溶液,需进行如下操作:① 计算;② 用托盘天平称量
_________g 氯化钠;③ 用__________(填“10mL”或“50mL”)量筒量取______mL水;④ 将两者置于烧杯中,用玻璃棒搅拌。
41、A是一种白色难溶于水的钙盐,由三种元素组成,其式量为100。
(1)用化学式表示:A ___________________,B ___________________
(2)写出A与盐酸反应的化学方程式:______________________________________
(3)D中含有的溶质可能有哪几种情况?
____________________________________________________________________
九、简答题(共14分)
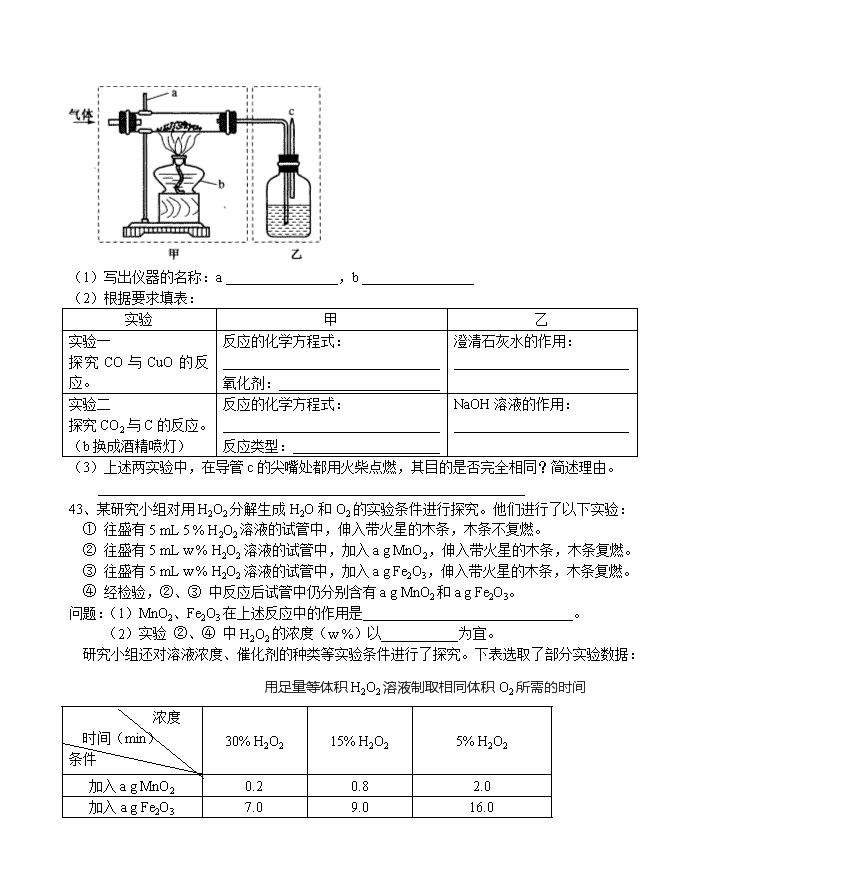
42、利用下图装置可进行气体性质的探究实验。甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液)。
(1)写出仪器的名称:a ________________,b ________________
(2)根据要求填表:
实验
甲
乙
实验一
探究CO与CuO的反应。
反应的化学方程式:
_______________________________
氧化剂:_______________________
澄清石灰水的作用:
_________________________
实验二
探究CO2与C的反应。
(b换成酒精喷灯)
反应的化学方程式:
_______________________________
反应类型:_____________________
NaOH溶液的作用:
_________________________
(3)上述两实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同?简述理由。
_____________________________________________________________
43、某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究。他们进行了以下实验:
① 往盛有5 mL 5 % H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
② 往盛有5 mL w % H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃。
③ 往盛有5 mL w % H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃。
④ 经检验,②、③ 中反应后试管中仍分别含有a g MnO2和a g Fe2O3。
问题:(1)MnO2、Fe2O3在上述反应中的作用是______________________________。
(2)实验 ②、④ 中H2O2的浓度(w %)以___________为宜。
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究。下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
浓度
时间(min)
条件
30% H2O2
15% H2O2
5% H2O2
加入a g MnO2
0.2
0.8
2.0
加入a g Fe2O3
7.0
9.0
16.0
问题:(3)从上表中能得出哪些结论?_______________________________________
_______________________________________________________________
十、本大题分为A、B两组,请在选定组的括号内打“√”。选A组的考生答B组不给分,选B组的考生答A组不给分,两组同时选择或同时不选,以A组为准。(共10分)
A组
44、某元素原子结构示意图为,则x的值为_________。根据元素原子结构示意图,不能直接获得的信息是________(填编号)。
① 核电荷数 ② 相对原子质量 ③ 电子层数 ④ 最外层电子数
45、将下列各组物质混合后溶于水,得到无色溶液的是———————————( )
A、NaNO3、NaCl、Na2SO4 B、MgCl2、NaOH、KNO3
C、CuSO4、CaCl2、MgCl2 D、BaCl2、AgNO3、KCl
46、某学生用250mL的集气瓶收集4瓶氧气,进行硫、红磷、木炭、铁丝的燃烧实验。
(1)为了得到干燥的氧气,可将氧气通过右图的洗气瓶。则洗气瓶中盛放的液体是_____________。
(2)写出铁丝在氧气中燃烧的实验现象:
______________________________________________
(3)写出红磷在氧气中燃烧的化学方程式:
______________________________________________
(4)若要制取本实验所需的4瓶氧气(),至少需要氯酸钾多少克?(精确到0.01g)
B组
44、下列物质中不属于化石燃料的是———————————————————( )
A、煤 B、石油 C、酒精 D、天然气
45、某学生在学习CO2的化学性质及实验室制法的原理后,联想起在实验室中用H2O2制取O2的实验。
(1)O2和CO2是否均能使用右图实验装置制取?_________
(2)若将制得的CO2通入水中,测得溶液的pH _____ 7。
(填“>”、“=”或“<”)
46、矿物燃料中常含有硫元素,在燃烧过程中会产生污染环境的SO2
气体,该气体可用氢氧化钙悬浊液吸收,生成难溶于水的亚硫酸钙(CaSO3)和水。
(1)亚硫酸钙(CaSO3)的摩尔质量是_________________,其中Ca、S、O元素的原子个数比为_________________;1mol CaSO3中约有___________________个硫原子。
(2)写出吸收SO2的化学反应方程式:__________________________________________
(3)根据上述化学反应,若要吸收32 g SO2气体,理论上需要__________mol Ca(OH)2。
2006年上海市初中毕业生统一学业考试理化试卷答案与评分标准化学部分
六、填表题(10分)
27、
铝
氧化镁
硝酸
Al
KOH
NaCl
※
氧化物
碱
酸
盐
※ 单质(金属)一列的名称和化学式对应无错别字可得2分,如不对应则得1分。
七、单项选择题(10分)
28
29
30
31
32
33
34
35
36
37
D
B
D
B
B
C
A
C
A
C
八、填空题(16分)
38、(1)N2 (2)CO2 (3)He (4)H2、CH4(本格共2分)
39、3 ; 分子间有间隙,当水和酒精分子混合后,相互渗入对方分子的间隙里,混合溶液的总体积就会减少。
40、② 2.5 ③ 50 mL、47.5
41、(1)A、CaCO3,B、CaO
(2)CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
(3)NaOH ; NaOH和Na2CO3 ; NaOH和Ca(OH)2 (本格共3分)
九、简答题(14分)
42、(1)铁架台、酒精灯
CO + CuO Cu + CO2
CuO
检验CO2气体
CO2 + C 2CO
化合反应(氧化还原反应)
除去(或吸收)CO2气体
(2)
(3)不完全相同,实验一的目的是除去有毒的CO尾气,防止污染(1分);实验二的主要目的是证明高温下CO2与C能反应,且产物为CO(1分)。(不写理由不给分,本格共2分)
43、(1)催化作用
(2)5 %
(3)相同条件下,MnO2的催化效果比Fe2O3好(1分);在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快。(1分)(本格共2分)
十、(10分)A组
44、11,②
45、A
46、(1)浓硫酸
(2)剧烈燃烧、火星四射;生成黑色固体。
(3)4P + 5O2 2P2O5
(4)氧气质量 = 4×0.25×1.43 = 1.43 g 1分
1分
x = 3.65 g 1分
B组:
44、C
45、(1)是
(2)<
46、(1)120 g/mol (本格2分);1:1:3;6.02×1023
(2)SO2 + Ca(OH)2 → CaSO3 + H2O 或SO2 + Ca(OH)2 → CaSO3↓+ H2O(本格2分)
(3)0.5
相关文档
- 浙江省杭州市2010年中考数学试卷及2021-05-1010页
- 上海市静安区、青浦区2014年中考数2021-05-1010页
- 2020年中考生物复习专题汇编 生命2021-05-107页
- 上海市杨浦区数学中考二模试卷与答2021-05-108页
- 2020年中考政治 交往艺术新思维知2021-05-103页
- 山东省青岛市中考化学试题及答案2021-05-109页
- 2020年中考语文二模试卷分类汇编 2021-05-104页
- 2019年中考语文真题汇编 02诗歌赏2021-05-106页
- 2019年中考语文真题分类汇编 文言2021-05-1013页
- 2020年中考语文真题试题(含解析) 新2021-05-1015页