- 2.01 MB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
北京市平谷区2014年九年级第一次模拟考试
化 学 试 卷
学校 班级 姓名 准考证号
考
生
须
知
1.本试卷共8页,共四道大题,35道小题,满分80分。考试时间100分钟。
2.在试卷和答题卡上准确填写学校名称、班级、姓名和准考证号。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.本试卷化学方程式中的“ ”和“ ”含义相同。
可能用到的相对原子质量
H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Ca40
一、选择题(每小题只有1个选项符合题意。共25个小题,每小题1分,共25分)
1.空气成分中,体积分数最大的是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
2.地壳中含量最多的金属元素是
A.硅 B.氧 C.铝 D.铁
3.下列变化中,属于化学变化的是
A.蜡烛燃烧 B.冰雪融化 C.香水挥发 D.干冰升华
4.碳酸钠可用于制造玻璃,其俗称是
A.小苏打 B.熟石灰 C.生石灰 D.纯碱
5.下列物质在氧气中燃烧,火星四射,有黑色固体生成的是
A.红磷 B.木炭 C.甲烷 D.铁丝
6.豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指
A.原子 B.分子 C.元素 D.单质
7.下列物质中,属于溶液的是
A.牛奶 B.豆浆 C.冰水 D.糖水
8.下列生活中的做法,不利于节约用水的是
A.用淘米水浇花 B.用洗过衣服的水冲马桶
C.隔夜的白开水直接倒掉 D.洗手打肥皂时暂时关闭水龙头
9.草木灰是一种农家肥料,其有效成分是K2CO3,它属于
A.钾肥 B.磷肥 C.氮肥 D.复合肥
10.下列物品所使用的材料中,属于有机合成材料的是
A.钛合金表链 B.紫砂壶 C.手机塑料外壳 D.真丝围巾
11.下列物质中,含有氧分子的是
A.O2 B.MnO2 C.CO2 D.H2O2
12.牙膏中的含氟化合物对牙齿有保护作用。一种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为
A.7 B.9 C.10 D.19
13.决定元素种类的是
A.核外电子数 B.中子数
C.最外层电子数 D.质子数
14.下列方法能鉴别氧气和空气的是
A.闻气味 B.将集气瓶倒扣在水中
C.观察颜色 D.将带火星的木条伸入集气瓶中
15.下列实验操作中,正确的是
A.加热液体 B.过滤 C.稀释浓硫酸 D.称量固体
16.下列物质溶于水时,溶液温度明显降低的是
A.氯化钠 B.硝酸铵
C.浓硫酸 D.氢氧化钠
17.下列是人体中几种体液的正常pH,酸性最强的是
A.胆汁(6.8~7.4) B.唾液(6.6~7.1)
C.血液(7.35~7.45) D.胃液(0.8~1.5)
18.将密封良好的方便面从平原带到高原时,包装袋鼓起,是因为袋内的气体分子
A.间隔增大 B.质量增大 C.体积增大 D.个数增多
19.下列物质露置于空气中,质量会减少的是
A.浓硫酸 B.浓盐酸 C.氢氧化钠 D.氯化钠
20.下列化学方程式书写正确的是
A.2P + 5O2 P2O5 B.2NaOH + H2SO4 Na2SO4 + H2O
C.CO2 + Ca(OH)2 CaCO3↓+H2O D.2Fe + 6HCl 2FeCl3 + 3H2↑
21.下列实验方案中,能达到实验目的的是
选项
实验目的
实验方案
A
分离碳酸钠和氢氧化钠的混合物
加入过量氢氧化钙溶液,过滤
B
除去氯化钠固体中的少量碳酸钠
加入适量稀硫酸,充分反应后,蒸发
C
检验一氧化碳气体中含有少量的二氧化碳
澄清石灰水,观察澄清石灰水的变化
D
鉴别氯化钠溶液、氢氧化钠溶液和稀盐酸
各取少量溶液于试管中,分别滴加无色酚酞溶液,观察溶液颜色的变化
22.氨基酸分子中含有氨基(—NH2,具有碱的性质)和羧基(—COOH,具有酸的性质)。
氨基酸分子具有的性质是( )
A.只能与硫酸反应,不能与氢氧化钠反应 B.只能与氢氧化钠反应,不能与硫酸反应
C.既能与硫酸反应,又能与氢氧化钠反应
D.既不能与硫酸反应,又不能与氢氧化钠反应
23.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是①②③④⑤
资料:A的溶解度
温度/℃
20
30
40
50
60
溶解度/g
37.2
41.4
45.8
50.4
55.2
A.②中A的质量分数最大
B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液
D.①③④⑤中没有固体存在
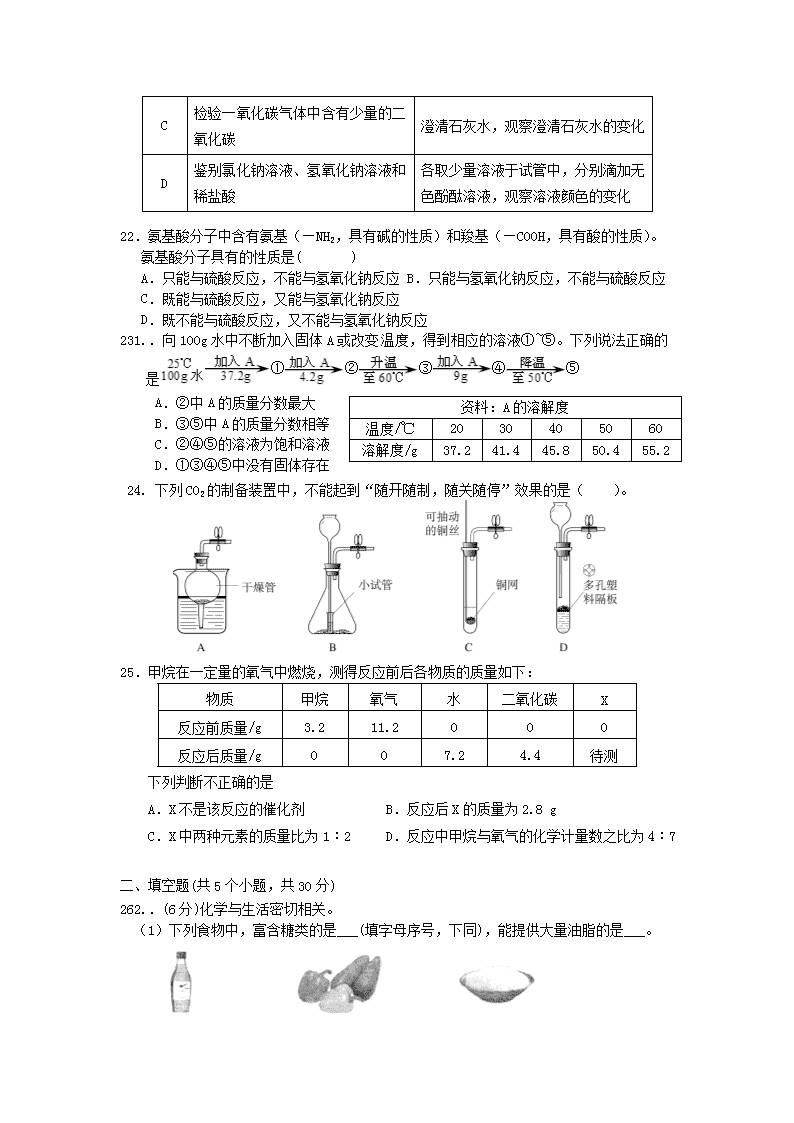
24. 下列CO2的制备装置中,不能起到“随开随制,随关随停”效果的是( )。
25.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下:
物质
甲烷
氧气
水
二氧化碳
X
反应前质量/g
3.2
11.2
0
0
0
反应后质量/g
0
0
7.2
4.4
待测
下列判断不正确的是
A.X不是该反应的催化剂 B.反应后X的质量为2.8 g
C.X中两种元素的质量比为1︰2 D.反应中甲烷与氧气的化学计量数之比为4︰7
二、填空题(共5个小题,共30分)
26.(6分)化学与生活密切相关。
(1)下列食物中,富含糖类的是___(填字母序号,下同),能提供大量油脂的是___。
A.橄榄油 B.蔬菜 C.米饭
(2)下列服装所使用的材料中,属于有机合成材料的是________(填字母序号)。
A.纯棉帽子 B.羊毛衫 C.涤纶运动裤
(3)食用下列食品有损身体健康的是____________(填字母序号)。
A. 用纯碱和发酵的面团蒸制的馒头 B. 霉变的大米 C. 用甲醛浸泡过鸡翅
(4)汽车是重要的交通工具。
充电
①汽车使用天然气作燃料,排放污染较低。天然气的主要成分为________。
②完成车用铅酸电池充电的反应:2PbSO4 + 2H2O Pb + 2H2SO4 + _______。
27.(5分)物质的用途与其性质密切相关。
(1)干冰常用作制冷剂,是因为干冰易________。
(2)活性铁粉常用作食品双吸剂,利用它可以吸收食品包装袋内的________。
(3)熟石灰常用来处理泄漏的硫酸,其原因是(用化学方程式表示)________。
(4)碳酸氢钠可用于治疗胃酸(主要成分是盐酸)过多,其原因是(用化学方程式表示)________。
(5)硅是信息技术的关键材料。高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,同时生成氯化氢。该反应的化学方程式为________。
28、(6分)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其微观示意图如下所示:
C D
催化剂
氮原子
氧原子
反应后
反应前
△
A B
氢原子
(1)上述化学反应过程中,属于氧化物是 _________(填序号);
(2)A物质中氮元素的化合价为_________价,在化学反应前后,元素化合价没有发生改变的是__________元素;
(3)该反应的化学方程式为______________,其基本反应类型属于___________。
(4) 参加反应的A与B的最简整数质量比为 。
29.(7分)金属在生产和生活中有广泛的应用。
(1)下列金属制品中,利用金属导电性的是 (填字母序号)。
A.黄金饰品 B.铝蒸锅 C.铜导线
(2)钢铁生锈的条件是 。
(3)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为 。
(4)利用废旧电池铜帽(含 Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流
程如下(反应条件已略去):
①过程Ⅱ中分离操作的名称是 。
②过程Ⅲ中有气体产生,反应的化学方程式为 。
③A~E 中含铜、锌两种元素的物质有 (填字母序号)。
30.(6分)依据表中的元素所组成初中化学常见的物质,回答下列问题。
元素名称
氢
碳
氧
氯
钠
钙
元素符号
H
C
O
Cl
Na
Ca
(1)A、B组成元素相同,一定条件下可发生反应A→B+C,则C物质是______。
(2)D、E、F含有相同的金属元素,F俗称小苏打,已知在溶液中D与F反应生成E和B,则该反应的化学方程式为_____________________。
(3)向某红色溶液中滴加D溶液,溶液颜色经历红色→紫色→蓝色的变化过程,且无气体、无沉淀产生。则原红色溶液中的溶质是_______________,D物质是______________。
(4)向X物质的饱和溶液中加入物质Y,溶液变混浊,在向其中加入足量稀盐酸,溶液变澄清、无气体产生。则溶液变混浊的原因是__________[填序号]。
①X是Ca(OH)2、加入的物质Y是CO2,二者发生反应生成CaCO3;
②X是Na2CO3、加入的物质Y是Ca(OH)2,二者发生反应生成CaCO3;
③X是Ca(OH)2、加入的物质Y是CaO,CaO与水反应消耗溶剂使Ca(OH)2析出;
④X是Ca(OH)2、加入的物质Y是CaO,CaO与水反应生成的Ca(OH)2不能再溶解;
⑤X是Ca(OH)2、加入的物质Y是CaO,CaO与水反应放热使Ca(OH)2溶解度减小而析出;
三、实验题(共3个小题,共19分)
31.(6分)根据下图回答问题。
A B C D E
⑴实验仪器a的名称是________。
⑵实验室用高锰酸钾制取氧气的化学方程式为______________________________,所选用的发生装置是____(填字母序号,下同)。
⑶实验室用过氧化氢溶液和二氧化锰制取氧气是,二氧化锰起__________作用,所选用的收集装置是____或E。
⑷用排空气法收集一瓶氧气,验满时将带火星的木条放在瓶口,若观察到__________,说明瓶中已充满氧气。
32.(5分)某化学小组在课外活动时利用下图装置进行实验 (图中铁架台等仪器已略去)。
稀盐酸
石灰石
(1)若乙中盛有澄清的石灰水,通过分液漏斗加入稀盐酸后关闭活塞,同时打开止水夹,看到乙试管液体中有气泡冒出,澄清的石灰水未变混浊。
①写出甲中发生反应的化学方程式:_____________。
②澄清石灰水未变浑浊的可能原因是(用化学方程式表示)_____________。
(2)若乙中盛有NaOH溶液,通过分液漏斗加入稀盐酸后关闭活塞,同时打开止水夹,乙中未观察到明显现象;一会儿后再关闭止水夹,发现甲中液体流入乙中,乙中有气泡产生最终得到无色溶液。
①写出乙中产生气泡的化学方程式_______________。
②乙中所得无色溶液中的溶质是_________________(写出所有可能)。
33.(8分)NaOH能与CO2发生化学反应,其反应的化学方程式为________。然而,在化学课上老师向NaOH溶液通入CO2后无明显现象。提出问题:如何通过实验证明CO2与NaOH发生了反应。
【查阅资料】
①CaCl2溶液可与Na2CO3溶液发生复分解反应。
②向CaCl2溶液中通入CO2,无明显现象;在水溶液中CaCl2不与CO2、H2CO3等物质反应。
【实验一】证明反应物之一CO2消失了
(1)同学门设计了如右图所示的实验,打开分液漏斗活塞。向充满CO2的广口瓶中滴入NaOH溶液。一会儿后可观察到的实验现象是___________________。并据此现象判断NaOH与CO2发生了化学反应。
(2)老师提出上述实验不足以证明NaOH与CO2发生了化学反应。其理由是____________________。据此,你认为上述实验应做的改进是_____________________ 。
气球
【实验二】证明有新物质Na2CO3生成
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案一:打开瓶塞,向实验一所得的溶液中加入饱和的石灰水,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
(1)写出方案二发生反应的化学方程式:___________________________。
(2)你认为上述实验方案不可行的是________,理由是______________________________。
四、计算题(共2个小题,共6分。)
34.(3分)汽车尾气系统中使用催化转化器,可降低CO、NO等有毒气体的排放,其反应化学方程式为:2CO+2NO2CO2+N2,当有2.8gCO被转化时,计算同时被转化的NO的质量。
35.(3分)将Na2CO3和NaCl固体混合物32.9g放入烧杯中,此时总质量为202.9g,加入326.9g盐酸,恰好完全反应,待没有气泡逸出后再次称量,总质量为521.0g。计算所得溶液中溶质的质量分数(CO2的溶解忽略不计)。
北京市平谷区2014年初三第一次模拟考试
化学试卷参考答案及评分标准
一、选择题(每小题1分,共25分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
A
C
A
D
D
C
D
C
A
C
A
B
D
题号
14
15
16
17
18
19
20
21
22
23
24
25
答案
D
A
B
D
A
B
C
C
C
C
D
C
二、填空题(未标分数的空,每空1分,共30分)
26.(6分)
(1)C,A (2)C
(3)BC (4)①CH4 ②PbO2
27.(5分)
(1)升华吸热 (2)水和氧气
(3)Ca(OH)2+H2SO4=CaSO4+2H2O (4)NaHCO3+HCl=NaCl+H2O+CO2
(5)SiCl4+2H2=4HCl+Si(条件高温)
28.(6分)
(1)D (2)+3,H;
(3)4NH3+3O2=2N2+6H2O(条件加热、催化剂),置换。
(4) 17:24
29. (7分)
(1)C (2)与水和氧气同时接触
(3)3CO + Fe2O3 高温 2Fe+3CO2
(4) ①过滤 ②Zn+H2SO4=ZnSO4+H2 ③AC (该空两分)
30.(6分)
(1)O2 (2)NaHCO3+NaOH=Na2CO3+H2O
(3)稀盐酸,酚酞。NaOH
(4) 345(该空两分)
三、实验题(未标分数的空,每空1分,共19分)
31.(6分)
(1)酒精灯
(2)2KMnO4 △ K2MnO4 + MnO2 + O2↑ A
(3)催化,C
(4)木条复燃
32.(5分)
(1)①CaCO3+2HCl=CaCl2+H2O+CO2 ②Ca(OH)2+2HCl= 2H2O+CaCl2
(2)①Na2CO3+2HCl=2NaCl+H2O+CO2 ②CaCl2、HCl、NaCl;CaCl2、NaCl。(两分)
33.(8分)
CO2+2NaOH=Na2CO3+H2O
(1)气球变鼓
(2
)二氧化碳能溶于水,也能使气球变鼓,不能证明二氧化碳与氢氧化钠发生了反应。改进:设计对比试验,用同样体积的水与同样的二氧化碳,观察气球的形变。
【实验二】
(1)CaCl2+ Na2CO3= CaCO3+ 2NaCl
(2)方案一,理由是装置中有剩余的二氧化碳气体,水中也能溶解部分二氧化碳,能使
澄清的石灰水变浑浊。(该空两分)
四、计算题(每小题3分,共6分)
34.解:设被转化的NO的质量为x。
2CO+2NO2CO2+N2
56 60
2.8g x
= x==3g
答:被转化的NO的质量为6g
35.解:反应生成的CO2质量=202.9g+326.9g-521.0g=8.8g
设Na2CO3的质量为x,生成的NaCl的质量为y。
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 8.8g
x=21.2g y=23.4g
所得溶液中溶质的质量分数=×100%=10%
答:所得溶液中溶质的质量分数为10%。