- 2.17 MB
- 2021-05-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2017学年嘉定区第一学期期末考试九年级化学试卷
化学部分
考生注意:1.本试卷化学部分含三个大题。
2.答题时务必按要求在答题纸规定的位置上做答,在草稿纸、本试卷上答题一律无效。
可能用到的相对原子质量:C-12 H-1 O-16 Ca—40
六.单项选择题(共20分)
下列各题均只有一个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
27.属于化学变化的是
A.燃放烟花 B.冰雪融化 C.灯泡发光 D.石蜡熔化
28.物质化学式的读法和写法都正确的是
A.氯化钠 NaCl B.碳酸钠NaCO3 C.氢氧化钠Na(OH)2 D.氧化铁FeO
29.属于纯净物的是
A.洁净空气 B.可乐 C.大理石 D.蒸馏水
30.空气成分中,体积分数最大的是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
31.不属于碳元素的同素异形体的是
A.金刚石 B.石墨 C.二氧化碳 D.C60
32.物质在氧气中燃烧的实验现象描述错误的是
A.铁丝:生成黑色固体 B.木炭:发出白光
C.硫:有刺激性气味 D.镁:生成氧化镁固体
33.将少量物质分别放入水中,充分搅拌后能形成溶液的是
A.泥土 B.面粉 C.白糖 D.汽油
34.pH是水质检验的重要指标之一。下列水样中,酸性最强的是
A.pH = 5.6的雨水 B.pH = 1.3的工业废水
C.pH = 7.0的蒸馏水 D.pH = 7.3的矿泉水
35.下列方法不能鉴别氧气和二氧化碳的是
A.将集气瓶倒扣在水中 B.将澄清的石灰水倒入集气瓶中
C.观察气体颜色 D.将带火星的木条伸入集气瓶中
36.实验操作正确的是
A.倾倒液体 B.滴加液体 C.蒸发食盐水 D.加热液体
37.根据质量守恒定律,电解NaCl的水溶液,不可能得到的生成物是
A.H2 B.C12 C.Na2CO3 D.NaOH
38.化学方程式书写正确的是
A.CuSO4 + H2OCuSO4·5 H2O B.P + O2PO2
C.S+ O2SO2↑ D.CH4+2O2CO2+2H2O
39.关于教材中各图表提供的信息或应用的说法中,错误的是
A.根据相对原子质量表,可进行物质摩尔质量的计算
B.根据溶解度曲线图,可选择从溶液中获得晶体的方法
C.根据常见气体的密度,可选择能否用排水法收集气体
D.根据元素的化合价,可判断某化学式书写的正误
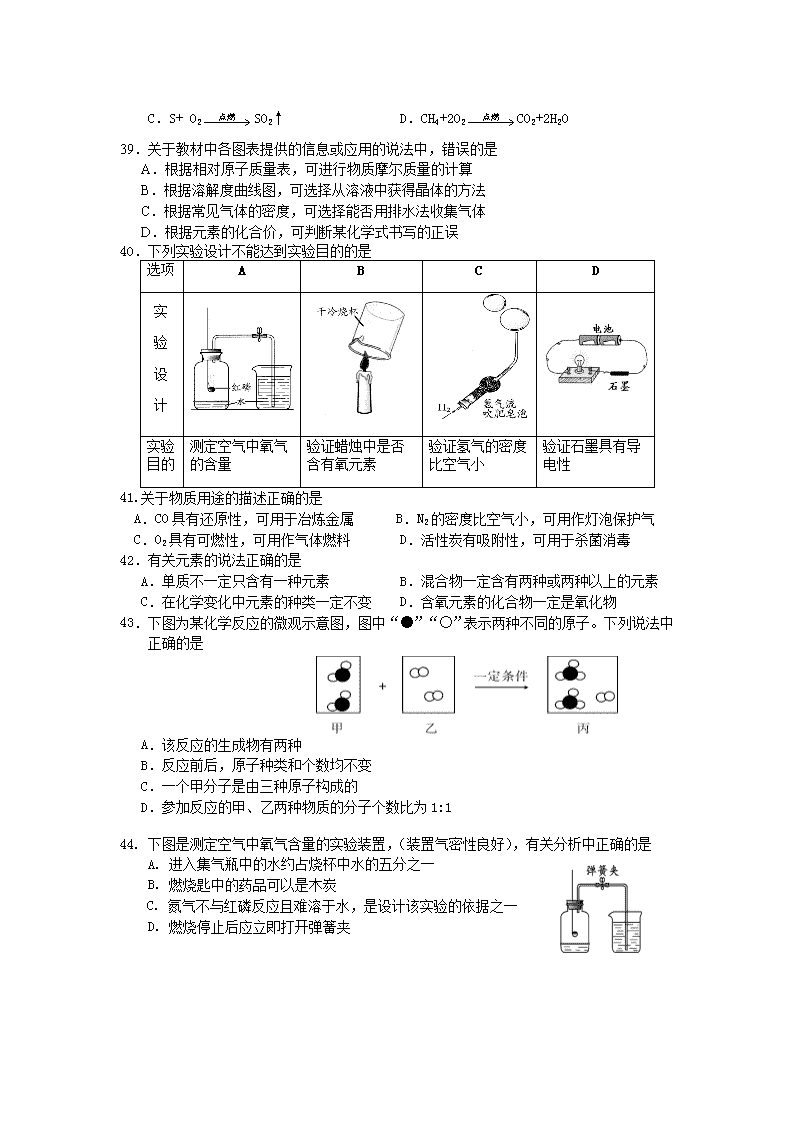
40.下列实验设计不能达到实验目的的是
选项
A
B
C
D
实
验
设
计
实验目的
测定空气中氧气的含量
验证蜡烛中是否含有氧元素
验证氢气的密度比空气小
验证石墨具有导电性
41.关于物质用途的描述正确的是
A.CO具有还原性,可用于冶炼金属 B.N2的密度比空气小,可用作灯泡保护气
C.O2具有可燃性,可用作气体燃料 D.活性炭有吸附性,可用于杀菌消毒
42.有关元素的说法正确的是
A.单质不一定只含有一种元素 B.混合物一定含有两种或两种以上的元素
C.在化学变化中元素的种类一定不变 D.含氧元素的化合物一定是氧化物
43.下图为某化学反应的微观示意图,图中“●”“○”表示两种不同的原子。下列说法中正确的是
A. 该反应的生成物有两种
B.反应前后,原子种类和个数均不变
C.一个甲分子是由三种原子构成的
D.参加反应的甲、乙两种物质的分子个数比为1:1
44. 下图是测定空气中氧气含量的实验装置,(装置气密性良好),有关分析中正确的是
A. 进入集气瓶中的水约占烧杯中水的五分之一
B. 燃烧匙中的药品可以是木炭
C. 氮气不与红磷反应且难溶于水,是设计该实验的依据之一
D. 燃烧停止后应立即打开弹簧夹
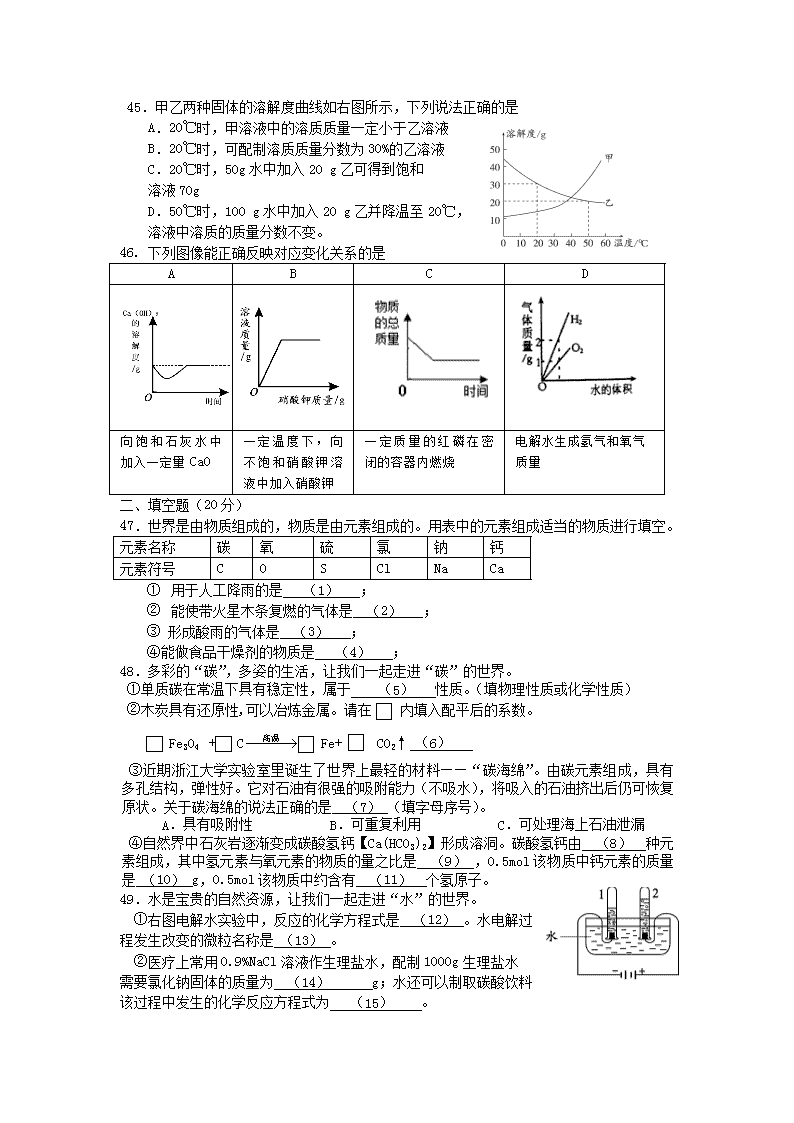
45.甲乙两种固体的溶解度曲线如右图所示,下列说法正确的是
A.20℃时,甲溶液中的溶质质量一定小于乙溶液
B.20℃时,可配制溶质质量分数为30%的乙溶液
C.20℃时,50g水中加入20 g乙可得到饱和
溶液70g
D.50℃时,100 g水中加入20 g乙并降温至20℃,
溶液中溶质的质量分数不变。
46. 下列图像能正确反映对应变化关系的是
A
B
C
D
向饱和石灰水中加入一定量CaO
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
一定质量的红磷在密闭的容器内燃烧
电解水生成氢气和氧气质量
二、填空题(20分)
47.世界是由物质组成的,物质是由元素组成的。用表中的元素组成适当的物质进行填空。
元素名称
碳
氧
硫
氯
钠
钙
元素符号
C
O
S
Cl
Na
Ca
① 用于人工降雨的是 (1) ;
② 能使带火星木条复燃的气体是 (2) ;
③ 形成酸雨的气体是 (3) ;
④能做食品干燥剂的物质是 (4) ;
48.多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
①单质碳在常温下具有稳定性,属于 (5) 性质。(填物理性质或化学性质)
②木炭具有还原性,可以冶炼金属。请在 内填入配平后的系数。
Fe3O4 + C Fe+ CO2↑ (6)
③近期浙江大学实验室里诞生了世界上最轻的材料——“碳海绵”。由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。关于碳海绵的说法正确的是 (7) (填字母序号)。
A.具有吸附性 B.可重复利用 C.可处理海上石油泄漏
④自然界中石灰岩逐渐变成碳酸氢钙【Ca(HCO3)2】形成溶洞。碳酸氢钙由 (8) 种元素组成,其中氢元素与氧元素的物质的量之比是 (9) ,0.5mol该物质中钙元素的质量是 (10) g,0.5mol该物质中约含有 (11) 个氢原子。
49.水是宝贵的自然资源,让我们一起走进“水”的世界。
①右图电解水实验中,反应的化学方程式是 (12) 。水电解过程发生改变的微粒名称是 (13) 。
②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水
需要氯化钠固体的质量为 (14) g;水还可以制取碳酸饮料该过程中发生的化学反应方程式为 (15) 。
③某化学兴趣小组欲进行粗盐的初步提纯。
粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、 (16) 、a(填编号)。
若NaCl的产率偏低,则可能的原因是 (17) (填字母)。
A.过滤时滤纸有破损 B.蒸发后所得精盐未完全蒸干,含有水。
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:
④已知KCl的溶解度20°C时为34 g/100g水,40°C时为40 g/100g水。某实验小组做了如
下实验。
D
加入
25 gKCl
加热
到40℃
B
C
E
A
再加入
25 gKCl
冷却
至20℃
再加入
25 g H2O
20℃
40℃
20℃
100gH2O
A中所得溶液中溶质与溶剂的质量比为 (18) ;
溶质的质量分数相等的是 (19) 。
Ⅰ.B和C Ⅱ.B和E Ⅲ.C和D Ⅳ.D和E
八、简答题:(共20分)
50.小明来到实验室完成氧气和二氧化碳气体的制取实验,请按照要求答问题:
① 实验台前有如下仪器和药品,请写出仪器A的名称:A (1)
小明利用上述仪器和药品可以做制取氧气的实验,实验前他发现其中缺少一种药品,
该药品是 (2) ;该反应的原理是(用化学方程式表示) (3) 。
② 下表是小明制取二氧化碳的主要步骤及相关实验装置,其中 (4) (填字母序号)步骤中的实验装置有错误,改正的方法是 (5) 。
改正后进行实验,这些步骤的正确操作顺序是 (6) (填字母序号)
实验
步骤
a.制备气体
b.收集气体
c.检查装置气密性
d.清洗仪器、整理桌面
相关
实验
装置
③上述装置改进成右图甲装置制取二氧化碳气体,甲装置的优点
是 (7) 。请简述甲装置中长颈漏斗的作用 (8) 。
④右图乙是一个气密性良好的启普发生器也可制取二氧化碳气体,反应一段时间后关闭活塞K,不可能观察到的现象是 (9) 。
(A)固液接触,无气泡产生
(B)固液接触,仍有气泡产生
(C)M中液面不断下降、N中液面不断上升
(D)N中液面下降至L中
⑤用大理石与稀盐酸反应制备CO2,滴加盐酸后,产生了4.4克二氧化碳,这些二氧化碳的物质的量为 (10) ,计算反应消耗HCl的物质的量。(根据化学方程式列式计算) (11) 。
51. 有一无色气体,可能是由CO、CO2、H2O(水蒸气)中的一种或几种组成。为确定其组成,某同学按下列方案进行实验,请回答下列问题
①若观察到 (12) 现象,说明氧化铜发生了还原反应,证明原无色气体中一定含有一氧化碳。写出装置A中的化学反应方程式 (13) 。
②若观察到B中无水硫酸铜不变色,则无色气体中一定不含有 (14) 。
③若观察到澄清石灰水变浑浊,写出C装置中的化学反应方程式 (15) 。[
来由此现象,并不能确定原无色气体中有二氧化碳,理由是 (16) 。
④从保护环境的角度分析,本实验的不足是 (17) 。
参考答案:
一、选择题(20分)
27
28
29
30
31
32
33
34
35
36
A
A
D
A
C
D
C
B
C
C
37
38
39
40
41
42
43
44
45
46
C
D
C
B
A
C
B
C
D
A
二、填空题(20分)
题号
小题号
答案
分值
备注
47
1
二氧化碳或CO2
1分
2
氧气或O2
1分
3
二氧化硫或SO2
1分
4
氧化钙或CaO
1分
48
5
化学性质
1分
6
1,2,3,2
1分
7
A B C
1分
全对得分
8
四
1分
9
1:3
1分
10
20
1分
11
6.02×1023
1分
49
12
通电
2H2O → 2H2↑+ O2↑
1分
13
水分子
1分
14
9
1分
15
CO2 + H2O → H2CO3
1分
16
cbde
1分
17
C
1分
18
1:4
1分
19
Ⅱ、Ⅲ
2分
错一个扣一分,扣完为止
三、简答题(20分)
题号
小题号
答案
分值
备注
50
1
铁架台
1分
错别字不给分
2
二氧化锰或MnO2
1分
3
2H2O22 H2O +O2↑
1分
4
a
1分
5
将长颈漏斗的下端插入液面以下
1分
合理得分
6
c a b d
1分
7
随开随用,随关随停
1分
合理得分
8
开始时加入盐酸,反应停止后盐酸回流其中
2分
表达完整得2分
9
C
1分
10
0.1mol
1分
单位不写不得分
11
设:盐酸中氯化氢为x mol
CaCO3 +2HCl →CaCl2 +H2O + CO2↑(1分)
2 1
Xmol 0.1mol
(1分)
X=0.2mol(1分)
答:略
3分
51
12
黑色粉末变成红色
1分
13
CO+ CuOCu + CO2
1分
14
H2O
1分
15
CO2+Ca(OH)2→CaCO3↓+ H2O
1分
16
可能是一氧化碳与氧化铜反应产生的二氧化碳
1分
合理得分
17
没有尾气处理
1分
合理得分